锂离子电池(Lithium-IonBattery,简称LIB)是当今电子设备、便携式电源乃至电动汽车中最为常见的电池类型。其化学原理虽显复杂,但一旦解开其背后的科学,便能深刻理解为什么锂离子电池如此受到青睐。今天,我们就来深入探讨一下锂离子电池的化学原理,揭开它如何通过科学的魔法,成为现代社会不可或缺的能源提供者。
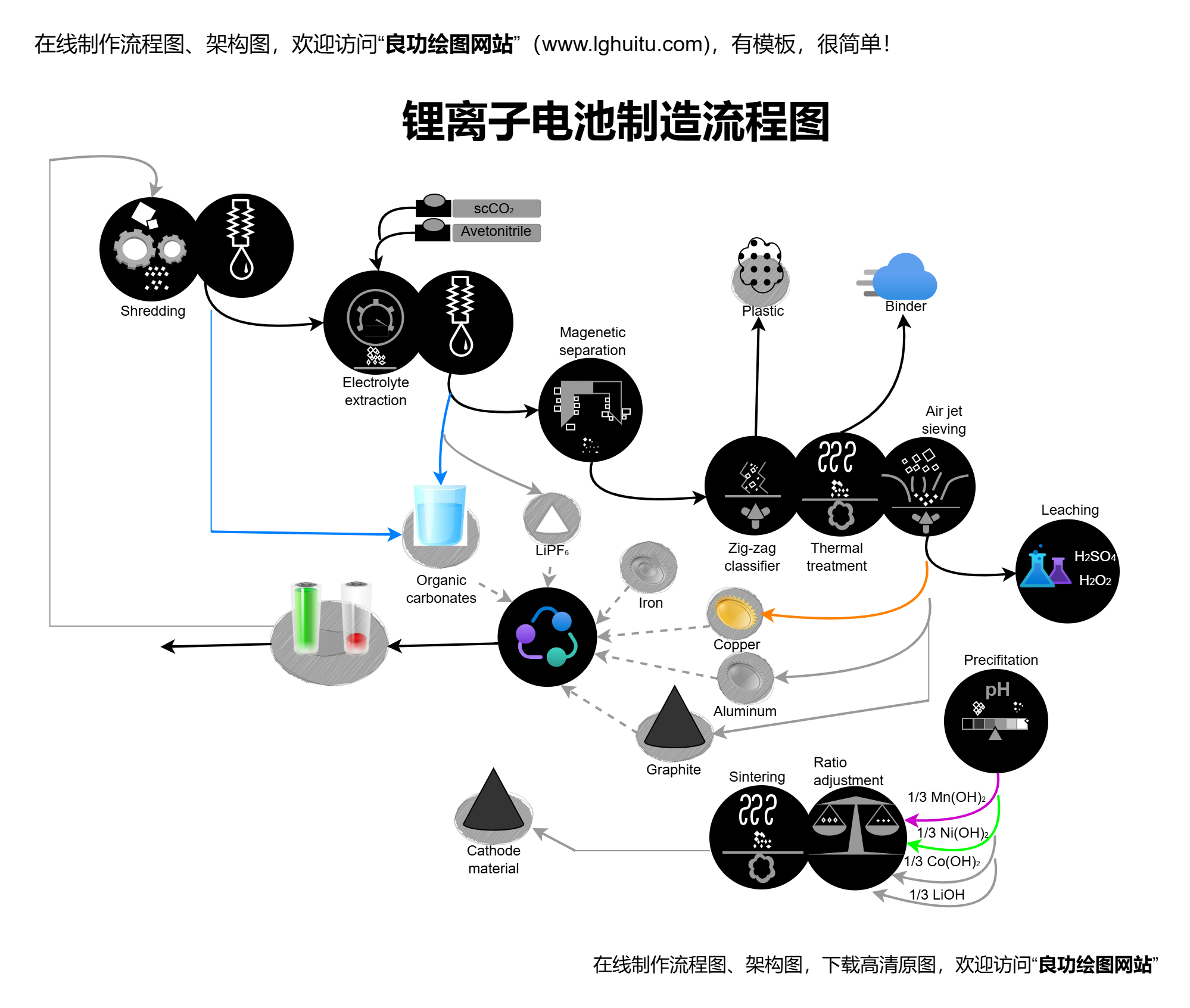
锂离子电池是一种二次电池(可充电电池),它的工作原理与电池内部的锂离子在电解液中的迁移密切相关。锂离子电池主要由正极、负极、电解液和隔膜组成。正极通常由锂金属氧化物(如LiCoO₂)构成,负极通常使用石墨(Graphite)材料。电解液则是由锂盐(如LiPF₆)溶解在有机溶剂(如碳酸二甲酯)中,起到导电的作用。
当锂离子电池充电时,电流通过外部电路,正极的锂离子通过电解液迁移至负极,在负极的石墨层中嵌入并储存。这一过程称为“插层”。负极上的石墨层具有丰富的空隙结构,可以轻松地吸附锂离子。当电池充满电时,正极的锂离子几乎完全被移至负极。
而当电池开始放电时,锂离子会从负极的石墨层中脱离,重新通过电解液移动回正极,同时释放电子,形成电流供给外部负载。电池放电过程中,锂离子在电解液中的迁移与电子的流动同步进行,最终完成一次完整的能量释放过程。
可以看出,锂离子电池的化学反应本质上是锂离子在电池内部不同电极之间的来回迁移。电池的高效能和较长的使用寿命正是源于锂离子能够在充电和放电过程中迅速而稳定地嵌入和脱离石墨负极,并且反复进行这一过程。相较于其他类型的电池(如铅酸电池),锂离子电池的能量密度更高,体积更小,重量更轻,成为了便携设备和电动交通工具的首选。
锂离子电池的这一特性并非偶然,它得益于锂金属的独特性质。作为一种轻质金属,锂的标准电极电位非常低,这意味着它能很容易地释放出电子并与其他物质发生化学反应。在电池的正极,锂金属氧化物的氧化还原反应提供了大量的电子和离子,从而释放出能量。而在负极,石墨的层状结构为锂离子的嵌入提供了理想的空间,保证了锂离子能够高效存储。
从技术发展的角度来看,锂离子电池的能量密度与电池的充电速度和使用寿命密切相关。随着技术的不断进步,电池的能量密度逐渐提高,这不仅能够使便携式设备更加轻薄,也让电动汽车的续航能力不断增强。未来,锂离子电池还将继续发展,逐步克服当前面临的挑战,如电池寿命的延长、充电速度的提升以及成本的降低等。
除了高能量密度和长寿命,锂离子电池还具备其他一些重要的化学特性,使其在现代科技中占据着不可替代的地位。例如,锂离子电池的高电压是其另一个显著优势。典型的锂离子电池的电压范围通常在3.2V到4.2V之间,这比许多传统电池的电压更高,从而能为各种电气设备提供足够的能量。锂离子电池相对较低的自放电率也是其一大优势,这意味着即便在长时间不使用的情况下,电池的电量也能保持较为稳定的状态。
锂离子电池并非没有挑战。目前,最主要的技术瓶颈之一是电池的安全性。在充电和放电的过程中,锂离子电池内部的电解液可能会发生气体膨胀,甚至在极端情况下可能导致电池起火或爆炸。这一问题的根源在于电池内部的热量积累与电池内部物质的化学反应。为了应对这一问题,研究人员正在不断优化电池的设计,包括改进电解液的稳定性、开发更为耐高温的电池材料、以及增强电池外壳的安全性。
随着全球对环保问题的日益关注,锂离子电池的回收问题也日益凸显。尽管锂离子电池在使用过程中能够高效转换能量,但电池的使用寿命终究有限。如何实现电池的高效回收,避免资源浪费和环境污染,成为了业界亟待解决的问题。幸好,随着技术的不断进步,锂离子电池的回收技术已经取得了一些突破,越来越多的企业开始投入到电池回收的研发中。通过回收电池中的锂、钴、镍等重要金属,不仅能够减少对自然资源的依赖,还能有效降低电池生产的环境影响。
锂离子电池作为一种绿色能源技术,其优势远不止于高效能和长寿命。它对于推动全球清洁能源的应用,促进电动汽车的普及,甚至推动可再生能源的使用都有着不可忽视的贡献。随着锂离子电池技术的不断发展,未来的电力存储将更加智能化、绿色化,进一步助力全球实现碳中和目标。
锂离子电池的化学原理虽然充满复杂的物理和化学反应,但其背后的科技创新和应用却在改变着我们的世界。从日常使用的智能手机到未来绿色出行的电动汽车,锂离子电池的科技奇迹正在不断开创更美好的未来。