2020年发布的《药品注册管理办法》是我国药品管理制度的一次重要修订。作为药品研发和生产的基础性法规之一,新版办法在多个方面作出了深刻改革。本文将从几个关键方面为您详细解读这些变化,以及它们对药品行业的深远影响。
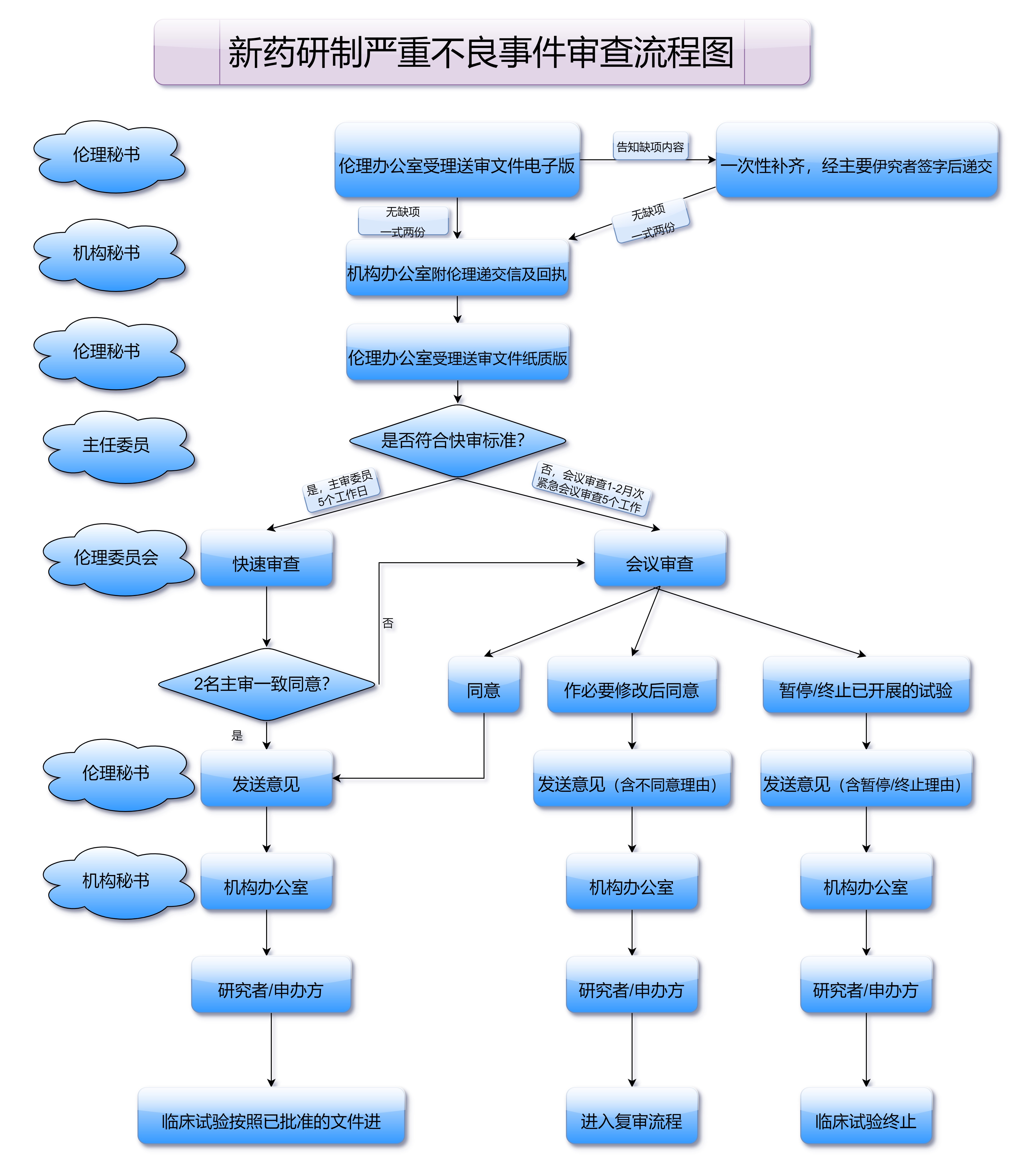
最重要的变化之一就是药品注册流程的简化和审批效率的提高。新的办法明确提出了药品注册的一系列新的规定,其中最为显著的是加快了药品上市审批的速度。以前,药品的注册周期通常较长,尤其是创新药品往往需要耗费数年之久才能完成注册。新版《药品注册管理办法》引入了优先审评和绿色通道等机制,对于符合特定条件的药品,审批速度可以大幅提升。

例如,对于创新药、临床急需药品,或者是治疗重大疾病的药物,将享有优先审评的权利。这一措施使得更多有潜力的药品能够迅速进入市场,满足患者的需求,尤其是在抗癌、罕见病等领域的应用,极大地提升了患者的生存质量。
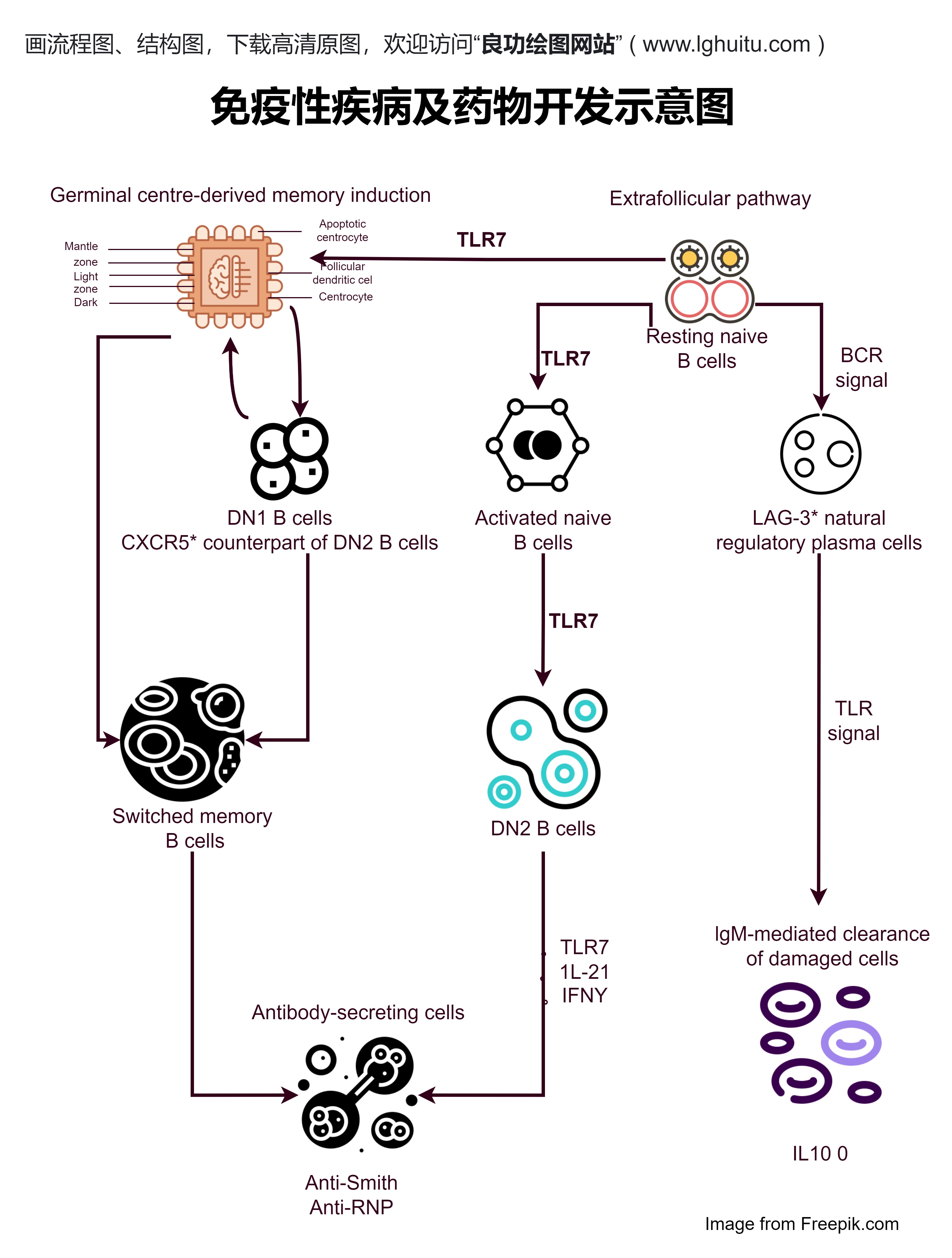
随着医疗技术的不断进步,药品创新成为全球药品市场的重要发展趋势。新版《药品注册管理办法》明确加强了对创新药品的支持,鼓励药品研发企业加大对新药的投入,推动更多原创药品进入市场。
为了更好地支持创新药品的研发,办法提出了一些新的注册要求。例如,对于进口药品的注册,新办法简化了审批程序,并且在一定程度上放宽了数据要求。特别是在临床试验数据方面,若符合条件的药物能够获得国外相关机构的临床数据,国内审评部门可以考虑直接采纳。这样不仅能减少重复试验的资源浪费,也能加快药品的临床研究和批准速度。
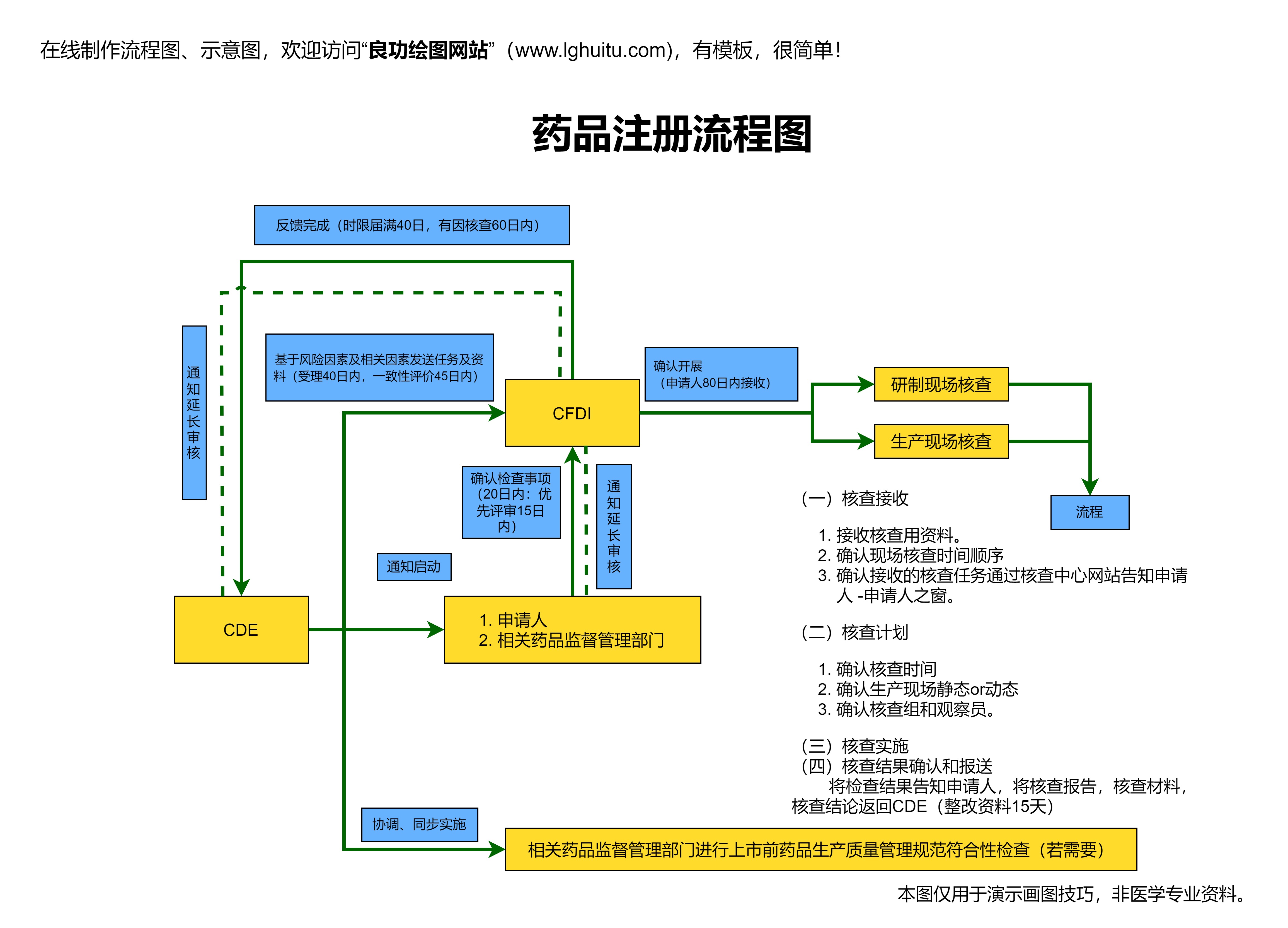
临床试验是药品注册过程中至关重要的一环。在新版的《药品注册管理办法》中,临床试验的要求和监管得到了进一步加强。新版办法明确了药品临床试验的相关规定,包括试验方案的审批流程、试验数据的标准化要求等。办法还特别强调了临床试验伦理审查的加强,确保试验过程中对患者的安全和权益有充分的保障。
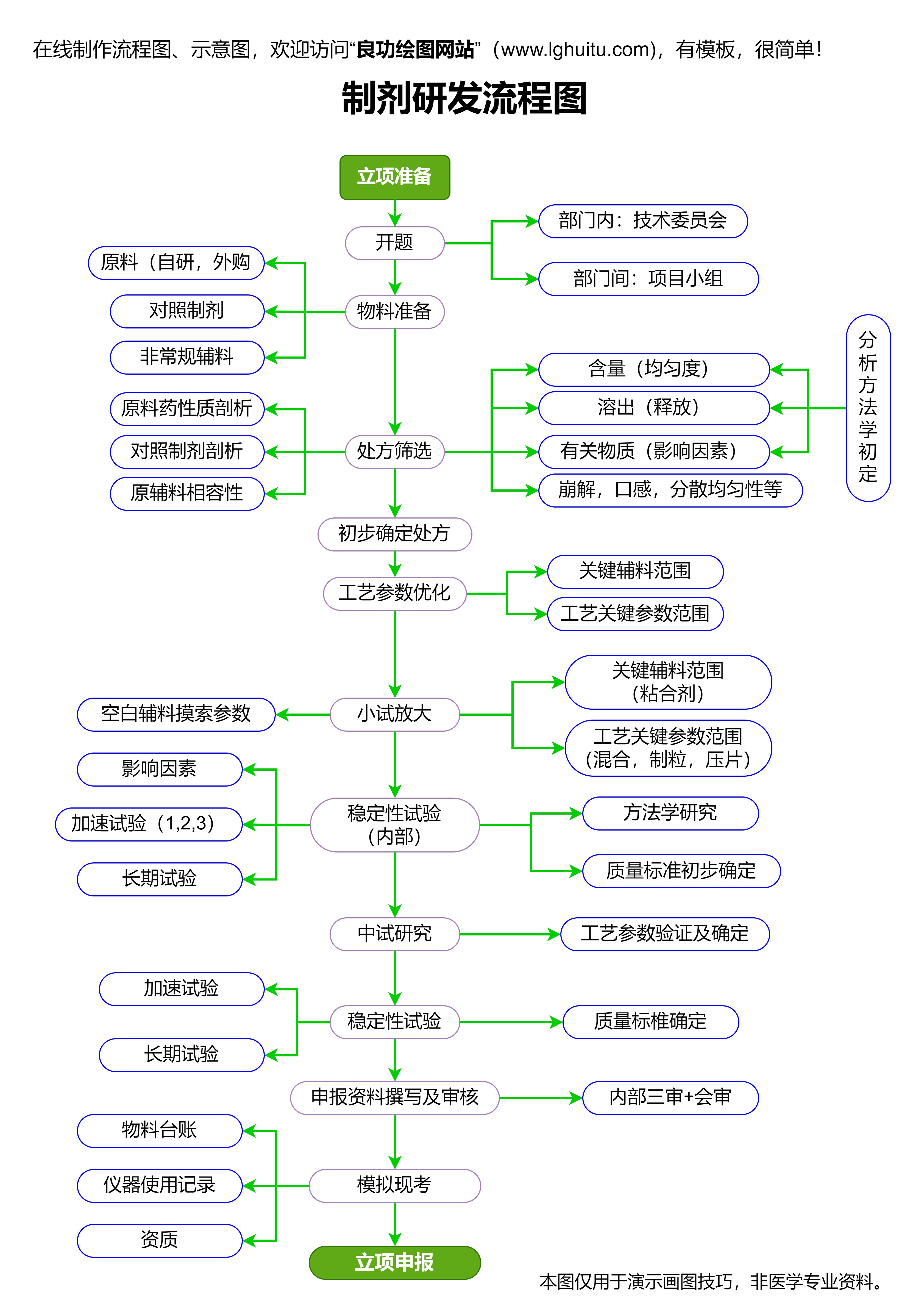
这项规定的出台,不仅提高了临床试验的质量,也为药品的上市创造了更为严格和规范的前提。通过科学、规范的临床试验,能够有效地保证上市药品的安全性和有效性。
除了对药品注册流程的简化和创新药品的支持外,2020版《药品注册管理办法》还在其他几个关键领域进行了重大调整。这些变化将进一步促进药品市场的良性竞争,并为企业创造更多机遇。
新版《药品注册管理办法》对药品的分类管理进行了新的细化。为了应对市场上日益复杂的药品种类,办法根据药品的特点、用途以及开发难度等因素,重新划分了药品的注册类别。例如,将药品分为常规药品、创新药品和特殊药品等多个类别,并针对不同类别的药品设置了不同的审评标准和审评流程。
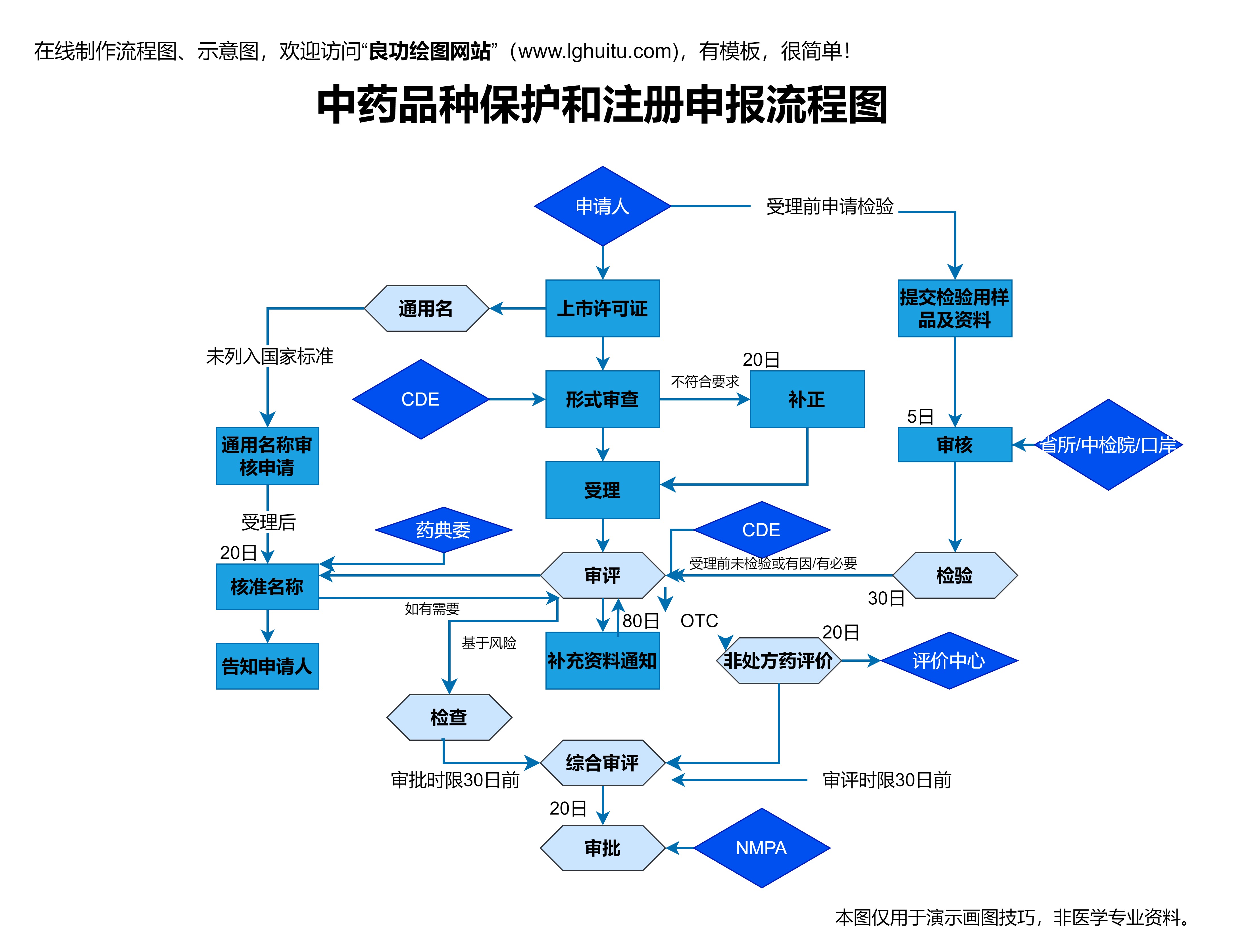
这一调整不仅为药品研发企业提供了更加清晰的方向,也帮助监管部门更加精准地进行市场监管。对于创新药品、仿制药、特殊用途药品等不同类型的药品,办法提出了不同的注册要求,确保了药品注册审批的高效性和精准性。
随着国内药品市场对仿制药需求的增加,2020版《药品注册管理办法》特别加强了仿制药的注册管理。新办法对仿制药的定义、审批流程、数据要求等进行了明确规范,要求仿制药在通过审评后,能够尽快进入市场。
办法提出了一系列激励政策,鼓励企业在仿制药的研发上进行技术创新,提高仿制药的质量和疗效。这些政策不仅有助于提高国内药品质量水平,还有助于推动更多仿制药产品符合国际标准,走向海外市场,提升我国药品的国际竞争力。
新版《药品注册管理办法》还特别强调了药品注册过程中的透明度问题,要求药品审评过程更加公开透明。这一规定的出台,既是对药品研发企业的激励,也是对药品市场和消费者的一种保障。通过提高透明度,药品注册的公正性和公开性得到了进一步保障,避免了审批过程中的不公正现象。
新办法明确了药品审评过程中的信息公开机制,包括审评标准、审批进度等信息都需要及时向社会公开。这将有助于增加社会对药品注册过程的信任,确保药品注册的公开、公平和公正。
2020版《药品注册管理办法》加强了药品上市后的不良反应监测和风险评估机制。办法明确了药品上市后的监控责任,要求药品生产企业在药品上市后要及时报告不良反应,并且加强药品风险评估,以便及时采取措施,保障患者的用药安全。
药品的安全性是药品管理中最为重要的一环。新版办法加强了对药品上市后不良反应的跟踪,确保药品在全生命周期中都能够保持高水平的安全性。
2020版《药品注册管理办法》的出台,意味着我国药品管理体制向更加现代化、科学化的方向迈出了重要一步。新办法通过加快审批速度、加强创新药品支持、优化分类管理等一系列改革措施,极大地推动了药品市场的规范化与国际化。对企业来说,这不仅是一次政策上的变革,更是一次抓住新机遇的黄金时刻。在未来,药品行业将迎来更加繁荣的发展局面。