近年来,随着药品管理要求的日益严格,药品注册考试作为专业人士的一项重要认证,吸引了越来越多的考生参与。2020版《药品注册管理办法》作为法规更新的重要组成部分,对于药品注册工作的影响深远。因此,掌握这一政策的要点,尤其是针对考试中常见的考题,显得尤为重要。
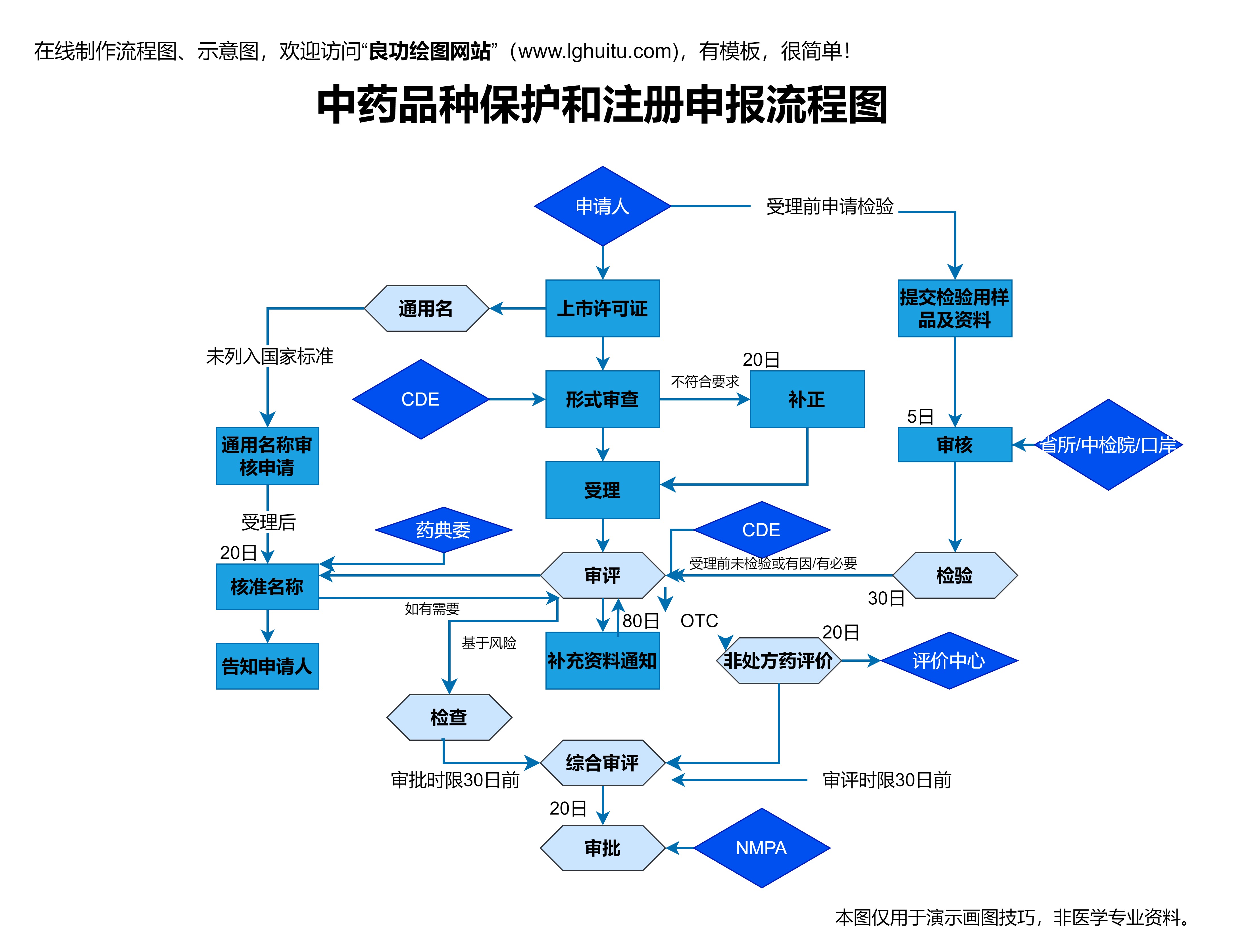
2020版《药品注册管理办法》的出台,不仅规范了药品注册流程,还针对药品研发、注册申请、审批等环节进行了全面细化。这一新版办法的学习重点也因此成了药品注册考试的关键,下面将针对一些常见的考题进行解析,帮助考生更好地应对考试。
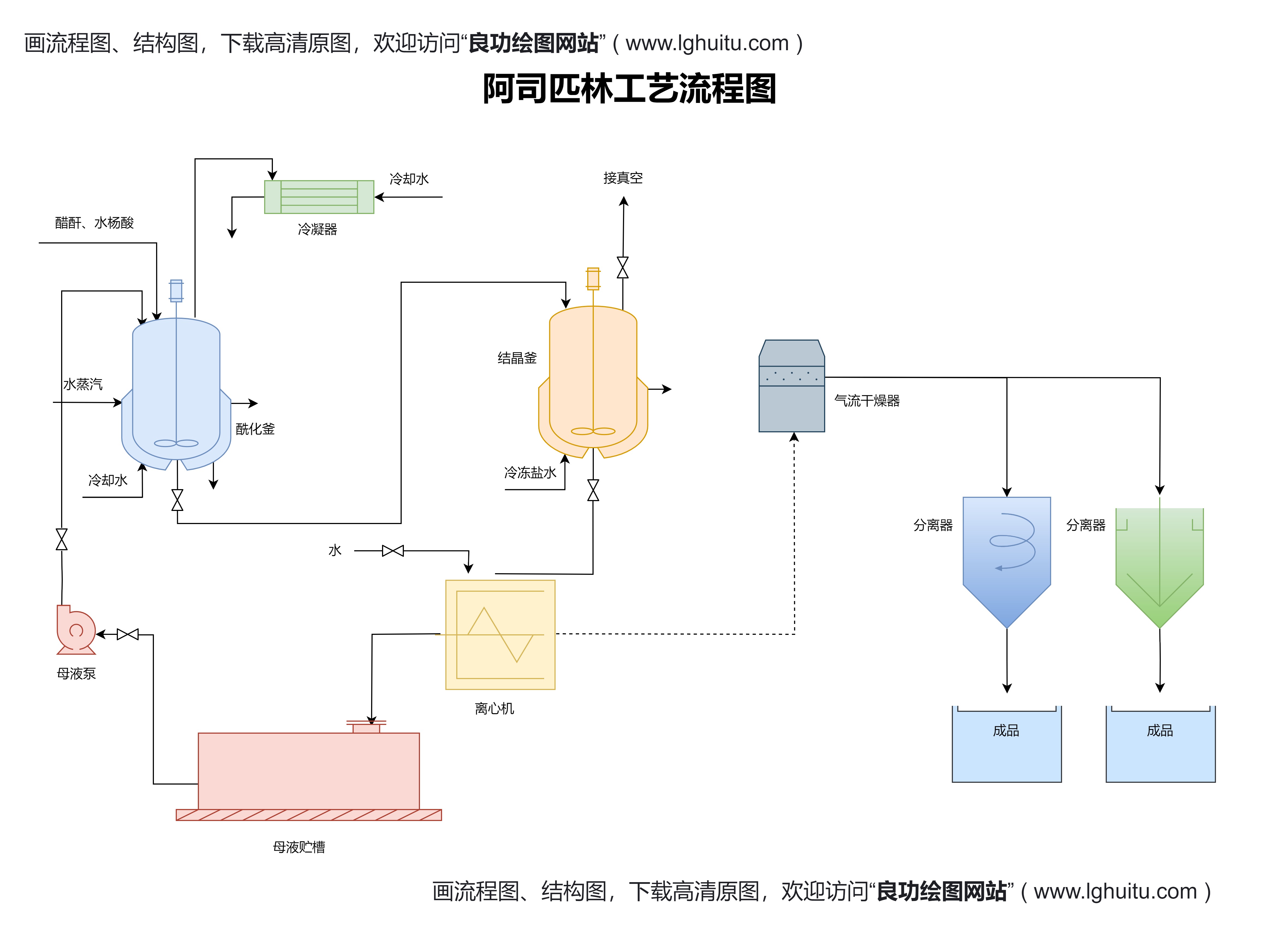
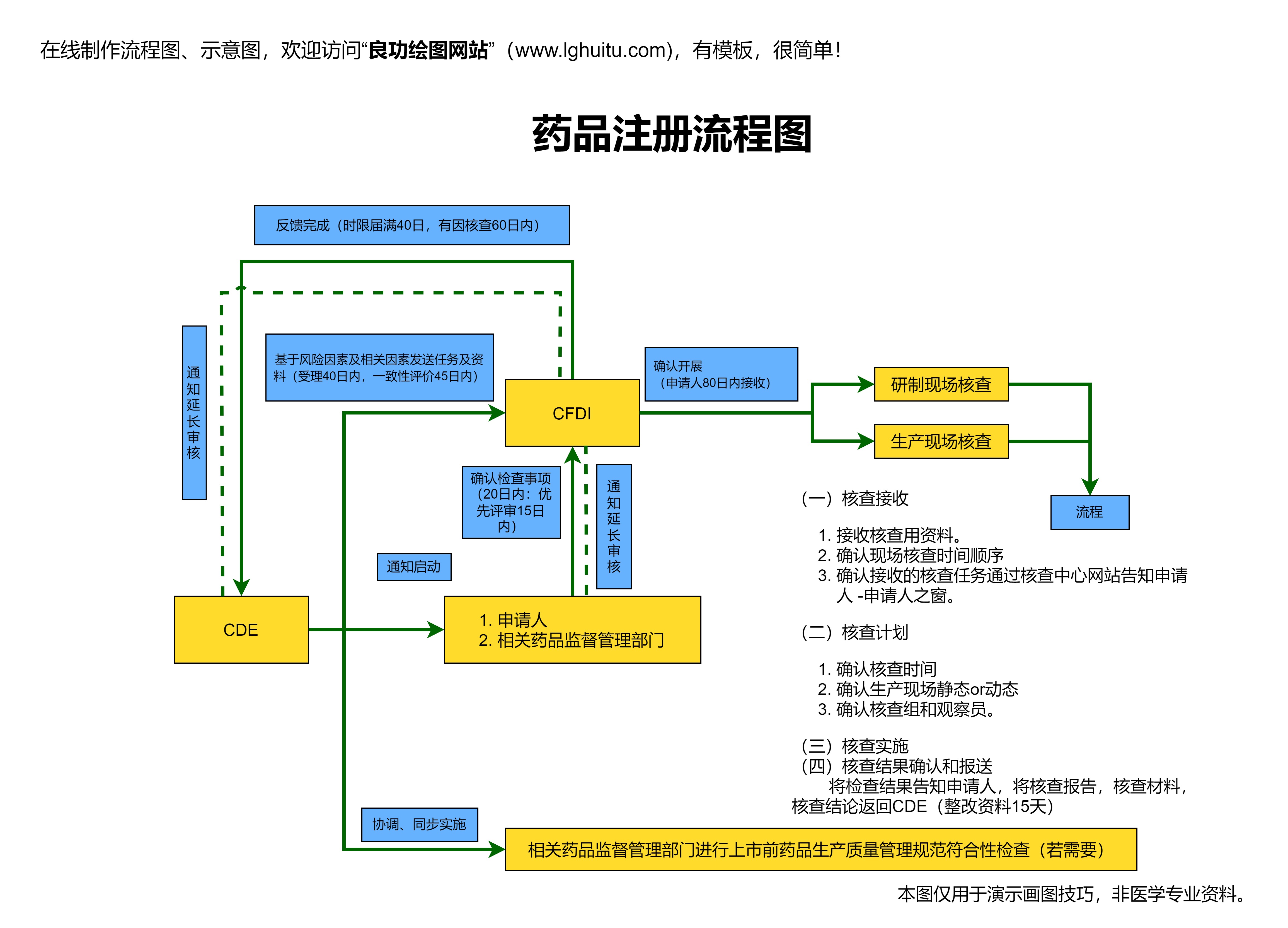
根据《药品注册管理办法》第八条,药品注册申请的基本程序包括:申请人向药品监管部门提交药品注册申请材料,药品监管部门对注册申请材料进行初审,审查合格后,药品监管部门进行专家评审,最后发布审批决定。这个程序的核心是审批流程的规范化和透明化,确保药品的质量、安全性与有效性。
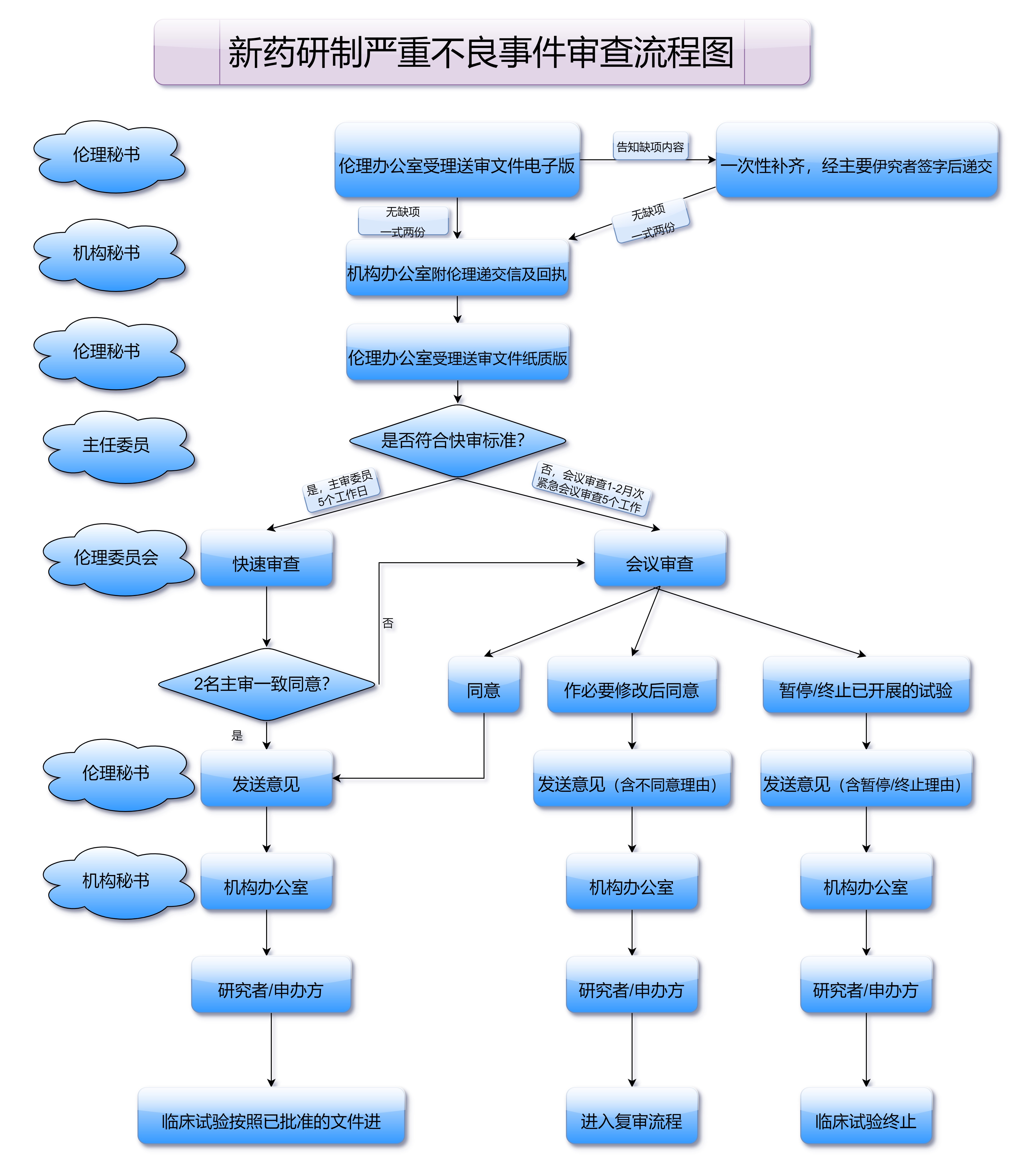
考题二:药品注册的审批程序中,哪些环节必须经过专家评审?
专家评审环节是药品注册审批的重要组成部分。根据《药品注册管理办法》的规定,专家评审环节主要针对药品的临床试验数据、药品的药理毒理试验结果以及药品的质量控制标准等进行审查。这一环节的设立,保证了药品注册审批中科学性和专业性的严格把关,能够最大程度地确保公众的用药安全。

在药品注册过程中,申请人所提交的材料如果存在缺失或不符合要求,药品监管部门有权要求申请人补充相关材料。《药品注册管理办法》明确规定,申请人可以在规定时间内进行补充,但如果超过了规定的时限,则会被视为不合格的注册申请。这一条款的设立,为药品注册过程中的材料审核提供了更加明确的时间框架,也有助于提高审批的效率。
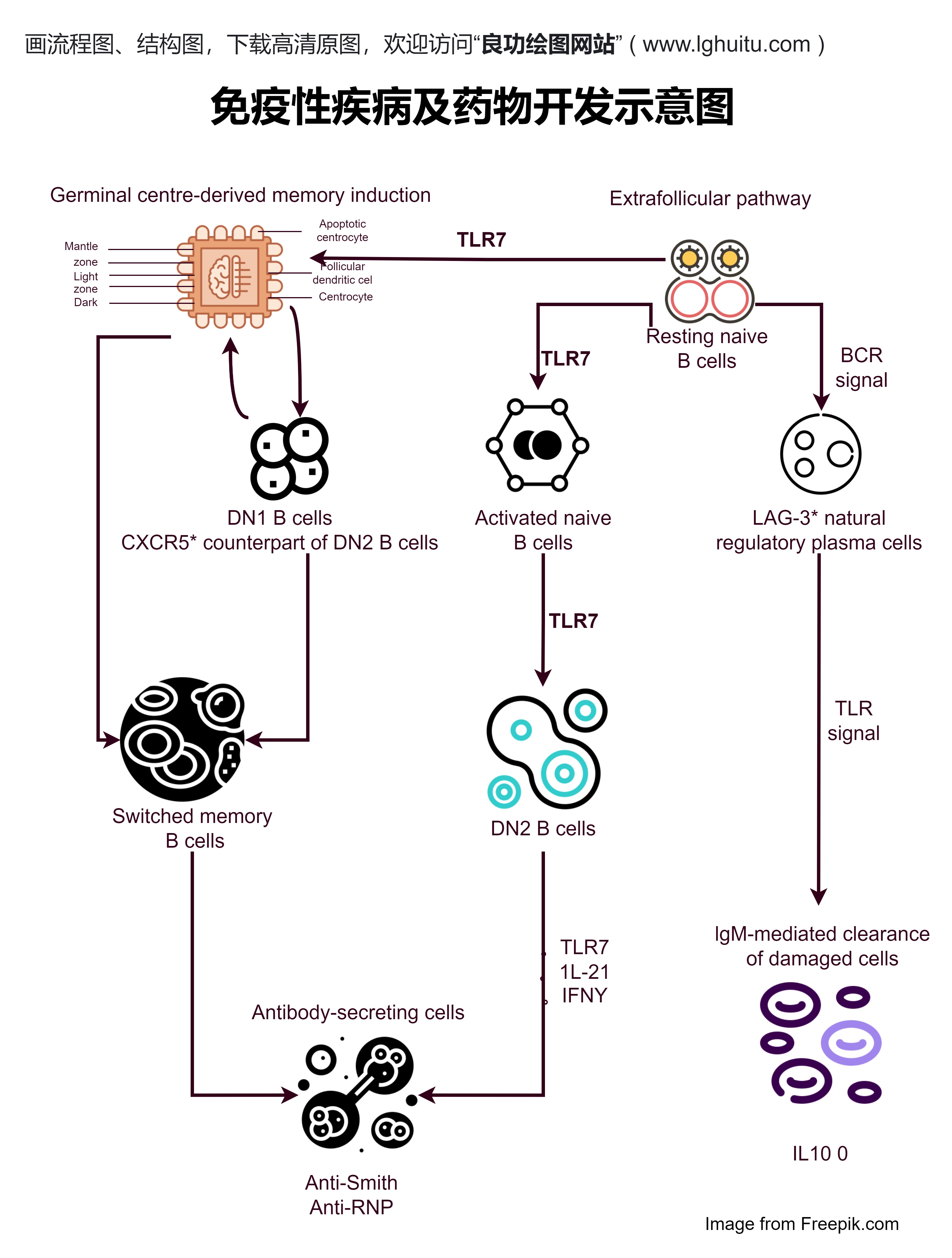
药品注册中的临床试验数据是药品审批的重要依据。《药品注册管理办法》规定,申请人应当提交符合国际标准的临床试验数据,并且在提交的试验数据中,必须包含临床试验的具体方案、试验结果、试验报告等内容。此项规定的推出,旨在确保药品注册过程中所有的临床数据能够得到有效核查,为药品的质量与安全性提供保障。
随着全球化进程的推进,跨境药品注册申请逐渐成为一个常见的现象。根据2020版《药品注册管理办法》的要求,药品注册申请在符合相关法规的前提下,申请人可以选择在境外药品监管部门已通过的情况下,进行跨境注册提交。这为药品企业提供了更多的便利,缩短了药品上市的时间,促进了国际市场的竞争力提升。
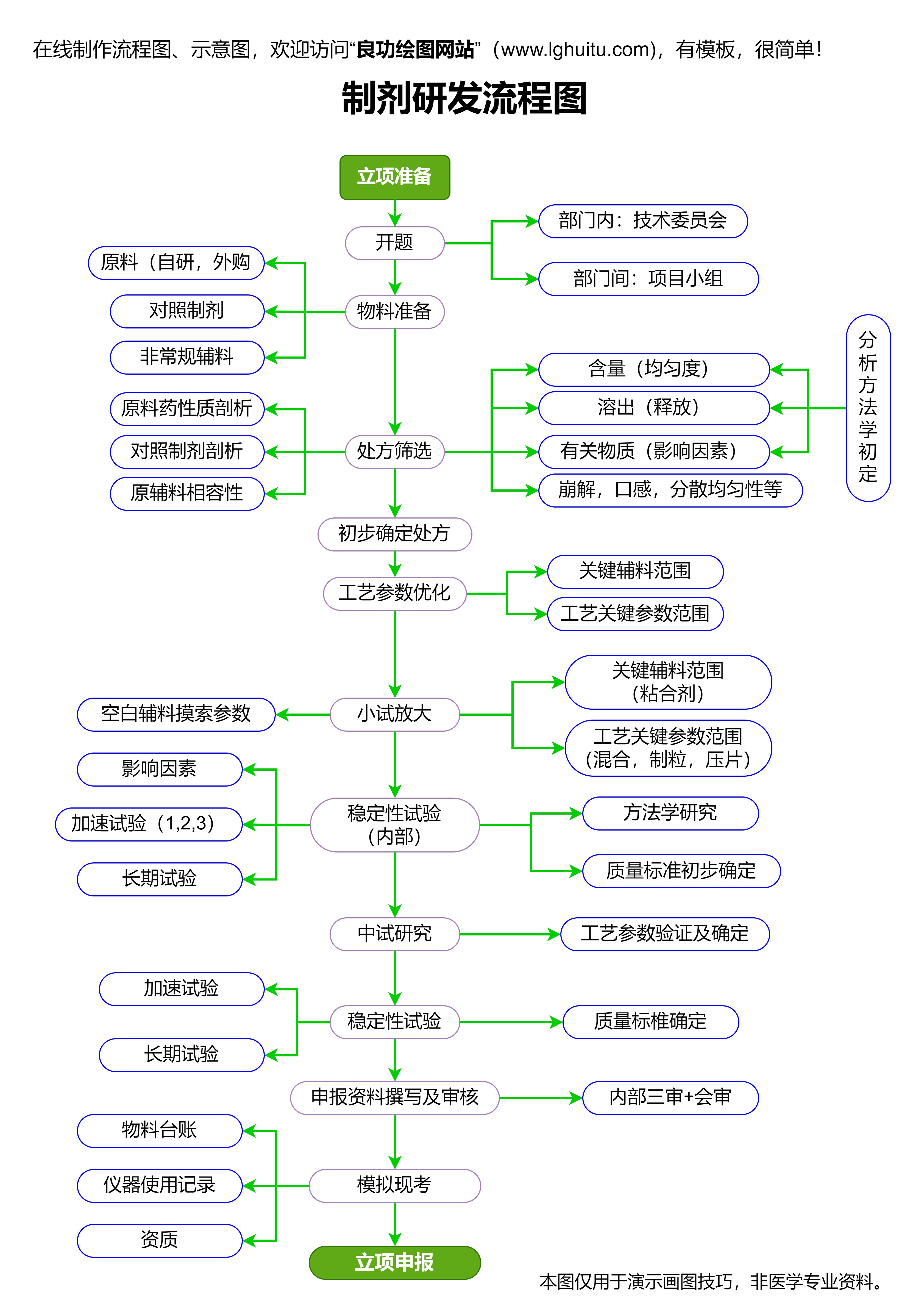
以上问题只是《药品注册管理办法》中的一部分,随着法规的逐步更新,更多与药品注册相关的条款可能会在考试中出现。通过系统学习并深刻理解这些法规,不仅能够在药品注册考试中获得理想成绩,也为实际工作中的药品注册过程提供了理论支持。
除了以上提到的常见考题,2020版《药品注册管理办法》中还涉及了一些其他关键的考试知识点。为了帮助考生深入理解这些内容,我们继续分析一些常见的考题,并提供详细的答案解析。
药品注册的有效期根据《药品注册管理办法》规定,药品注册证书的有效期一般为5年。在这段时间内,申请人可以根据需要进行续期注册。值得注意的是,续期申请时需要提交更新后的临床试验数据、药品质量标准等材料,以确保药品的继续符合相关法规和标准。这一规定旨在确保药品在市场上流通期间能够持续满足药品质量、安全性和有效性的要求。
考题七:药品注册过程中,哪些情况下可以申请紧急审批?
药品注册的紧急审批程序主要适用于那些具有重大公共卫生意义的药品,如疫苗、抗病毒药物等。根据《药品注册管理办法》的规定,在一些突发公共卫生事件中,申请人可以向药品监管部门申请紧急审批。紧急审批程序将优先考虑药品的疗效和急需性,同时也需要保证药品质量的安全性。紧急审批的设立,能够为重大疾病的防控提供及时有效的药品支持。
根据《药品注册管理办法》的要求,药品注册的部分信息是需要向公众披露的。包括药品的注册证书、药品的基本信息、药品的主要成分、临床试验数据等。这些信息的披露有助于增加药品注册的透明度,使公众能够更加清晰地了解药品的质量和安全性。这也促进了药品监管部门与公众之间的沟通与信任。
药品注册成功后,药品上市并不意味着监管工作就结束了。根据《药品注册管理办法》的规定,药品上市后仍然需要进行定期的质量监控和安全性评估。药品生产企业需要定期向药品监管部门报告药品的上市后情况,包括药品的不良反应、市场反馈等内容。如果发现药品存在安全性或质量问题,药品监管部门有权要求生产企业采取措施,甚至撤销药品的注册证书。
药品注册证书和生产许可证是两个不同的概念。药品注册证书是对药品的质量、安全性和有效性进行审核并给予批准的证明,而生产许可证则是药品生产企业必须持有的证书,它证明企业具备合法生产药品的资格。这两者虽然在功能上有所不同,但在药品上市过程中缺一不可。
通过对《药品注册管理办法》的学习和考题解析,考生可以全面了解药品注册的各项规定。掌握这些法规知识,能够在药品注册考试中占据优势,为自己的职业发展奠定坚实的基础。对于实际从事药品注册工作的人来说,深入理解和应用这些规定,也能有效提升工作效率与合规性。