在药品注册管理的过程中,掌握2020版药品注册管理办法的核心内容,是每一位药品从业者和考生的必备技能。随着药品行业的不断发展,药品注册的相关政策也在不断优化和调整。2020版药品注册管理办法作为新一轮法规体系中的重要部分,其深刻的行业意义和严格的法规要求,不仅影响药品注册的审批流程,也对考试的难度和内容产生了重要影响。
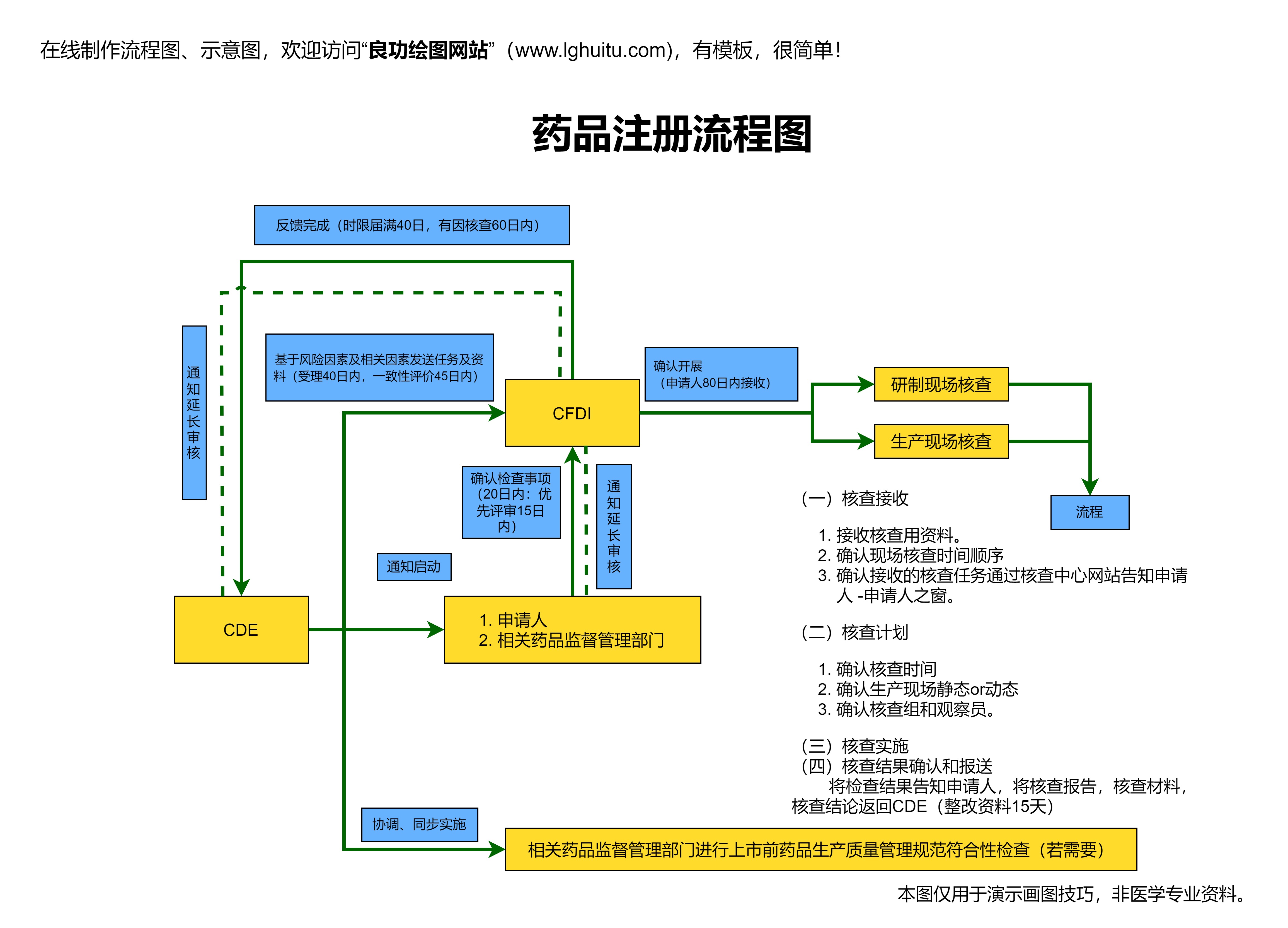
近年来,随着药品注册管理的规范化和透明化,越来越多的从业人员开始重视相关法规的学习。而2020版药品注册管理办法的推出,更是对药品行业的一次深刻洗礼,尤其对于药品注册考试的考生来说,理解和掌握这一办法成为了通过考试的关键。
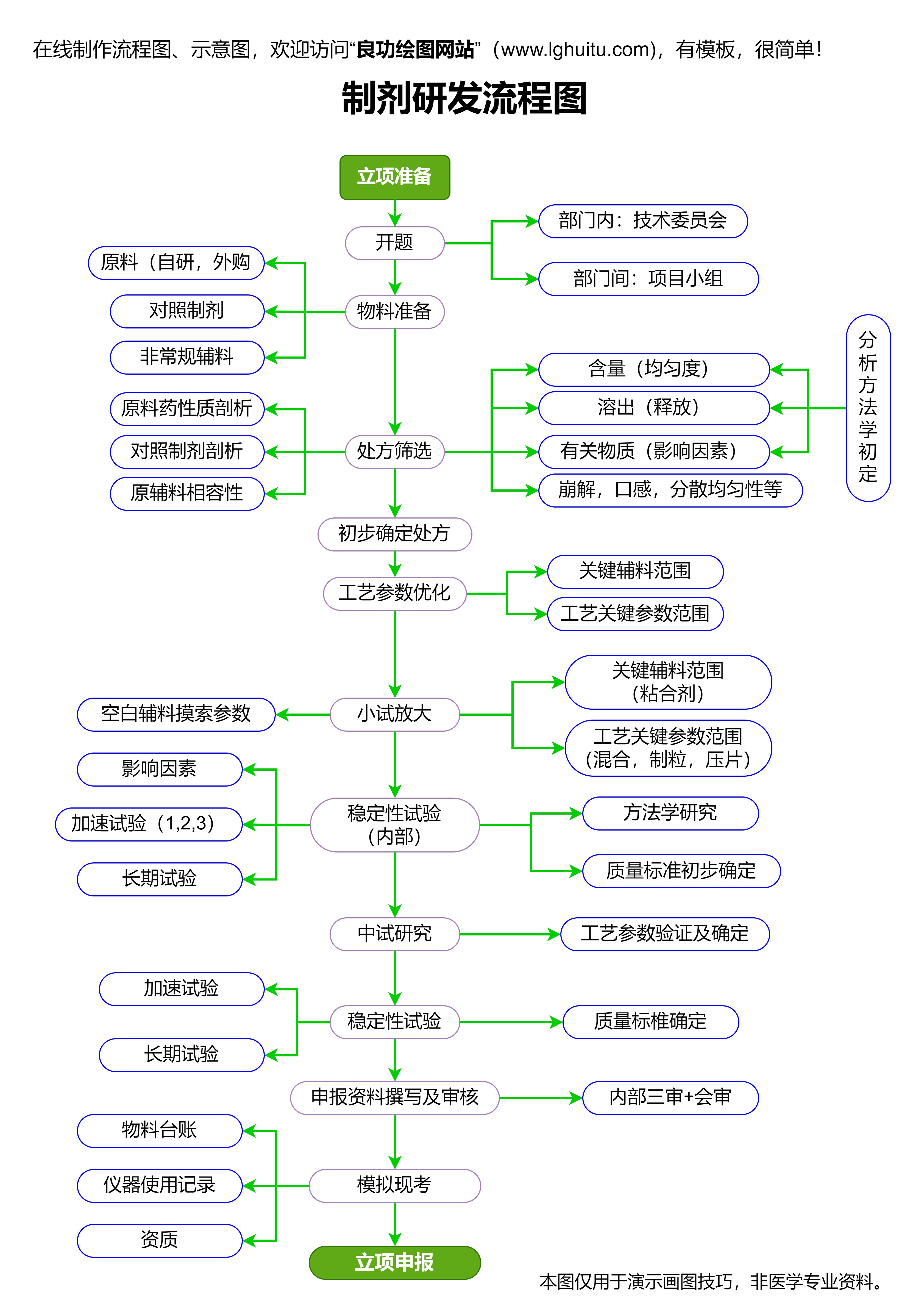
2020版药品注册管理办法的重点之一,就是对药品注册审批的程序进行了详细规定。无论是国内生产药品,还是进口药品,其注册审批流程都变得更加规范,特别是在药品的临床试验、技术要求、数据提交等方面的要求都有了更严格的规范。对考生而言,考试内容往往会围绕这些重要环节展开,考察其对新办法的理解和掌握。
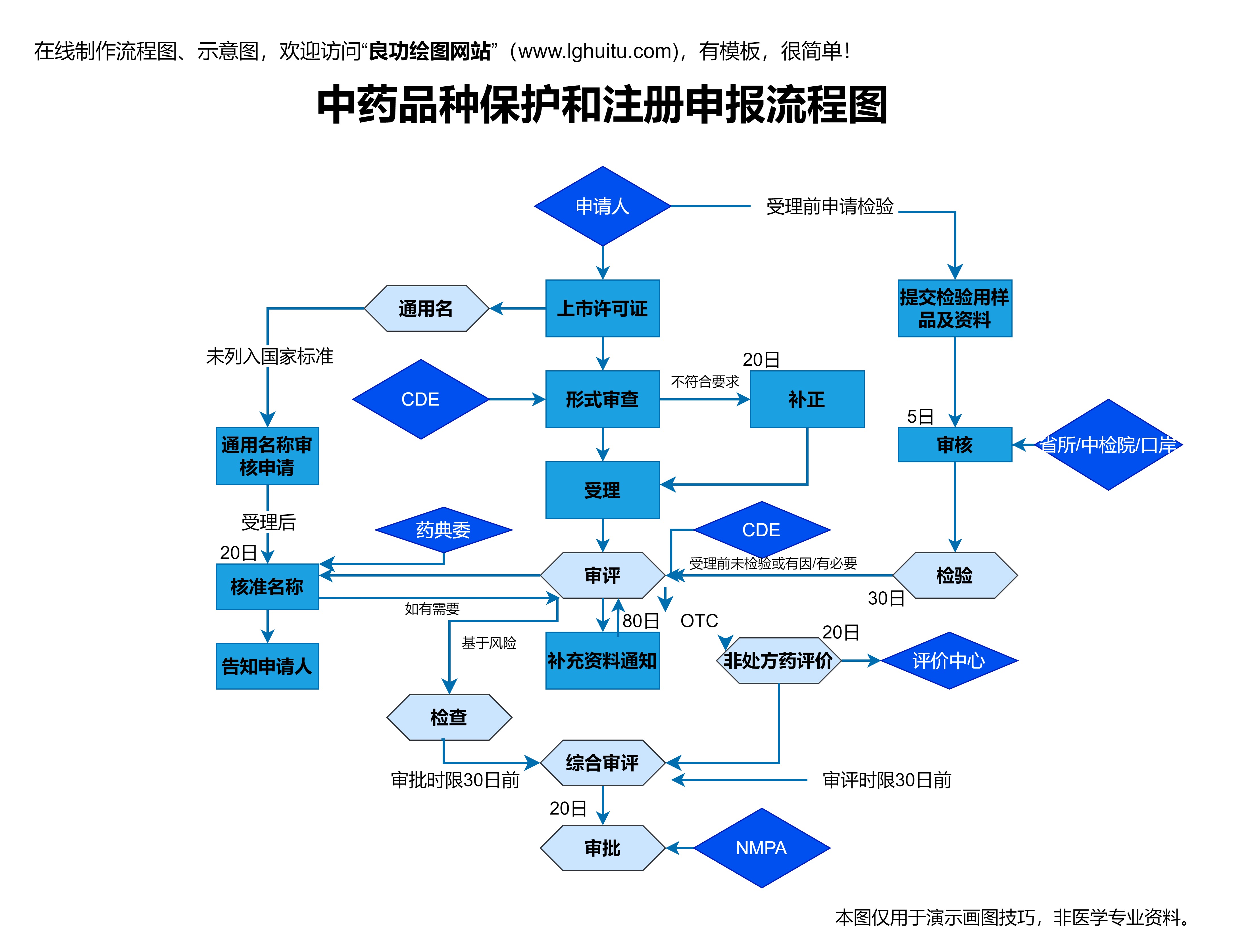
新办法还强调了药品注册资料的完整性和真实性。2020版办法要求,所有的药品注册资料必须真实、完整,任何虚假资料将导致注册申请被拒。考题往往会结合这一要求,测试考生是否了解并能够正确识别注册资料中的关键问题,避免因细节上的疏忽而导致考试失误。
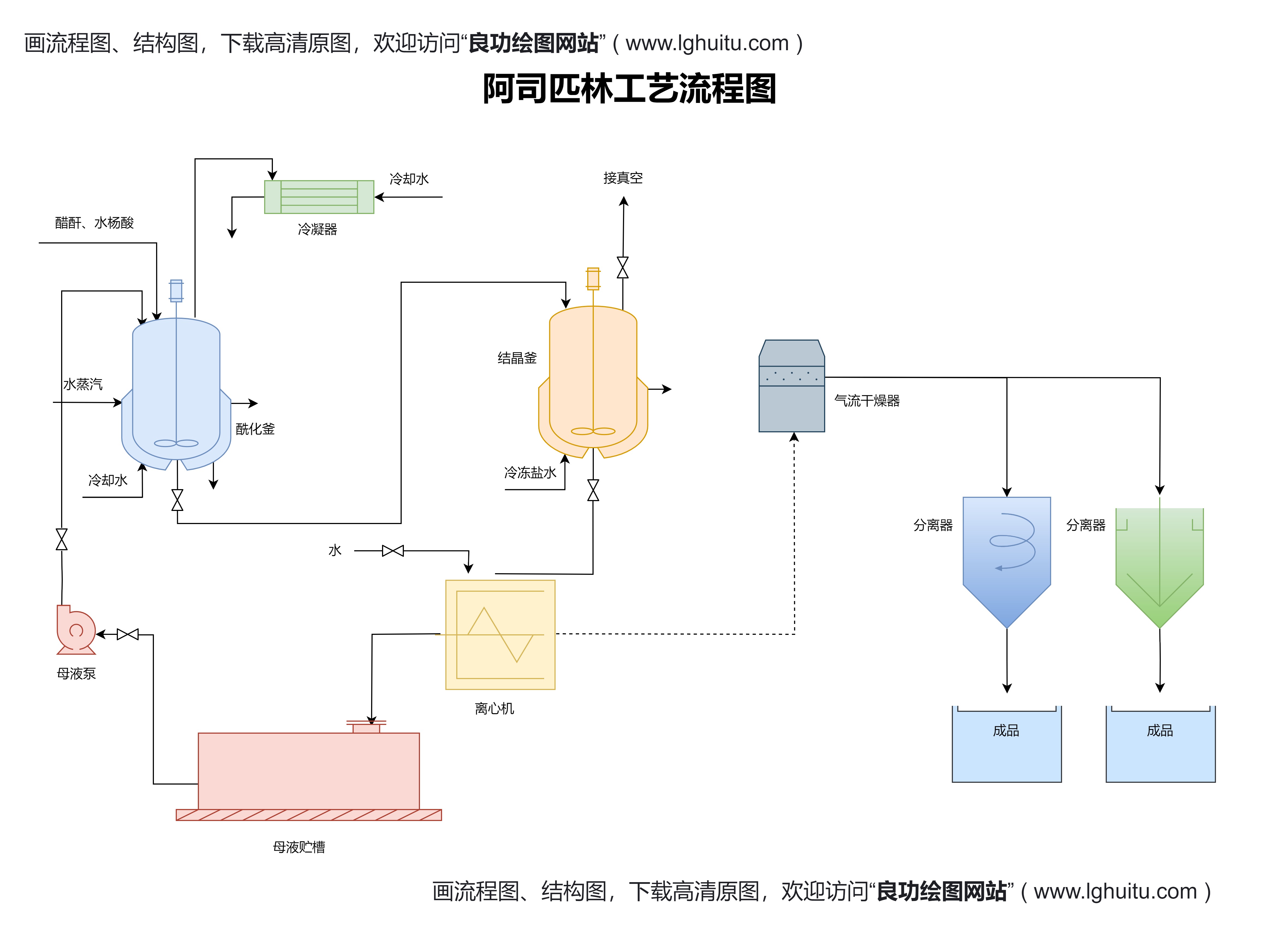
在考试的过程中,考生需要特别注意两个方面。要清楚理解2020版药品注册管理办法中对于不同类型药品的注册要求。无论是化学药品、生物制品还是中药,其注册标准和程序都有所不同,因此考生在备考时,务必根据不同药品类别的特点,逐一掌握其注册流程及相关的法律规定。
考生还应关注办法中关于药品注册审评标准的变化。在2020版办法中,药品的审评标准不仅考虑药品的质量和疗效,还逐步加入了药品的临床需求、市场前景等方面的综合评估,这对于药品的市场准入产生了深远影响。考题往往会考察考生对审评标准变化的理解,考生需要通过大量的习题和案例分析,进一步加深对这一内容的把握。

2020版药品注册管理办法的发布,是中国药品管理制度的一次大革新。其对药品注册流程、审评标准、资料要求等方面的规定,不仅在实践中提高了药品注册的透明度,也为药品行业的合规化发展奠定了坚实基础。对药品注册考试的考生而言,深入理解这些变化,是确保顺利通过考试、提升专业能力的必由之路。
进一步解读2020版药品注册管理办法的考点和答案解析,将有助于考生更加高效地备考。通过对考题的分析和答案的深入讲解,考生能够在考试中更加得心应手,提升自身的通过率。我们将对一些常见的考题进行详细解析,帮助考生理解并掌握核心内容。
考生常常会遇到关于药品注册申请程序的题目。根据2020版药品注册管理办法,药品注册的申请过程分为多个阶段,其中包括了预审、技术审评、批准等重要环节。对于考题中的具体流程,考生需要注意的是,申请人需要在预审阶段提交完整的申请资料,经过技术审评后,药品注册是否能够通过,取决于其是否满足所有技术要求。因此,考生在回答关于申请程序的问题时,应详细掌握每个步骤的关键要求。
例如,一道典型的考题可能是:“在药品注册申请的过程中,哪一个环节最为关键,决定了药品是否能够获得批准?”答案解析:这是一个关于药品注册审批流程的综合性问题,答案应为“技术审评”。因为在技术审评阶段,专家评审委员会将对药品的质量、疗效、安全性等方面进行严格评估,决定药品是否能够进入市场。因此,考生应重点关注这一环节的要求。
2020版药品注册管理办法还特别强调了药品注册资料的真实性和完整性。在考试中,考生常会遇到关于药品注册资料填写规范的题目。为了帮助考生更好地理解这一考点,以下是一个典型的考题及答案解析:“药品注册过程中,申请人提交的临床试验数据如果存在虚假情况,可能会导致什么后果?”答案解析:根据2020版药品注册管理办法,如果药品注册过程中提交虚假资料,特别是临床试验数据,可能会导致注册申请被拒绝,甚至可能会面临处罚。考生需要在备考时,牢牢记住这一点,理解其对整个注册流程的影响。
考生还应当对2020版药品注册管理办法中的新规定进行深入分析。例如,新办法中对药品注册审评标准进行了调整,加入了更多的临床需求评估和市场准入的考量。在答题时,考生需要特别注意这些细节,明确审评标准的变化,并能够在题目中识别出其关键要素。
想要在药品注册管理办法考试中取得好成绩,考生必须掌握新办法中的关键内容,特别是在药品注册流程、资料要求、审评标准等方面的变化。通过大量的题目练习与解析,考生能够加深对相关知识点的理解,并在考试中轻松应对各类考题。通过系统学习和精心备考,相信每一位考生都能够顺利通过考试,为自己在药品行业的职业发展打下坚实的基础。