在中国,药品注册管理办法是药品上市的重要程序之一,直接影响着新药的研发和市场准入。2020年,国家药品监督管理局对药品注册管理办法进行了大幅修订。新修订的《药品注册管理办法》不仅顺应了国家对药品监管的整体发展趋势,也为药品市场的竞争注入了更多的活力。

药品注册审批的效率直接关系到药品的上市速度。传统的审批程序较为繁琐,一度成为制药公司面临的重要挑战。2020版《药品注册管理办法》通过简化注册程序,缩短了审批周期。例如,部分药品可通过“优先审批”通道进行加速审批,尤其是在应急药品、新冠疫苗等突发公共卫生事件中,政策的灵活性表现尤为突出。药品的审批不再局限于传统的化学药品或传统中药,生物制药、基因工程药物等创新药物也得到了快速通道,进一步加速了新药的研发与上市。
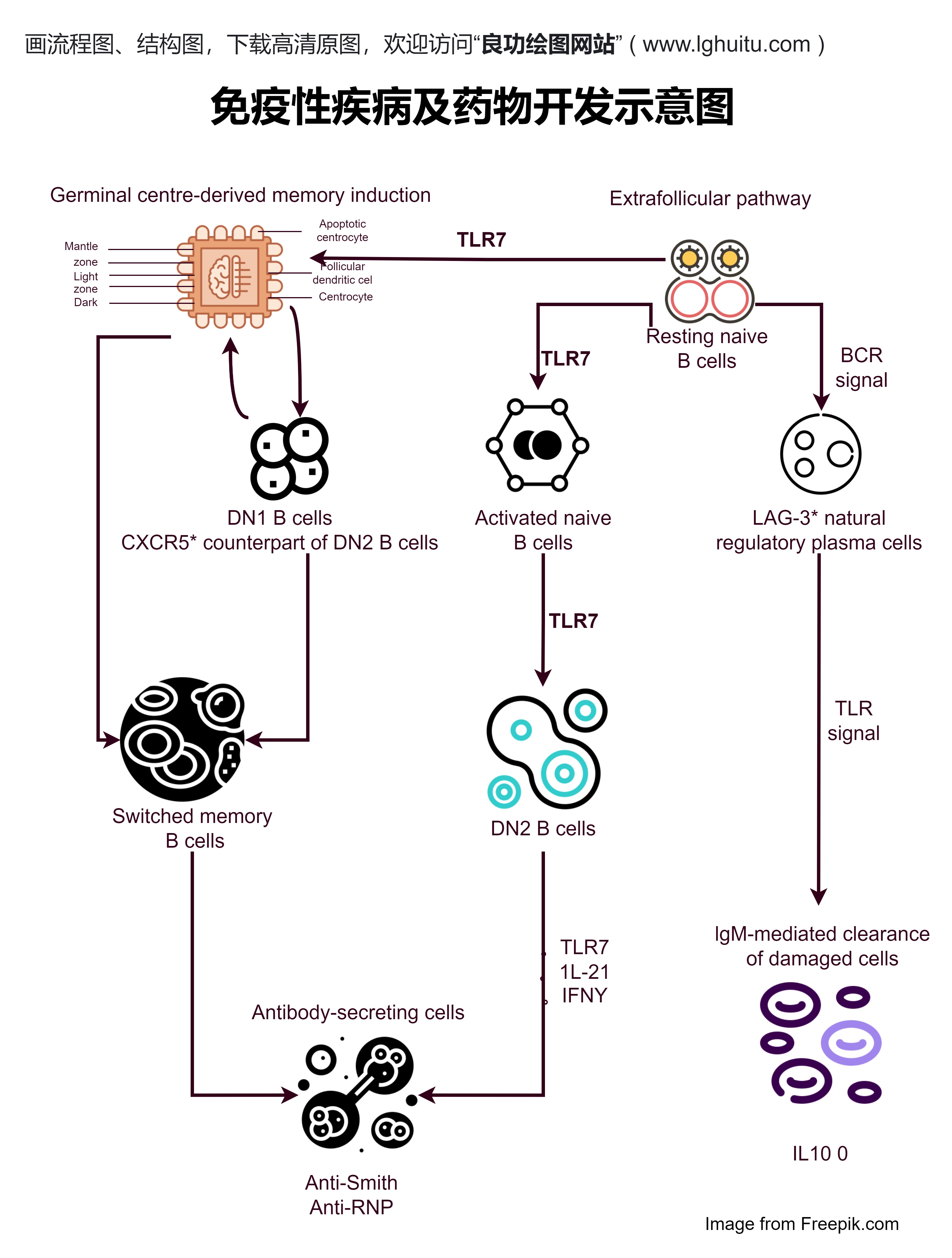
2020版《药品注册管理办法》对于药品临床试验的管理进行了更加严格的规定,特别是在国际多中心临床试验的要求上做出了新的规定。新的规定要求,对于有国际合作的药物临床试验,需要明确向监管机构报告,且必须符合国际标准。这不仅提升了国内药品的研发水平,还增强了药品在国际市场的竞争力。
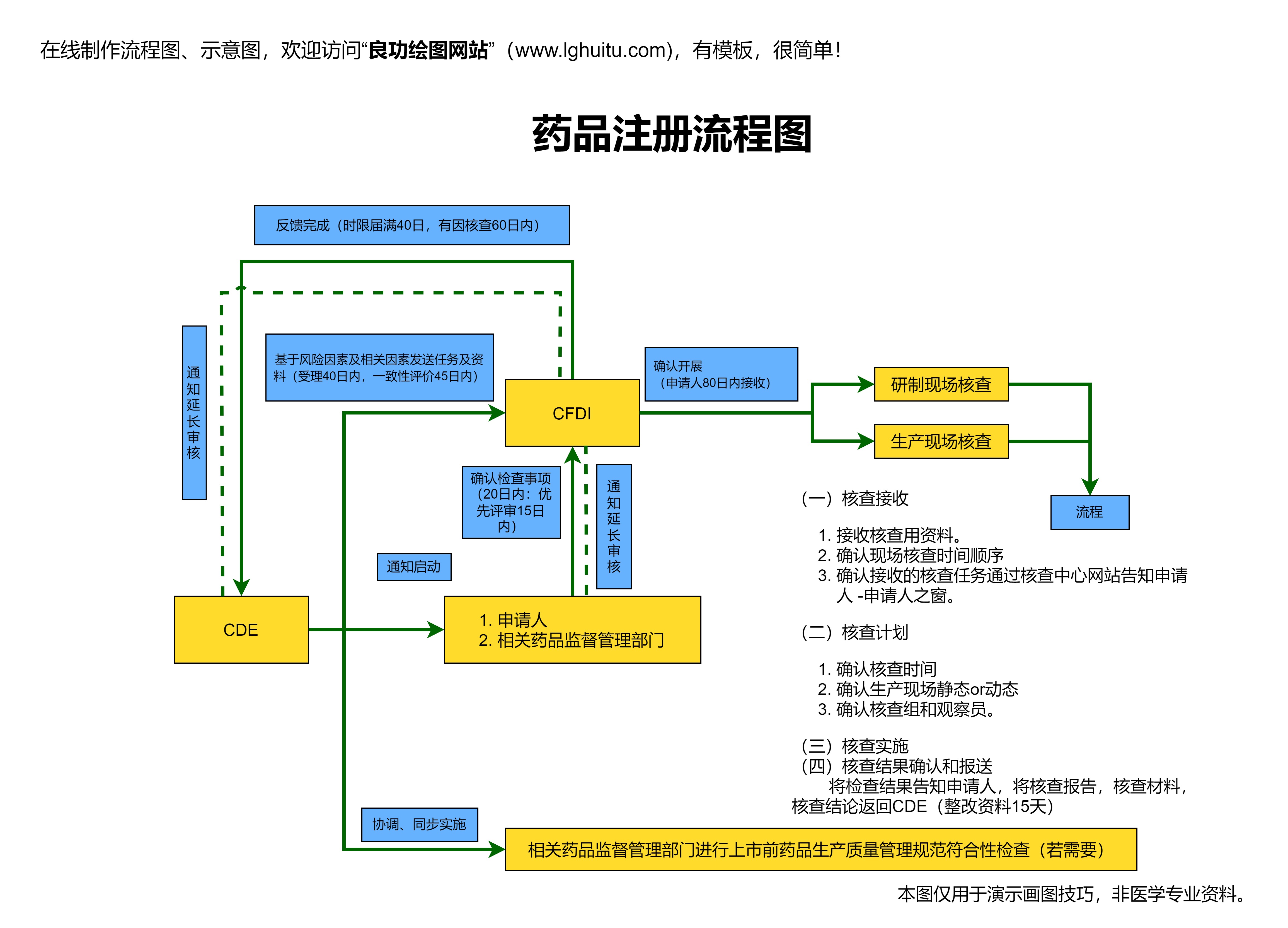
新的管理办法还加强了对临床试验的全过程监管,确保每个环节都符合伦理标准,保障受试者的安全与权益。药品的临床试验数据必须真实有效,且不允许虚假数据的存在,这样的规定为药品注册的透明度和公正性提供了保障。
对于创新药物的扶持力度,2020版《药品注册管理办法》无疑是一个巨大的利好。新办法明确提出,对于具有创新性、满足未满足临床需求的药物,将优先受理,并且在注册环节给予相对宽松的要求。例如,部分特定的创新药物可不再需要进行全套的临床试验,而是允许通过数据共享和跨国临床试验来减少重复试验的负担。
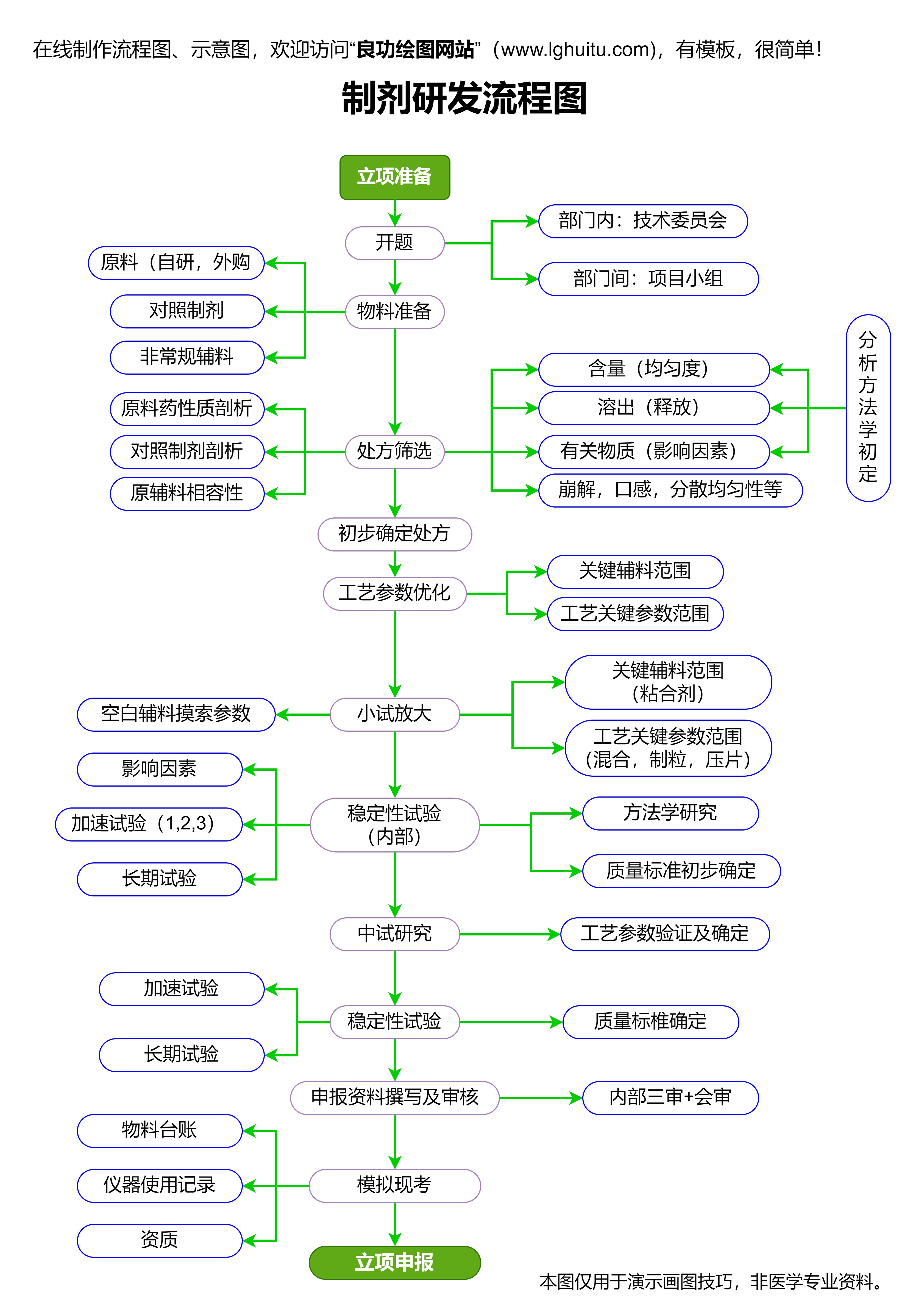
办法还支持药品研发企业通过获得“突破性疗法”认定来加速注册程序,进一步优化了新药进入市场的路径。通过这一政策,国内的制药企业有机会和国际制药巨头站在同一起跑线上,推动了创新药物的本土化生产和应用。
药品注册的工作并不仅仅是上市批准,它的后期管理同样至关重要。新的注册管理办法对药品的后续监管提出了更高要求,特别是在药品上市后的风险管理、定期跟踪评估等方面。新规要求药品生产企业在药品上市后要定期报告药品的不良反应以及相关安全数据,并且要根据市场反馈进行必要的药品质量改进。
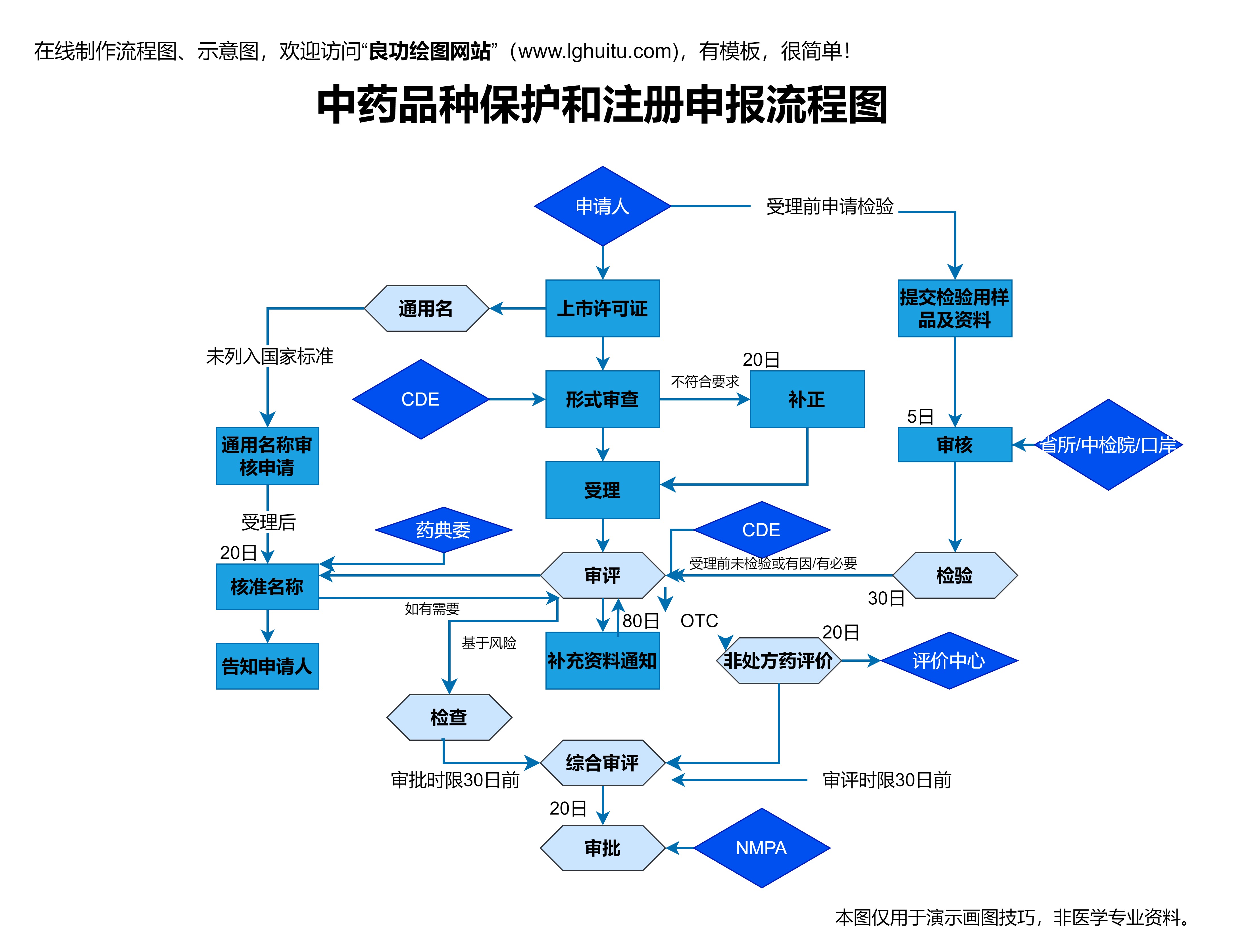
通过这些加强后的后期监管,药品的安全性得到了进一步保障,也避免了不合格产品对公众健康带来的风险。此举无疑增强了消费者对药品市场的信任度。
2020版《药品注册管理办法》在明确药品注册流程的也更加清晰地规定了各方责任,尤其是药品研发企业的责任。新的规定要求,药品注册申请人必须对提交的所有资料真实性和完整性负责,且任何违规行为都将受到严厉的处罚。
药品注册过程中,不仅药品生产企业要承担责任,相关检测机构、临床试验机构以及药品监管部门都将承担起更加具体的责任。这种“全链条”的责任划分,进一步提高了药品研发和上市的透明度。
随着全球化的推进,中国药品市场的国际化趋势日益明显。在2020版《药品注册管理办法》中,国际合作的条款得到了进一步加强,特别是在跨国药品注册和审批方面。新办法提出,针对那些已经在发达国家(如美国、欧洲等)批准上市的药物,可以通过简化审批程序来快速进入中国市场。这一政策的推出,不仅为国外创新药物进入中国提供了便利,也进一步促使国内药品公司走向国际市场。
中国的药品注册机构也加强了与国际药品监管机构的合作,共享药品审评经验与数据,提升了国内药品的国际竞争力。通过这样的国际合作,中国的药品审批标准也将逐步与国际接轨。
药品注册管理办法的修订,进一步推动了药品市场的公平竞争。新规提出,药品审批不仅要关注药品的创新性,还要注重其临床疗效和市场需求。对于一些相似药物,监管部门将更为严格地评估其市场价值与疗效,从而减少盲目重复建设和市场竞争的无序性。
这种政策的变化为制药公司提供了一个更加公平的竞争环境,同时也避免了市场上无效药物的泛滥。这种严格的审批机制,不仅提高了药品质量,也保障了公众的用药安全。
2020版《药品注册管理办法》还提出了数字化监管的新理念,药品审批的整个过程将更多依赖于信息化平台来管理。新的办法要求,药品企业和监管机构应通过电子化手段进行信息共享,确保审批资料的高效传递与审查。这一转型不仅提高了审批效率,也减少了人工错误的发生,有助于药品审批的透明度和可追溯性。
与此数字化监管平台还提供了药品信息公开、药品查询等功能,方便了公众对药品信息的获取,进一步促进了社会的监督和药品安全管理。
随着2020版《药品注册管理办法》的实施,中国药品市场将迎来更加开放、公正、透明的竞争环境。药品创新的门槛有所降低,药品审批的效率大大提升。未来,药品市场的主体结构将更加多元化,创新药物、仿制药物、国际合作药物等将共同推动中国制药行业迈向更高的水平。
2020版药品注册管理办法的出台,标志着中国药品监管改革的深化。这不仅为国内药品企业创造了更多的发展机会,也为公众的用药安全提供了更有力的保障。在未来,我们可以期待一个更加健康、公平的药品市场。