近年来,随着我国医药行业的快速发展和全球市场对中国药品需求的不断增加,药品注册管理逐渐成为药品研发和生产企业亟待解决的重要问题。而作为药品注册管理的一项重大举措,2020版药品注册管理办法的出台无疑引发了行业内外的广泛关注。这一新的政策不仅对药品注册流程进行了优化,也对新药证书的发放流程进行了相应调整,使得越来越多的创新药物能够迅速走向市场,为患者带来更多治疗选择。

根据2020版药品注册管理办法的相关规定,药品注册的审批流程进一步简化,审批时限大幅缩短。在此政策指引下,新药证书的发放得到了更高效的支持。尤其对于一些创新药物的申请者来说,这意味着他们可以在更短的时间内获得新药证书,迅速进入临床试验阶段,甚至最终实现上市。这对于促进新药的研发和推动国内外药品市场的快速更新换代都具有重要意义。
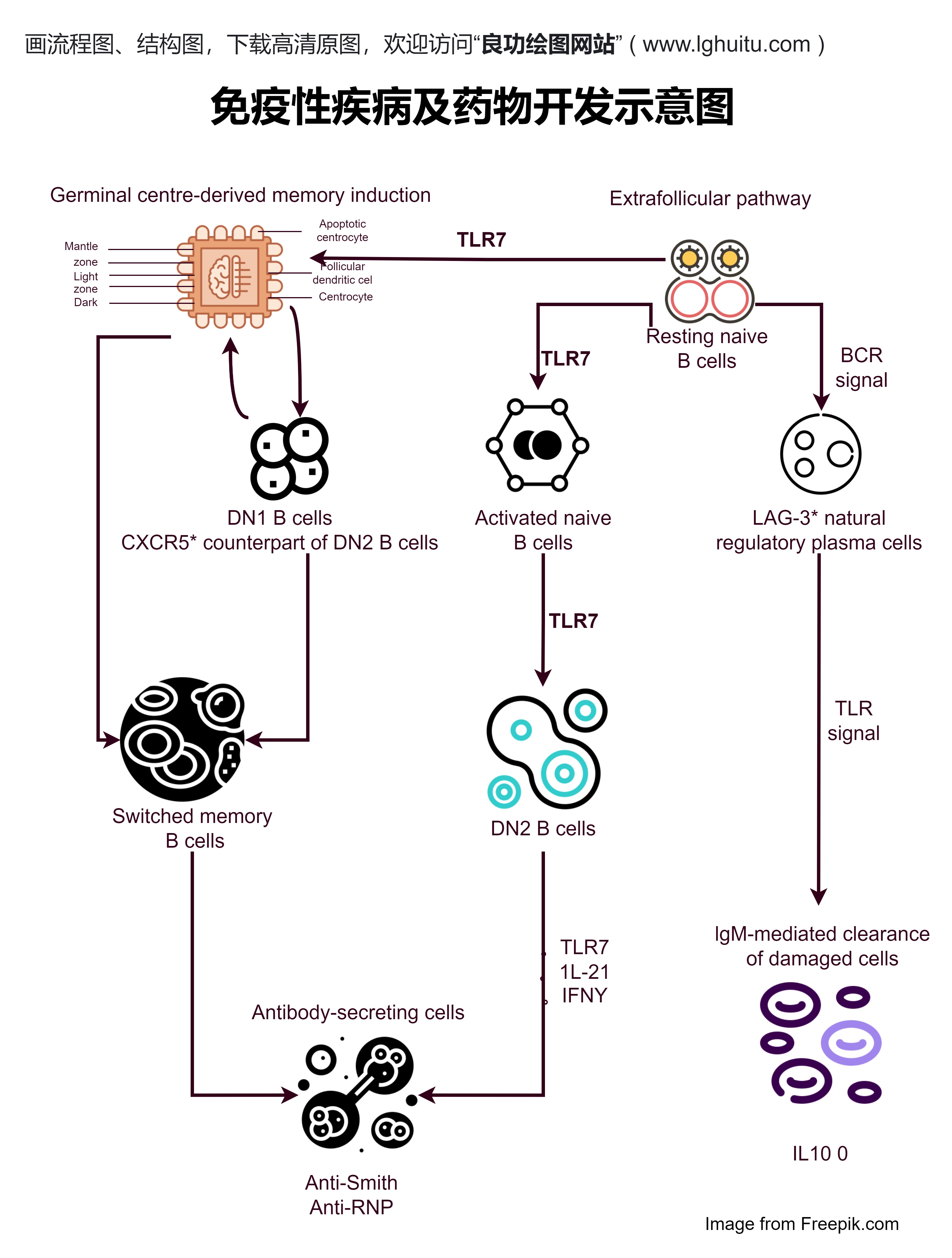
2020版药品注册管理办法对药品临床试验的管理也提出了新的要求和更高的标准。药品注册过程中,企业需提供更加严谨的临床数据支持,并且在临床试验中强调药品的安全性和有效性。这对于新药证书的颁发至关重要,确保了在药品审批过程中,药品的质量、疗效和安全性能够得到充分验证,从而减少药品上市后可能带来的风险。
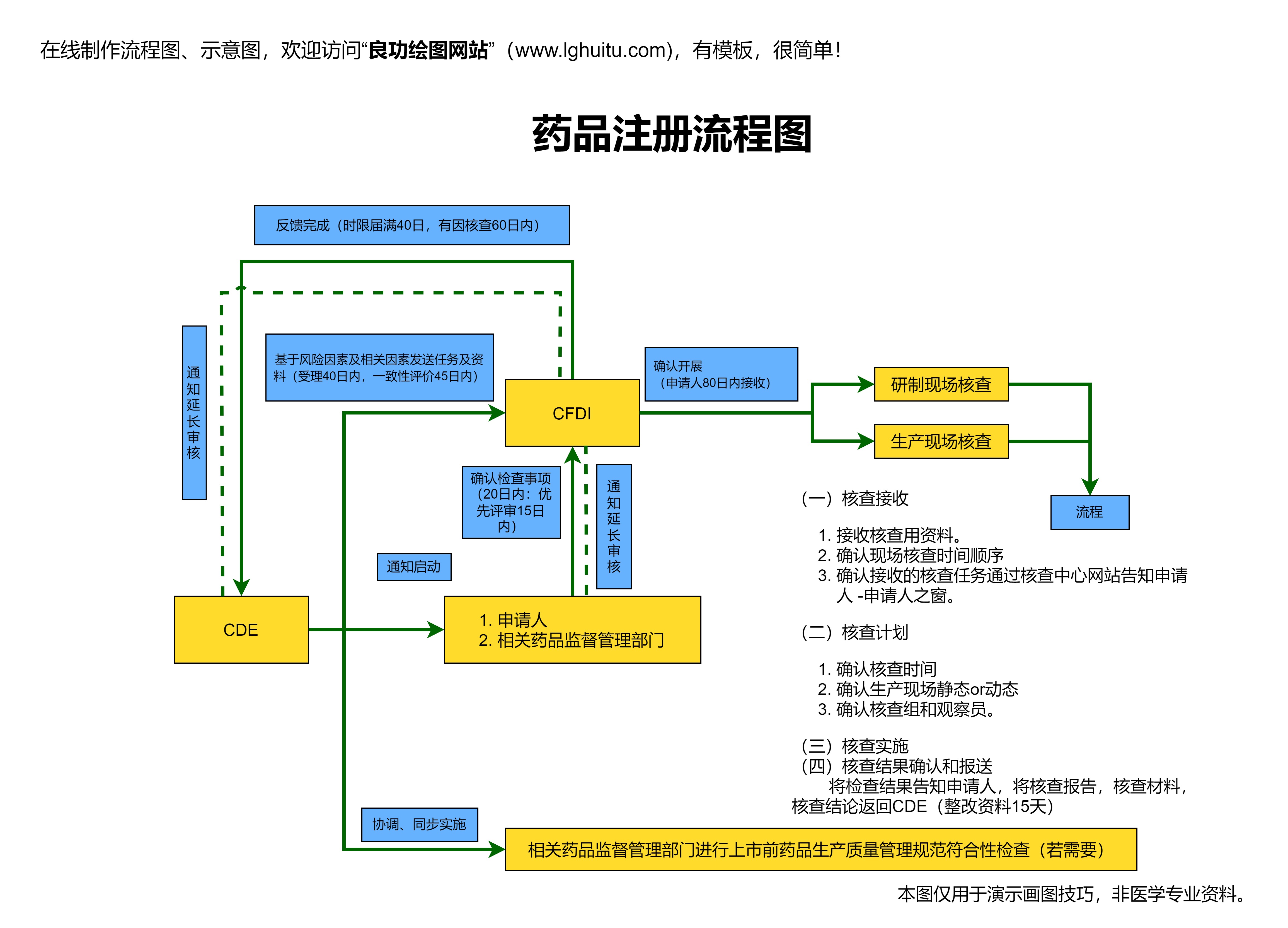
2020版药品注册管理办法还特别强调了药品注册的透明度和信息公开。在新药申请过程中,药品注册申请者可以更清晰地了解到药品注册的每一环节及审批进度。这一措施不仅提升了整个药品审批过程的透明度,还为药品注册管理的科学化、规范化奠定了基础。
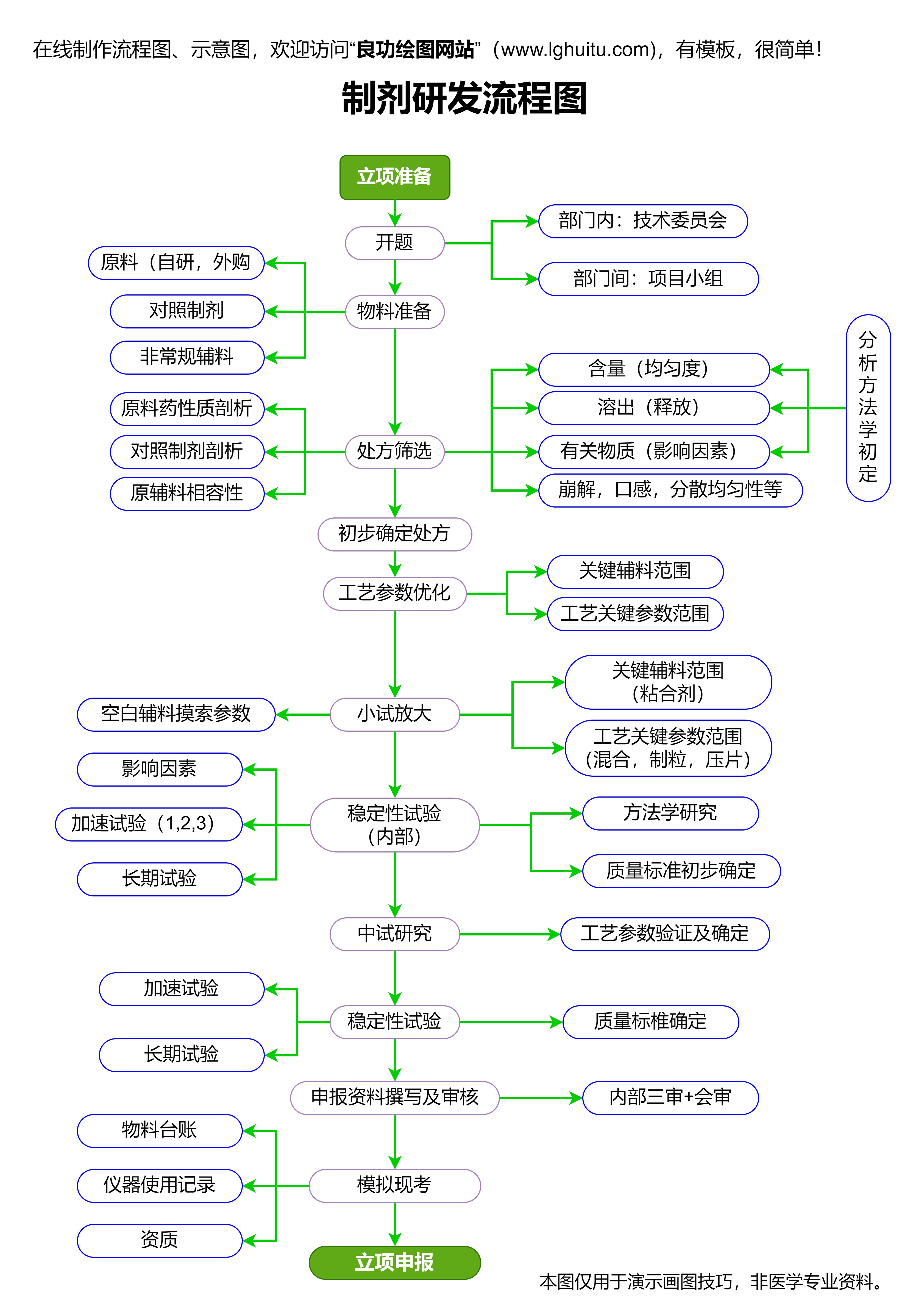
对制药企业来说,药品注册管理办法的变革无疑带来了更多机遇和挑战。尤其是对于那些积极推进创新研发的企业,新的药品注册办法使得他们的药品研发工作更加高效,能够在更短的时间内完成从研发到上市的全过程。与此药品注册的标准化和透明度提高,也让企业在整个申请过程中可以更加清晰地把握申报进度和审批细节,从而做出更有针对性的策略决策。
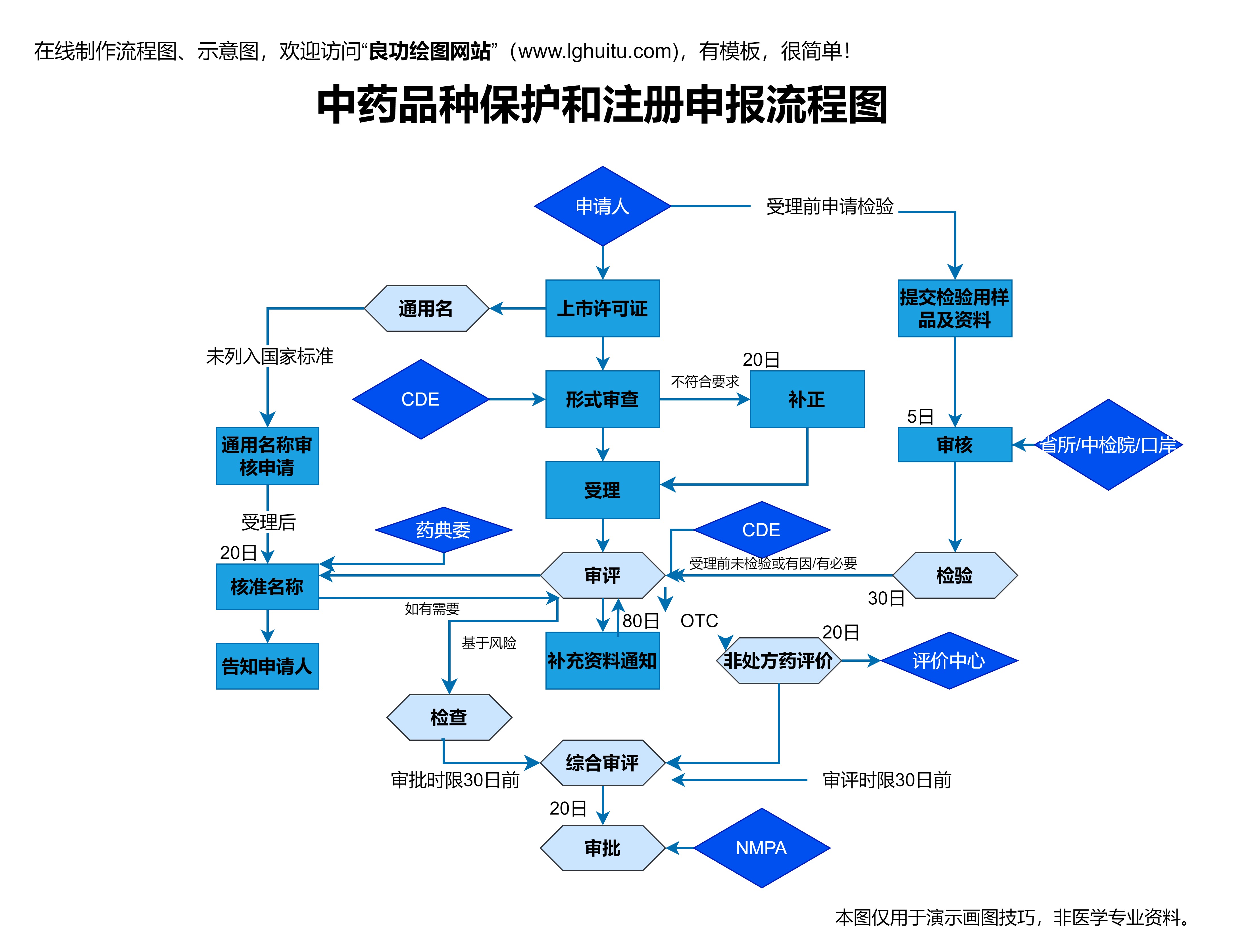
2020版药品注册管理办法的实施不仅有利于药品研发和生产企业,也有助于提高我国药品的国际竞争力。随着新药证书的高效发放,越来越多的创新药物能够迅速走向市场,解决患者未被满足的医疗需求。这不仅提升了公众对药品注册工作的信任度,也为我国医药行业的持续健康发展奠定了坚实基础。
值得一提的是,随着全球药品注册的国际化发展,药品注册管理办法的变化也顺应了国际接轨的趋势。2020版药品注册管理办法的出台,标志着我国药品注册管理在遵循国际药品审批标准方面迈出了重要一步。这一变化为国内制药企业提供了更加广阔的国际市场准入机会,也提升了我国药品的国际竞争力。
尤其对于那些有志于进入全球市场的中国制药企业而言,能够获得新药证书并顺利完成注册审批,不仅能够确保产品在国内市场的合法性,也能够在更广阔的国际舞台上进行推广。这一政策的实施,有望加速国内药品在国际市场的认可和上市,进一步促进我国制药行业的转型升级。
与此药品注册政策的优化还为跨国制药公司在中国市场的投资提供了更多的信心。随着政策的透明化和审批效率的提高,越来越多的跨国制药企业将能够顺利在中国注册和上市新药。这为国内患者提供了更多的国际先进药物选择,同时也进一步推动了我国医疗卫生水平的提高。
从更长远的角度来看,药品注册管理办法的变化对我国制药行业的未来发展具有深远影响。在全球药品市场竞争日益激烈的背景下,我国制药企业必须提升研发创新能力,尽快抢占市场先机。而药品注册管理办法的改革为企业提供了更加良好的政策环境,使其能够更加专注于药品的研发与创新,加快从研发到上市的步伐。
更重要的是,药品注册的高效推进,不仅仅是对制药企业的支持,也直接惠及广大患者。在新药证书的高效发放下,创新药物能够更快地进入市场,带给患者更多的治疗选择。这无疑是药品注册政策改革的核心价值所在——通过提高审批效率和加强监管,确保患者能够尽早享受到最新、最先进的药物治疗。
总结来看,2020版药品注册管理办法的实施,为中国药品注册带来了革命性的变化。从简化审批流程到提升注册透明度,再到对药品安全性和有效性的严格把控,这一系列措施无疑推动了中国药品注册管理迈向更加高效、规范的新时代。而随着新药证书的顺利发放,制药行业将在激烈的市场竞争中更加稳健前行,为全球患者带来更多创新的治疗方案。