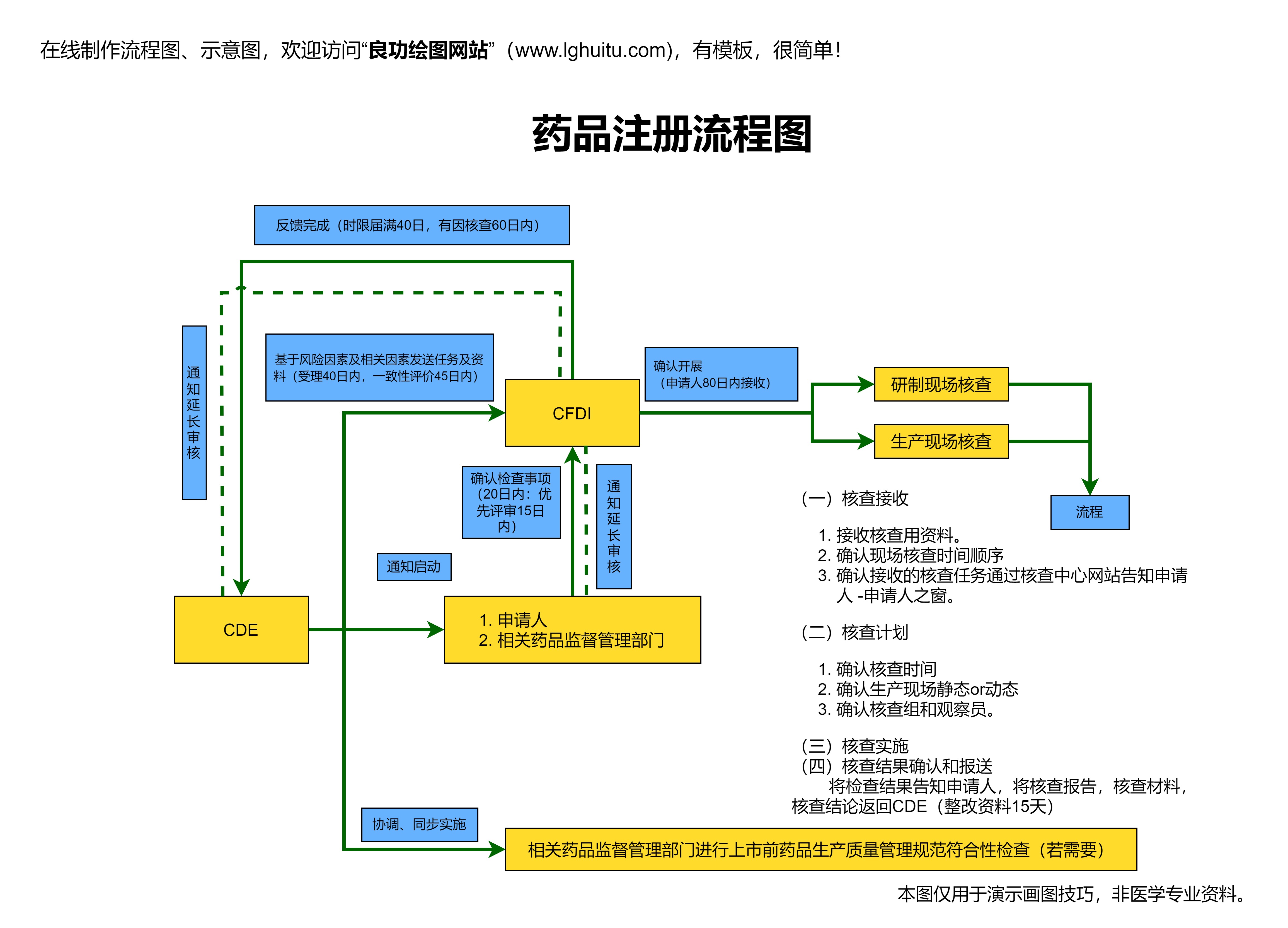
在中国药品市场中,药品的审批流程繁复且严格,尤其是中成药的准字号审批更是行业内关注的焦点。中成药作为传统中医药与现代科技结合的产物,具有深厚的文化底蕴和广泛的应用市场。想要让一款中成药成功上市,必须经过严格的审查与审批过程,其中“中成药准字号”便是其中至关重要的一环。
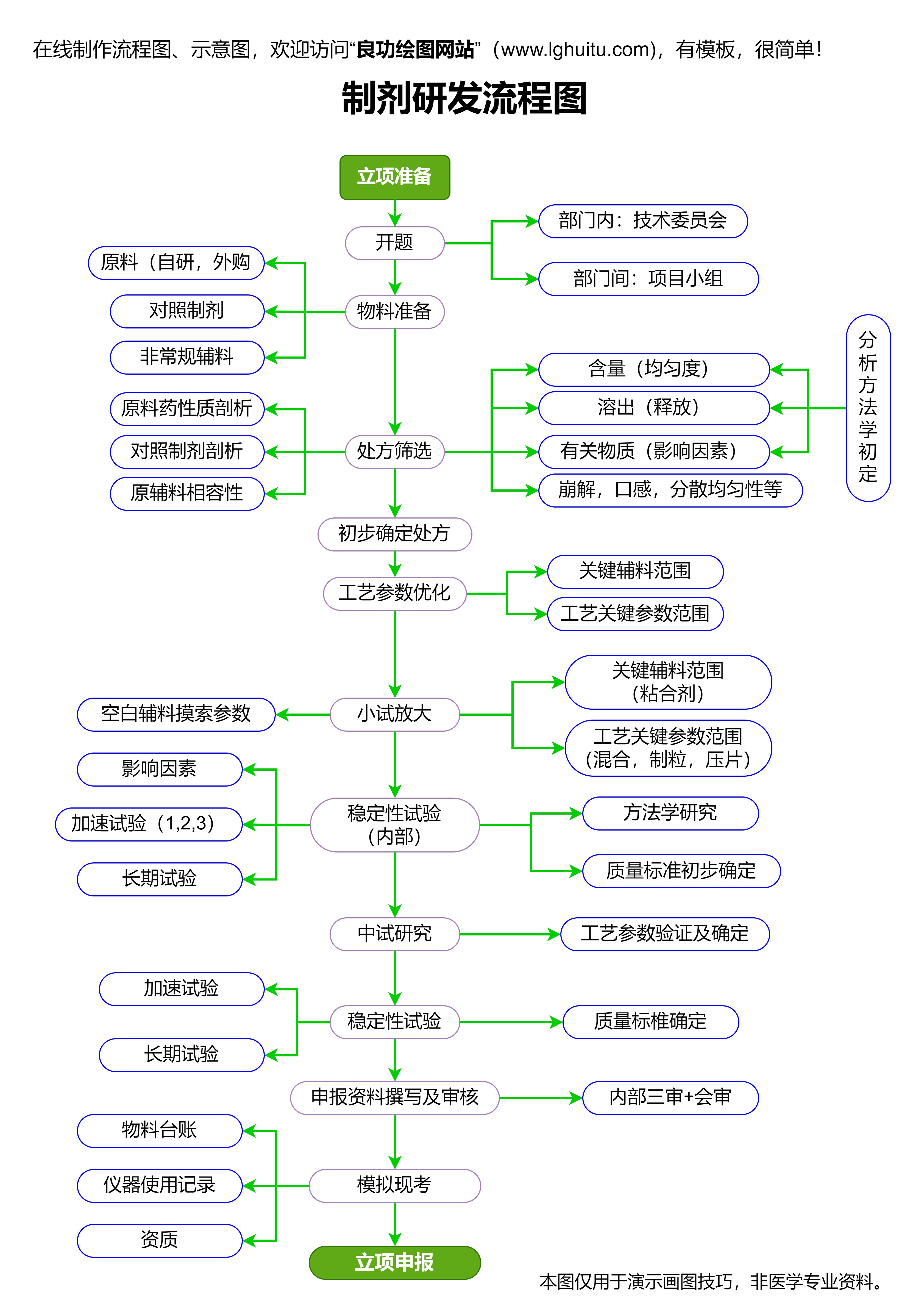
“中成药准字号”是指国家药品监督管理局(NMPA)对某种中成药的注册批准,并赋予其生产、销售资格的证明。这一批准标志着该中成药具备了在市场上流通的合法身份。药品的准字号审批不仅关乎药品的合法性和安全性,也关乎企业的生死存亡。因此,许多药企都将这一审批作为进入市场的“敲门砖”。
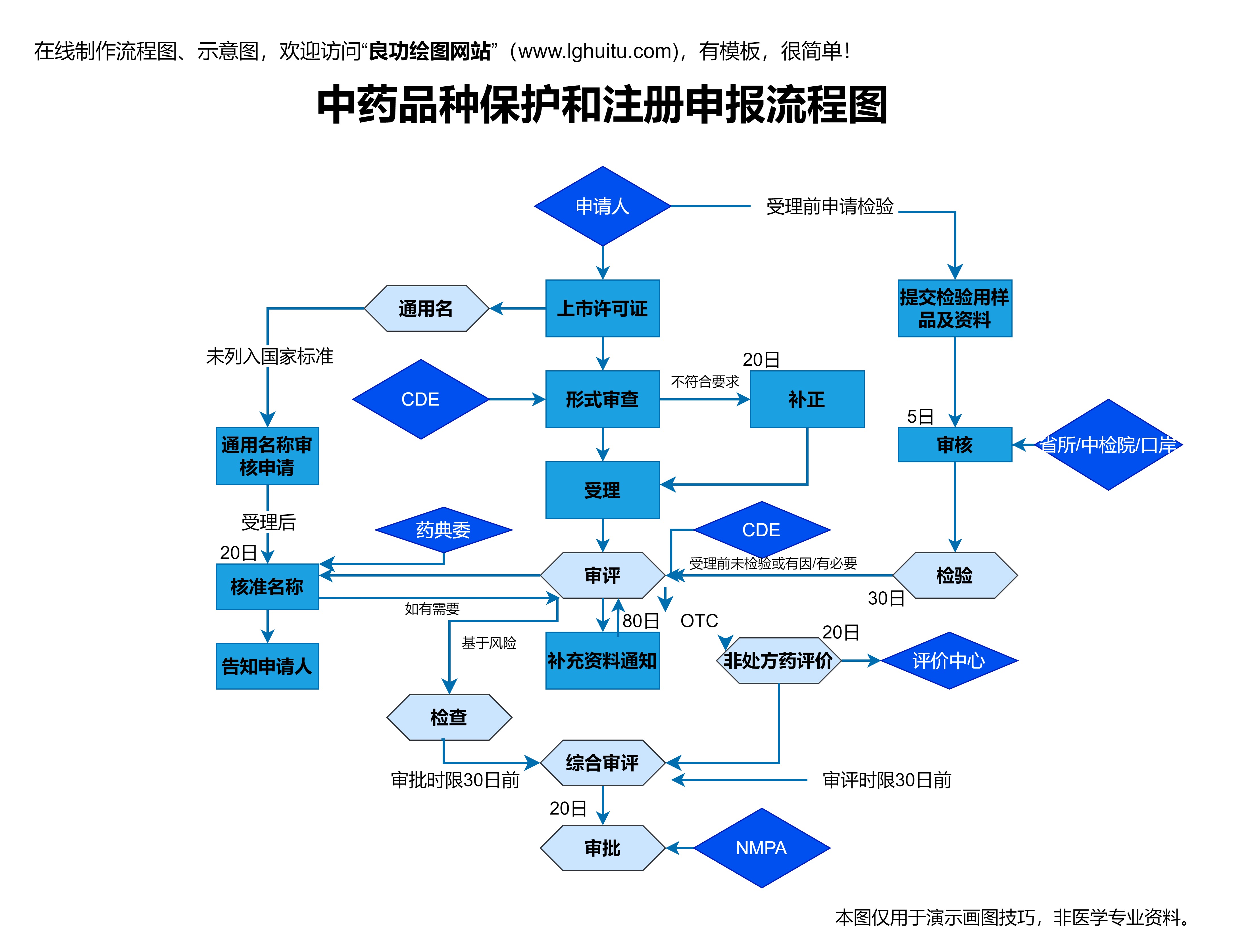
对于大多数药品来说,申请上市前都需要通过一系列复杂的审批流程。这些流程通常包括药品的临床试验、药品的质量检测、药品生产设施的检查等。而对于中成药来说,还需要额外的文化和历史背景考量。审批的具体流程大致如下:
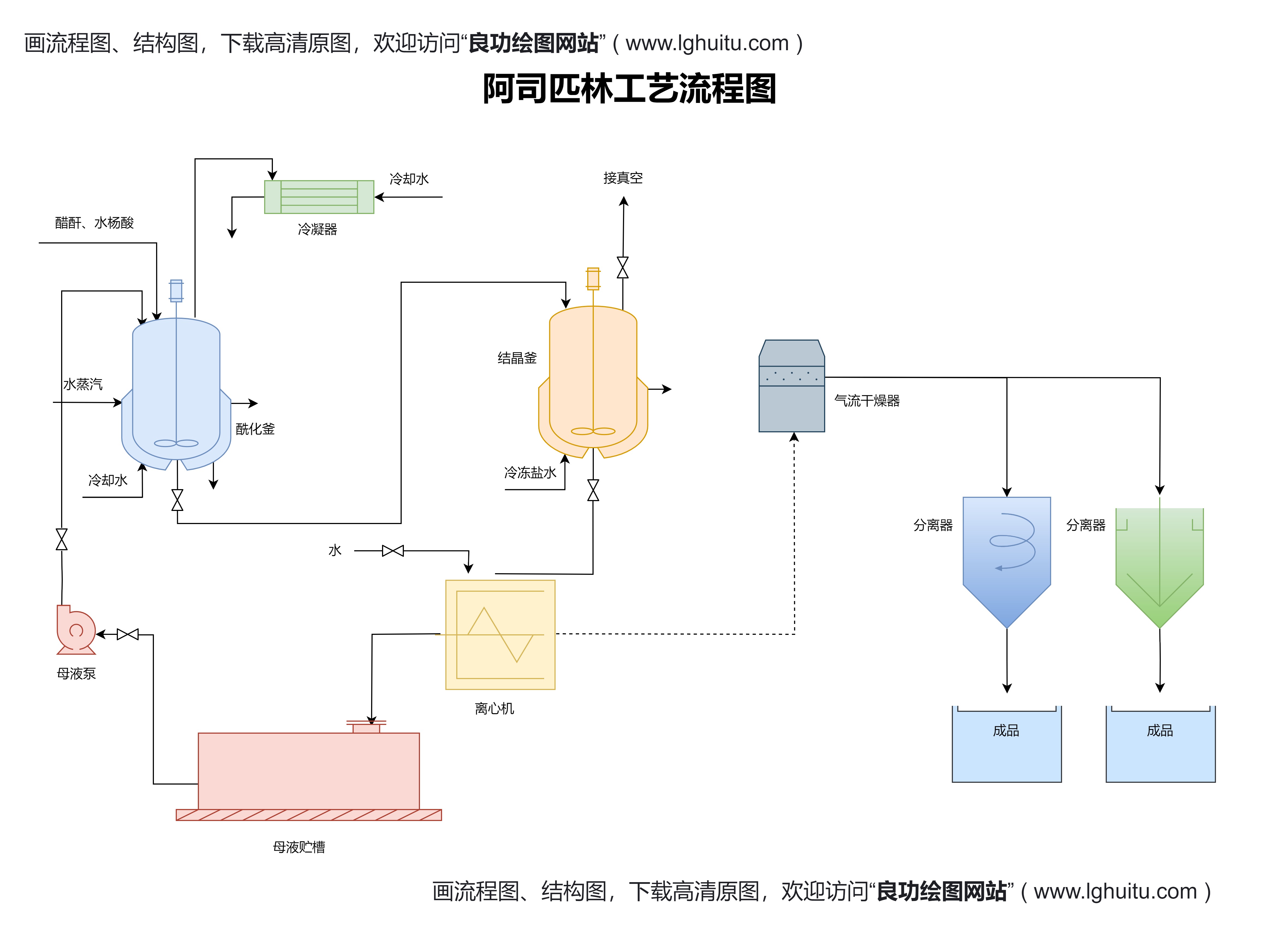
提交申请材料:企业首先需要向国家药品监督管理局提交药品注册申请材料,这些材料包括药品的研发背景、成分、适应症、生产工艺等详细信息。
临床试验与质量检测:部分中成药需要经过临床试验验证其疗效与安全性。而对于某些已经有历史应用的中成药,临床数据则可以参考现有的研究结果。与此药品的质量检测也必不可少,包括对药品的稳定性、含量等指标的检验。
生产与设施审核:药品的生产过程中需要符合GMP(药品生产质量管理规范)要求,这意味着药品生产环境、设备和人员等都需要经过相关部门的审核。
审批与发证:当所有环节都顺利通过审核后,国家药品监督管理局会发放中成药准字号,企业可以开始生产和销售该药品。
中成药的准字号审批到底需要多久才能拿下来呢?这个问题并没有简单的答案。事实上,审批周期的长短受多种因素的影响,下面是其中一些关键的影响因素:
药品的复杂程度:如果是一款传统配方的中成药,且已有大量临床数据支撑其疗效和安全性,那么审批时间相对较短。反之,如果是一款全新的配方或药物,其临床试验、质量检测等环节就会更加复杂,审批周期自然较长。
企业准备情况:药企的准备情况对审批时间也有较大影响。如果企业在提交申请前准备充分,材料齐全,且符合各项要求,审批过程将更加顺利。相反,若材料不全或存在不符合要求的情况,审批时间将大大延长。
审批部门的工作负担:国家药品监督管理局每年收到大量的药品注册申请,因此,审批的速度也可能受到其他申请量的影响。如果审批部门工作压力大,审核周期可能会延长。
政策变化:药品审批政策的变化也可能影响审批时间。例如,国家可能会对某些药品的审批流程进行简化或调整,这也会直接影响中成药准字号的审批时间。
尽管没有固定的标准时间来界定中成药准字号的审批周期,但一般来说,从提交申请到获得批准,大约需要1到3年的时间。特别是对于一些需要进行临床试验和质量检测的药品,时间可能会更长。因此,企业在申请过程中需要做好充分的准备,并预留充足的时间来应对可能出现的各种情况。

近年来,随着中医药产业的快速发展,国家对中成药的审批政策也不断进行优化和调整。尤其是在国家大力推动中医药现代化、产业化的背景下,药品审批的速度和效率逐步提高。
优先审评通道:对于一些具有创新性或重要公共卫生意义的中成药,国家药品监督管理局设立了优先审评通道。这类药品在提交申请后,会得到更高优先级的审批,审批时间大大缩短。
审评流程简化:为了提高审批效率,国家对部分符合条件的中成药采取了简化审批流程。这意味着,如果药品已有足够的临床数据和市场应用经验,审批周期可以得到有效压缩。
绿色通道政策:针对一些符合传统中医药理论、对疗效和安全性已有充分验证的中成药,国家实施绿色通道政策,快速审批。这类药品能够在更短的时间内获得准字号,帮助药企尽快将产品推向市场。
数据共享与协同审评:随着技术的发展,药品的审评过程中越来越多地采用数据共享和协同审评机制。这意味着,在审批过程中,企业可以借助更全面的数据支持,加速审批的进程。相关部门之间的协同工作,也能使得整个审批流程更加顺畅。
尽管中成药准字号的审批周期受多种因素的影响,但药企在申请过程中可以采取一系列措施来缩短审批时间:
提前做好准备:申请前,企业应确保所有材料准备齐全,尤其是临床试验数据和质量检测报告等。提前进行预审,确保资料无遗漏或错误。
选择合适的审批通道:企业可以根据药品的特点,选择合适的审批通道,如优先审评或绿色通道,以缩短审批时间。
加强与主管部门的沟通:在申请过程中,企业可以积极与药品监管部门沟通,了解审批进度并及时解决审批过程中可能出现的问题。
灵活应对政策变化:随着国家对中成药政策的不断调整,企业应时刻关注相关政策变化,灵活调整申请策略,以适应新的审批要求。
虽然中成药准字号的审批时间有时较长,但通过企业的精心准备和合理规划,审批周期是可以有效缩短的。企业在面对这一过程时,需要充分理解药品审批的各个环节,并根据自身情况做出相应的优化,从而更高效地推动中成药的市场准入。