随着人们健康意识的提高,中医药行业逐渐迎来了属于它的春天。作为传统中医的“瑰宝”,中成药不仅在国内市场备受青睐,更逐渐走向国际舞台,成为全球消费者健康生活的一部分。在这一背景下,中成药的申请工作也愈加重要,它直接关系到药品的研发、生产及市场准入等多个方面。
近年来,随着“中医药振兴计划”的推进和“健康中国”战略的实施,中成药的市场需求日益增长。中成药作为中医药理论的产物,不仅具有疗效显著、成分天然、安全性较高等优势,更因为其独特的调理作用,得到了越来越多消费者的青睐。
根据统计数据显示,中成药在中国的年销售额已经突破了千亿元大关,并且这一市场在未来几年内仍有强劲的增长潜力。尤其是在老龄化社会逐步加剧、慢性病及亚健康问题日益严重的背景下,中成药的市场需求更是不断扩大。中成药不仅能够帮助人们预防疾病、调节体质,还能在治疗常见病、慢性病时发挥重要作用。因此,中成药产业成为了许多药企和投资者争相布局的热土。
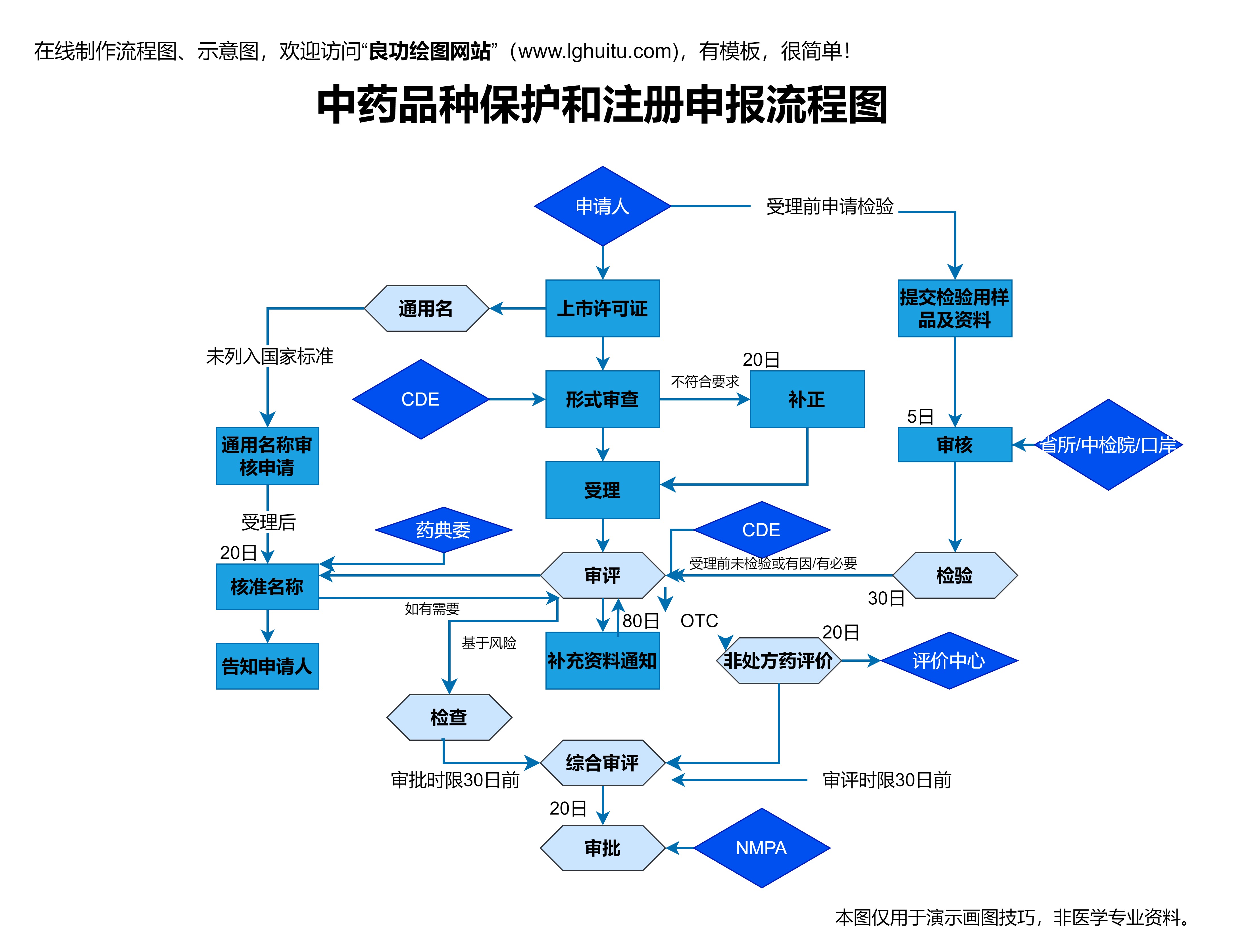
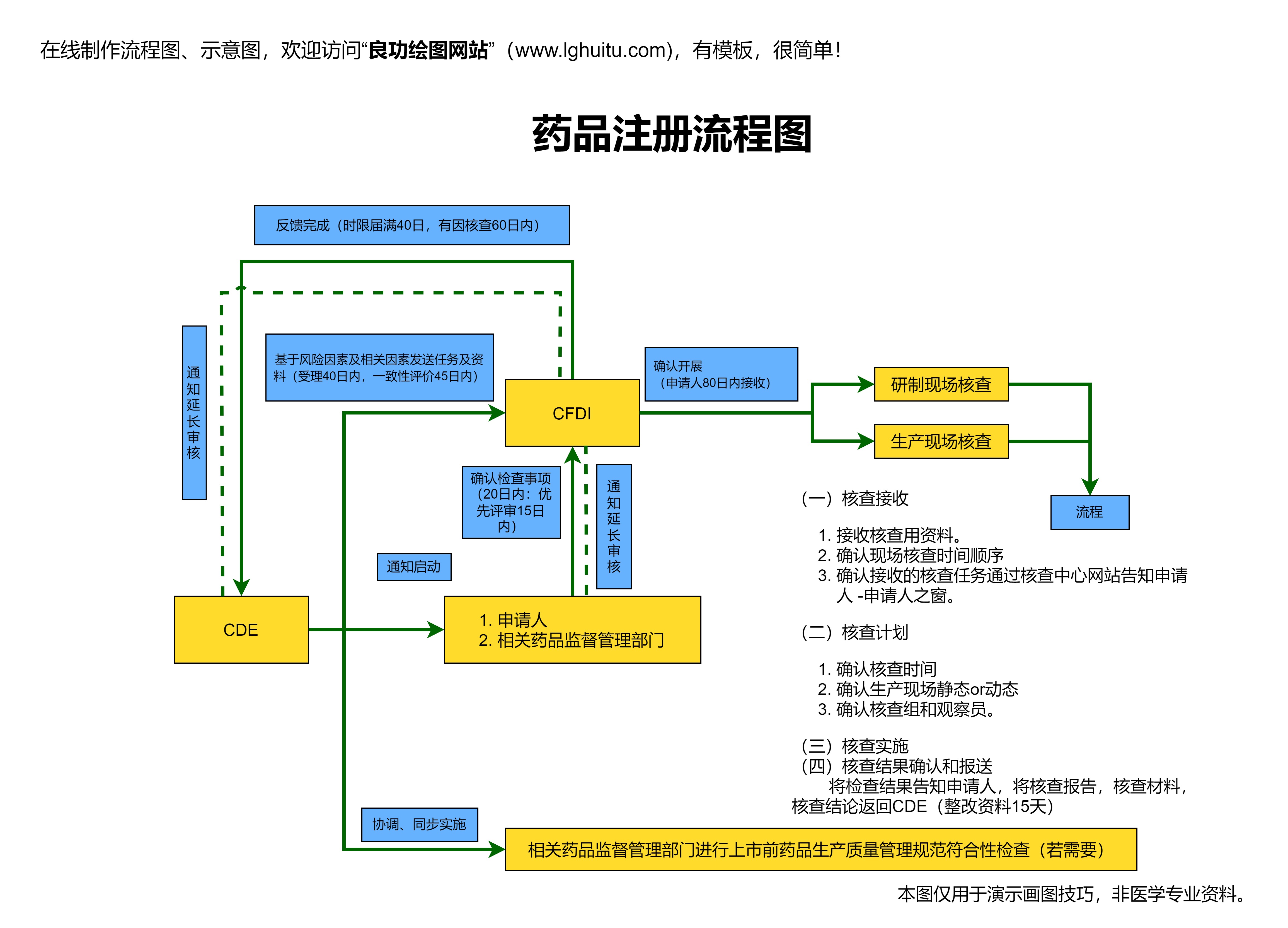
中成药的申请,首先是为了获得合法的市场准入资格。在中国,药品的上市需要经过严格的审批程序,只有经过国家药监局的批准,才能正式投入市场。中成药作为药品的一类,其申请流程与现代化西药有所不同。中成药的申请不仅需要通过临床试验、药理研究等环节,还需要对中成药的疗效、安全性、质量控制等方面进行详细的论证。
对于药企而言,中成药申请的成功与否,决定了该药品能否进入市场并获得消费者的信任。只有通过正规的申请流程,确保药品符合国家的质量标准,才能避免市场中的竞争风险。因此,中成药的申请不仅是法定的要求,更是药品成功进入市场的必要保障。
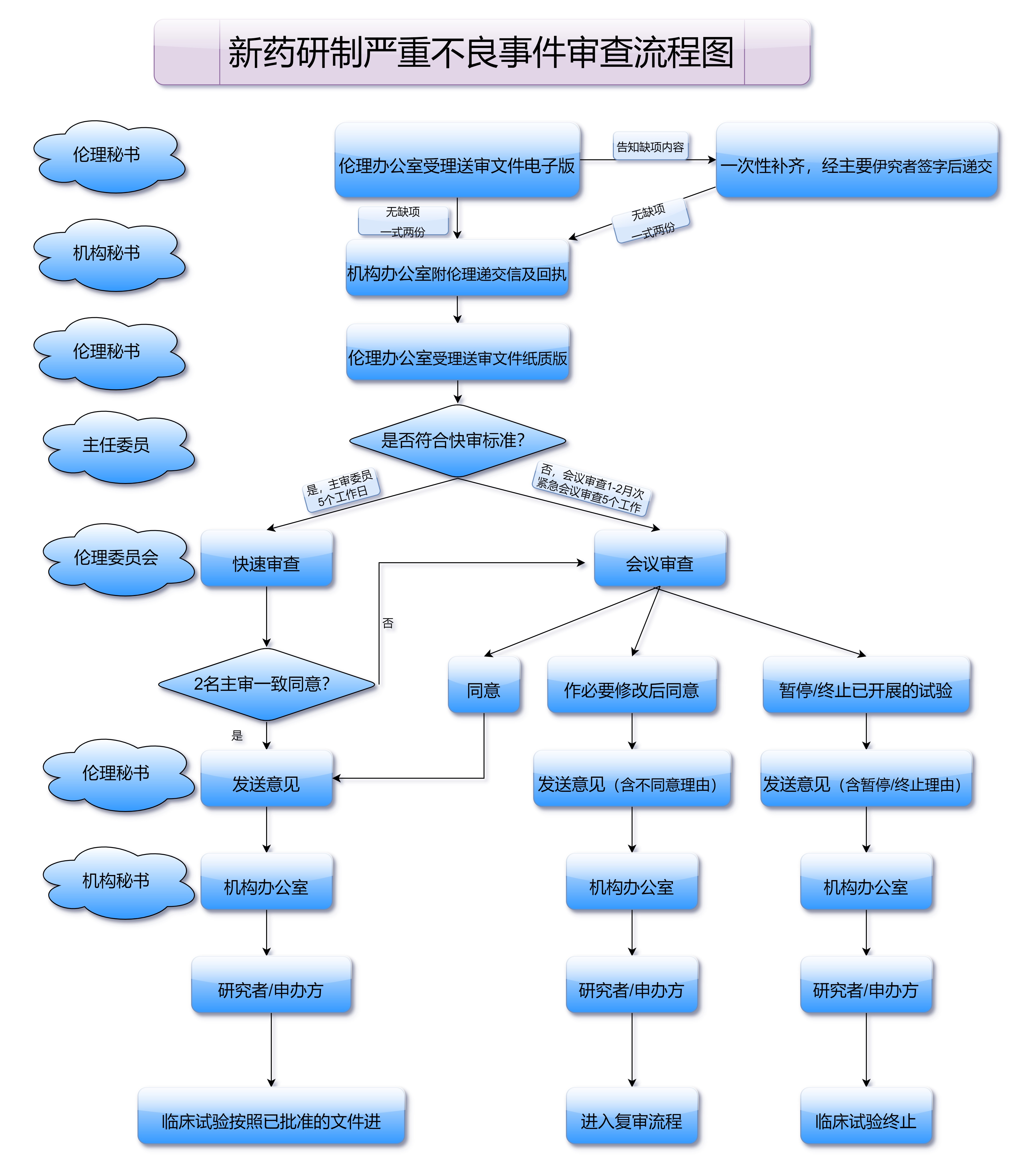
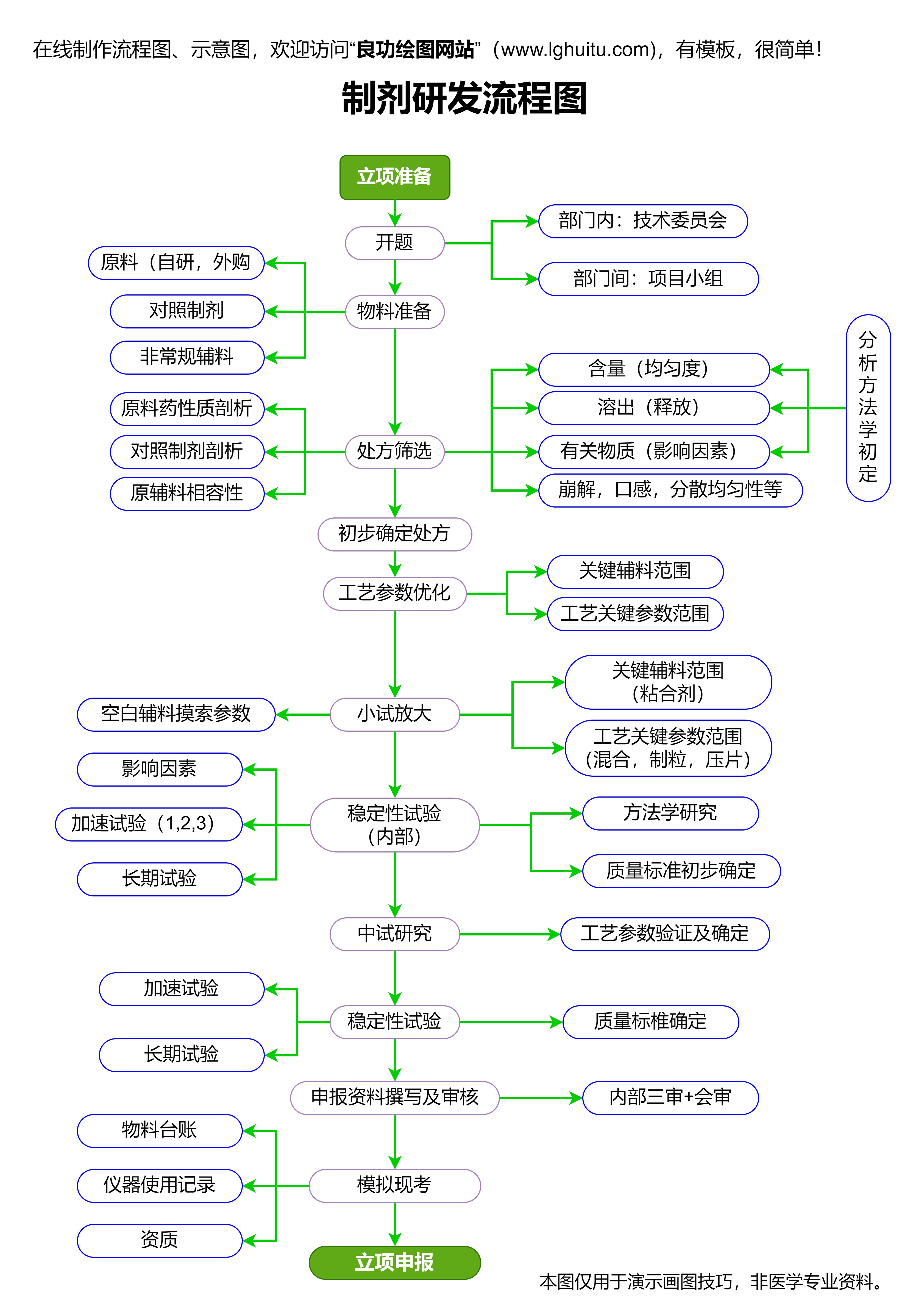
中成药申请的流程相对复杂,需要企业在研发、生产、申报等各个环节进行精细化操作。企业需要选择合适的中成药品种,并对其进行前期的科学研究,确保药品的安全性和有效性。接着,企业需要进行药品的生产工艺研发,确定药品的成分和配方,确保其在生产过程中能够达到预定的标准。

在药品的研发和生产环节完成后,企业需向国家药监局提交中成药申请书,并根据要求提供药品的相关资料。这些资料包括药品的成分、生产工艺、质量标准、临床试验结果等内容。药监局会根据这些资料对药品进行审评,必要时会要求企业提供进一步的实验数据或进行补充研究。
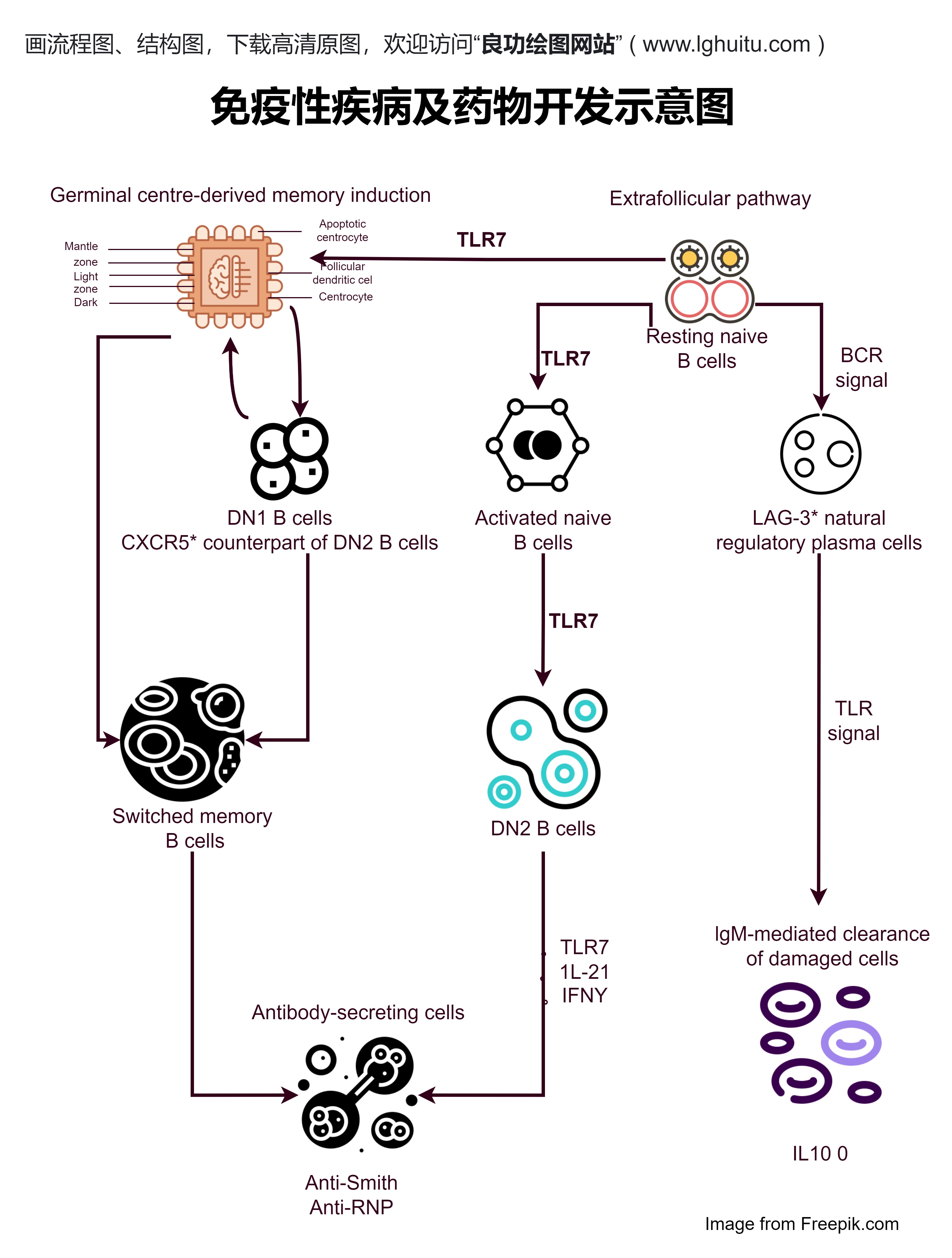
除了药品的安全性和有效性审核,药品的质量标准也是审核的重要内容。中成药的生产工艺复杂,涉及的原料种类繁多,因此,企业在申请时需要确保生产过程中严格遵循质量控制标准,避免出现质量问题。药监局会对药品的生产工艺、质量控制体系进行审核,确保其符合国家规定的药品质量要求。
中成药的研发离不开科学的理论支持和先进的技术手段。企业需要投入足够的研发资金,依托中医药理论,结合现代科技手段进行中成药的研发。注重多学科的交叉融合,采用现代药理学、毒理学等技术,提升药品的科研水平和技术含量,确保药品的安全性和有效性。
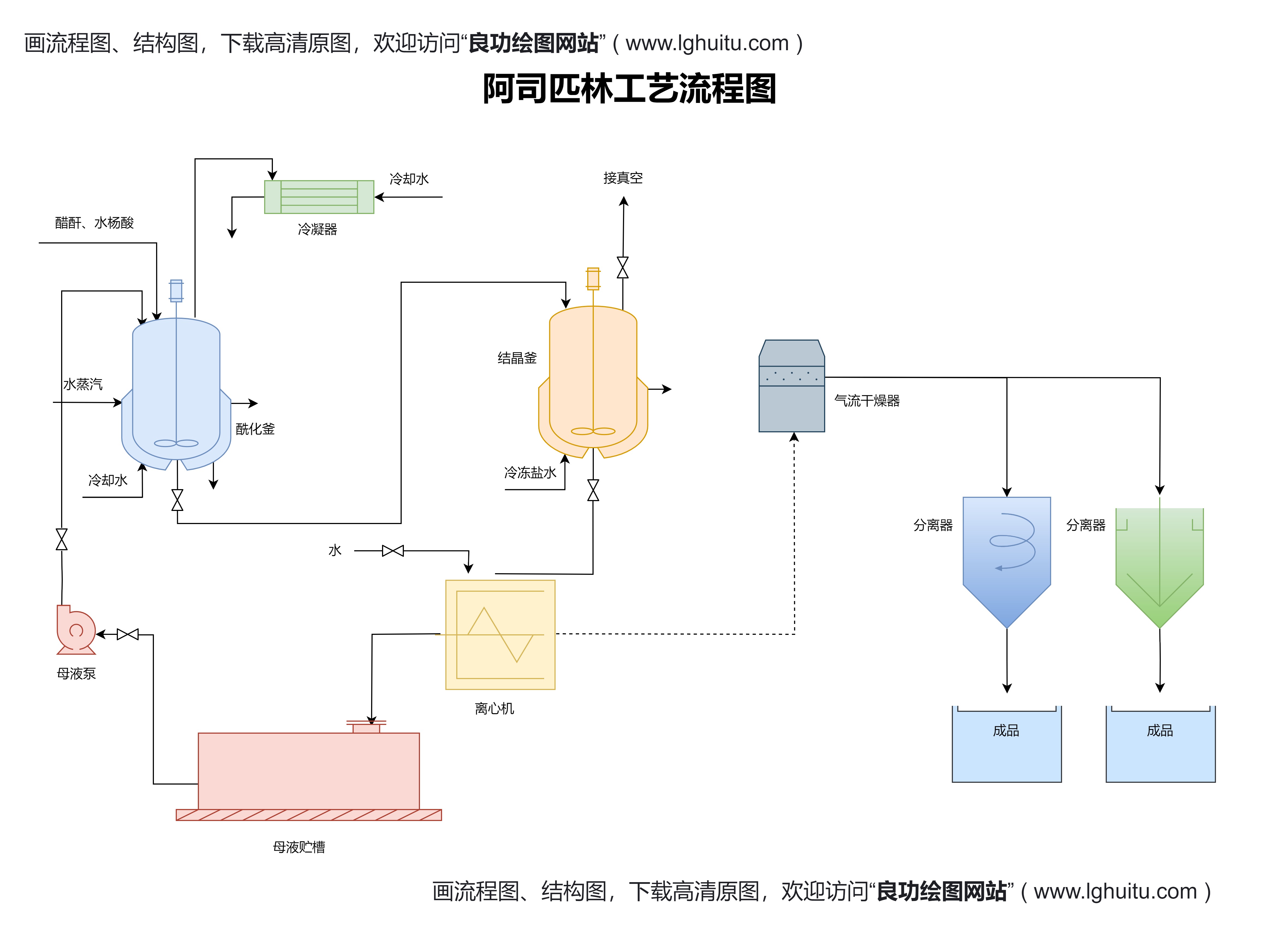
中成药的生产工艺关系到药品的质量和疗效,因此,企业应加强生产工艺的优化和升级。通过精细化管理,保证生产过程中的每一个环节都符合质量要求,提高药品的一致性和稳定性。企业还应加强与原料供应商的合作,确保药材的质量和供应的稳定性。
中成药的申请工作必须严格遵守国家的相关法律法规。企业要熟悉国家药监局对中成药申请的具体要求,提前做好资料准备,确保申请过程的顺利进行。要定期关注政策的变化和法规的更新,及时调整企业的申请策略和方案。
临床试验是中成药申请过程中不可忽视的一环。企业需要在临床试验阶段,确保药品的安全性和有效性,并对试验数据进行科学分析和总结。通过积累大量可靠的临床数据,企业可以为药品的申请提供有力的支持,提升药品的市场竞争力。