在现代生物制药行业中,抗体药物的研发是一个备受关注的话题。抗体药物不仅具有高度的靶向性,还能够有效地治疗多种复杂的疾病,如癌症、免疫性疾病、感染性疾病等。抗体药物的研发流程十分复杂,需要经历多个环节,结合多学科的知识和技术。今天,我们就来详细解读一下抗体药物的研发流程,带您走进这个充满挑战与创新的领域。
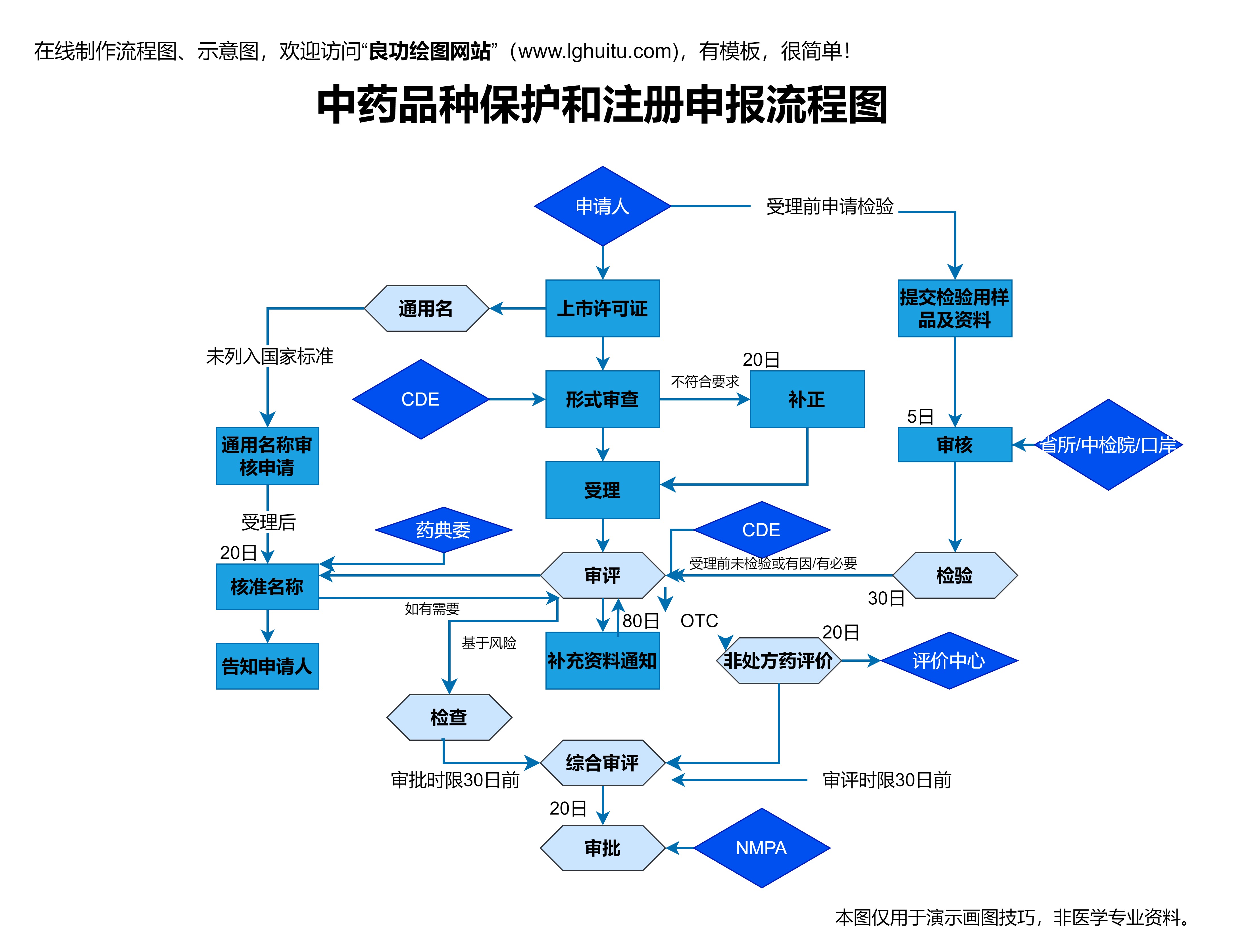
抗体药物研发的第一步是确定靶点。靶点通常是生物体内某种与疾病发生发展密切相关的分子,比如癌细胞表面的特定受体或抗原。在这一阶段,科研人员通过大量的基础研究,筛选出潜在的靶点并进行验证。
靶点的选择是抗体药物成功的关键。如果靶点选择不当,即使抗体药物设计得再完美,也无法有效地发挥治疗作用。因此,靶点验证需要通过各种技术手段,包括基因组学、蛋白质组学和生物信息学等方法,进行严格的筛选和评估。
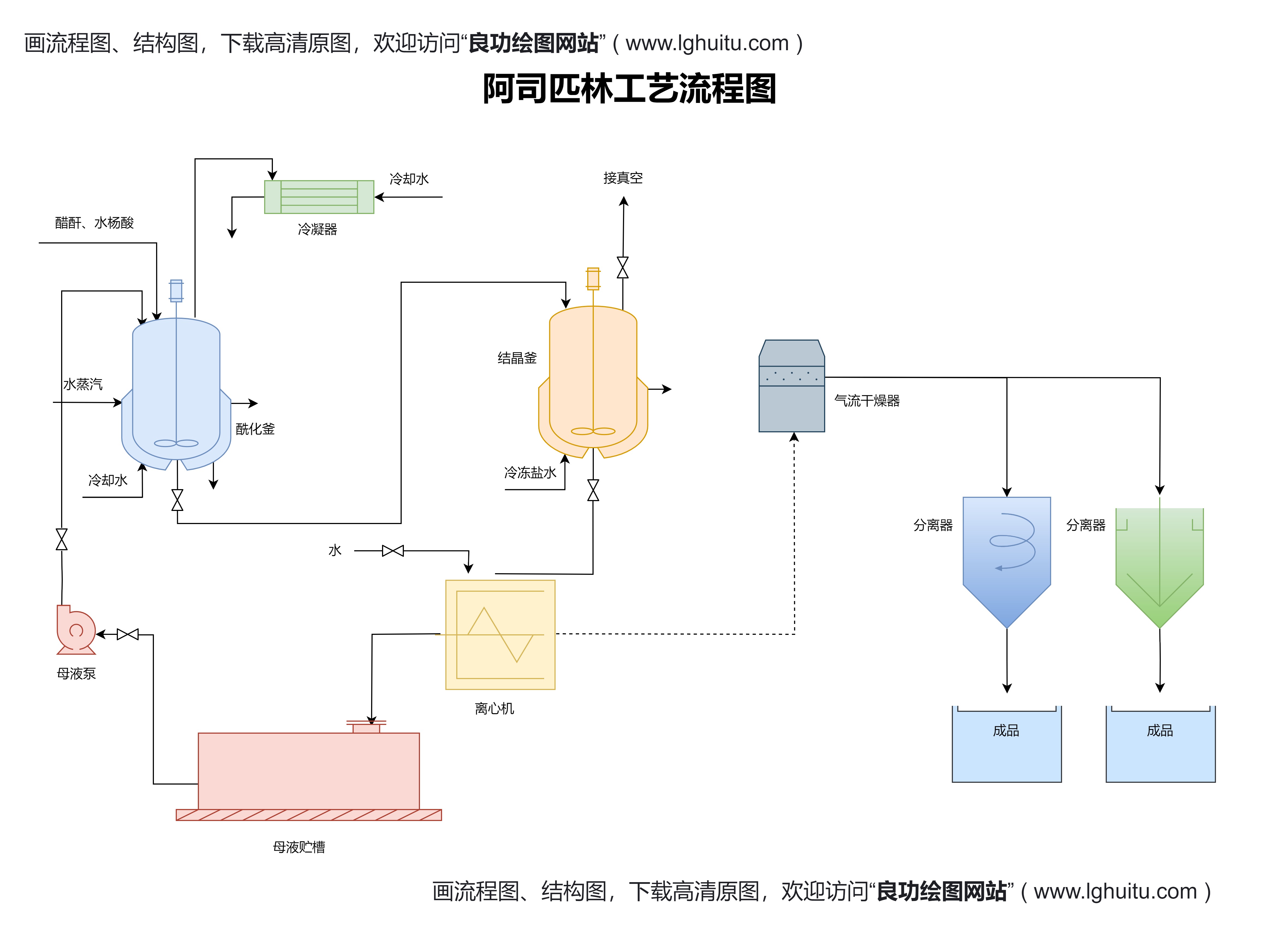
二、抗体的筛选与优化:从初步发现到高效候选抗体的诞生
靶点确定后,接下来的步骤是抗体的筛选与优化。最常见的抗体筛选方法包括单克隆抗体技术、噬菌体展示技术和基因工程技术。这些方法能够从大量抗体候选中筛选出与靶点结合力最强的抗体分子。
随着抗体筛选的完成,科研人员还需要对初步筛选出的抗体进行优化,以提高其在体内的稳定性、特异性和亲和力。抗体优化通常包括对抗体的结构进行工程化改造,增强其靶向性和免疫调节能力,以确保药物在临床应用中能够发挥最佳效果。
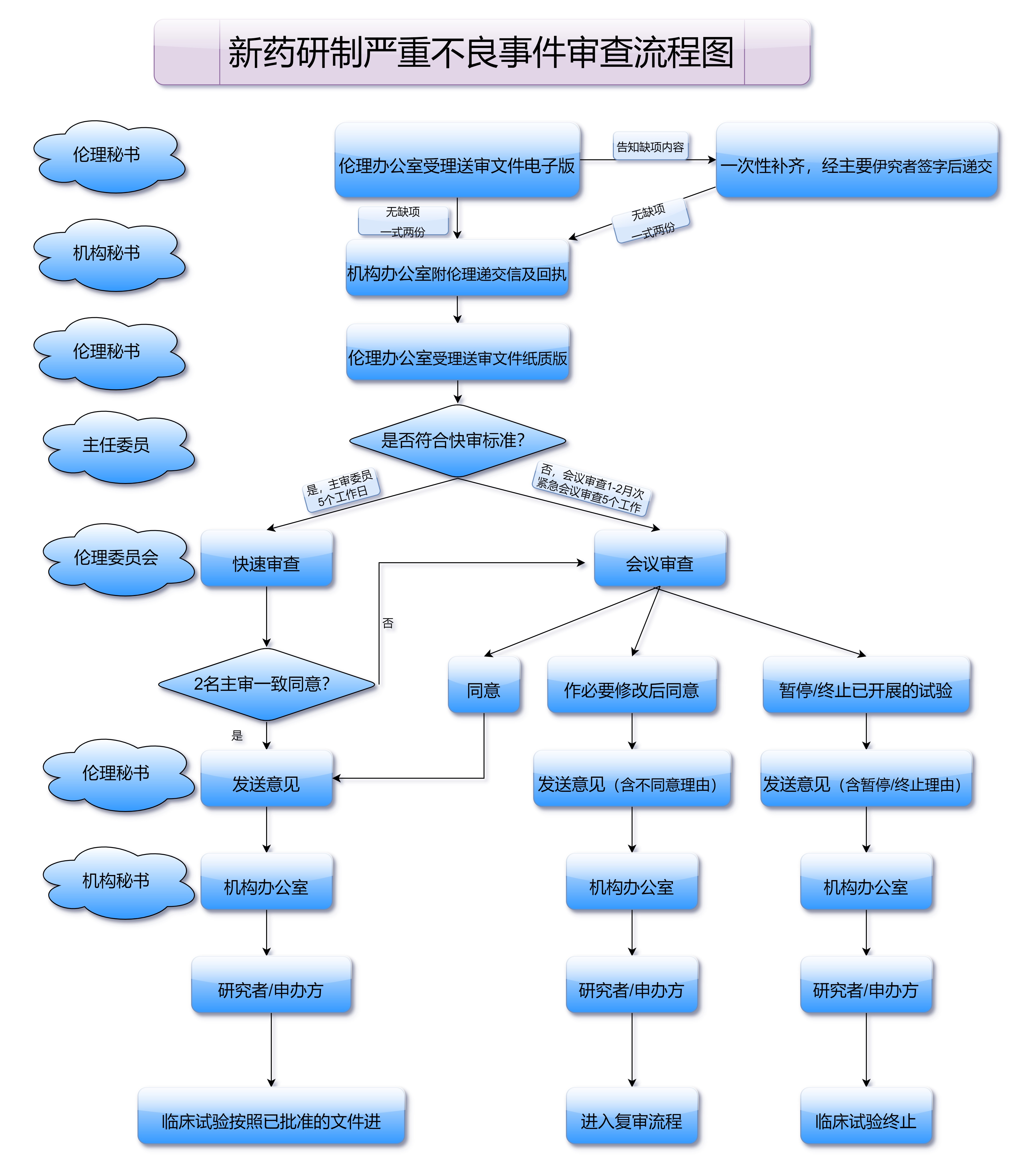
三、体外实验验证与动物实验:检验抗体的有效性与安全性
在抗体筛选与优化阶段之后,科研人员需要通过体外实验验证抗体的效果。这些实验主要是在细胞培养、免疫学试验和生化分析等方面进行,验证抗体是否能够特异性地与靶点结合,并发挥预期的功能。此阶段主要评估抗体的效价、亲和力以及与靶点结合后的生物学作用。

经过体外验证后,下一步是动物实验。在动物实验阶段,科学家们会将抗体药物注入动物体内,观察其对动物的药理作用、副作用和免疫反应。通过这些实验,科研人员能够初步评估药物的安全性和有效性,为后续的临床试验做准备。
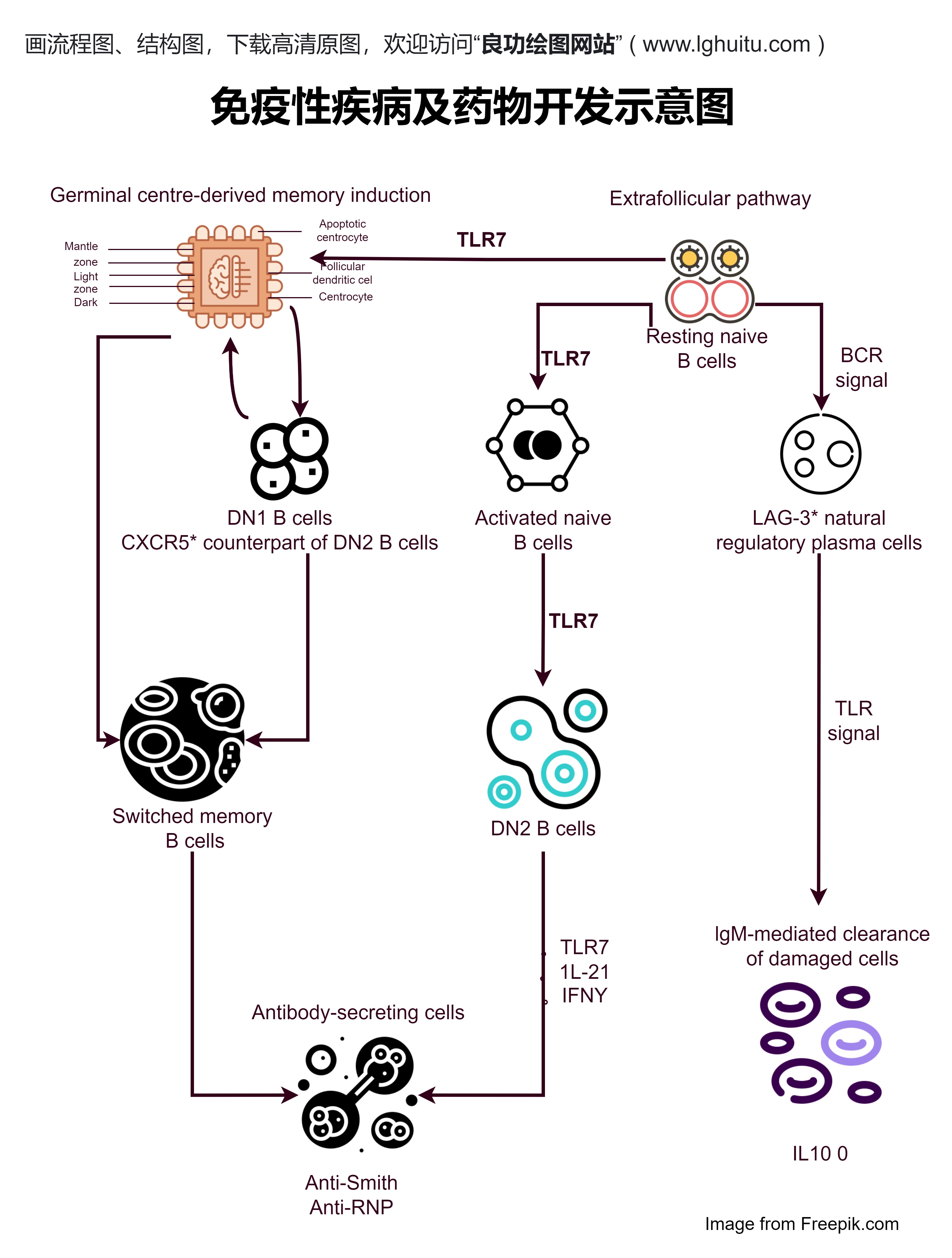
抗体药物在经过体外实验和动物实验验证后,进入临床前研究阶段。在这一阶段,药物开发公司会对抗体药物的药代动力学、毒理学等方面进行更为深入的研究。并且,在这一阶段,需要准备大量的临床前数据,为临床试验的审批提供依据。
通过临床前研究的积累,开发公司将提交相关资料向药品监管机构(如FDA、EMA等)申请临床试验的批准。监管机构会对抗体药物的安全性、有效性以及生产工艺进行评审,确保药物在临床试验中不会对患者造成不可控的风险。
一旦临床试验获批,抗体药物就进入了关键的临床研究阶段。临床试验一般分为三个主要阶段:I期、II期和III期。每个阶段的目标和试验规模有所不同。
I期临床试验:I期试验的主要目标是评估抗体药物的安全性和耐受性。一般在少数健康志愿者中进行,观察药物的基本药代动力学特性,包括药物在体内的吸收、分布、代谢和排泄等过程。
II期临床试验:II期试验主要是验证抗体药物的疗效,并继续观察其安全性。在此阶段,药物将会在小规模的患者群体中进行试验,进一步评估其治疗效果以及可能的副作用。
III期临床试验:III期试验是临床试验的最后阶段,目的是全面评估抗体药物的疗效和安全性,确保药物能够在大规模的患者中使用。III期试验通常涉及数百到数千名患者,是药物上市的关键一步。
通过临床试验后,抗体药物的开发公司需要提交完整的临床数据给药品监管机构,申请药物的上市许可。监管机构将根据试验数据、生产工艺、药物质量等多方面因素,决定是否批准该药物上市。
如果抗体药物成功获得批准,它将进入市场,供患者使用。这是抗体药物研发的最后一步,但也是最关键的一步。药物的上市并不意味着研发的结束,后续的上市后监测仍然至关重要,以便随时掌握药物在市场上的安全性和疗效。
随着生物医药技术的不断发展,抗体药物在治疗各类疾病中的应用前景广阔。未来,抗体药物不仅会在癌症免疫疗法中扮演更加重要的角色,还可能在免疫性疾病、传染性疾病等领域发挥更大作用。抗体药物研发依然面临许多挑战,包括研发成本高、研发周期长以及药物的生产和质量控制等问题。
抗体药物的研发是一项长期而复杂的任务,但它为人类健康事业带来了巨大的希望。随着技术的不断创新,抗体药物将在更多领域发挥重要作用,推动医学科学的发展。