在当今快速发展的医疗行业,新药的研发与上市不仅能够改变患者的生活质量,还能为制药企业带来巨大的商业回报。要将一个新药从实验室研究推向市场,并非一件简单的事。药品注册申报,是药品上市前不可避免的一项程序。它不仅关系到药品是否能够顺利上市,还涉及到药品的质量、安全性以及疗效等多个方面的严格审查。

药品注册是指药品在进入市场前,必须经过药品监管部门的批准,确保其符合国家法律法规的相关要求。新药品注册申报流程的最终目的是确保患者使用的药品是安全、有效且具有质量保证的。药品注册不仅是一个法律程序,更是对药品研发成果的科学验证和规范管理。
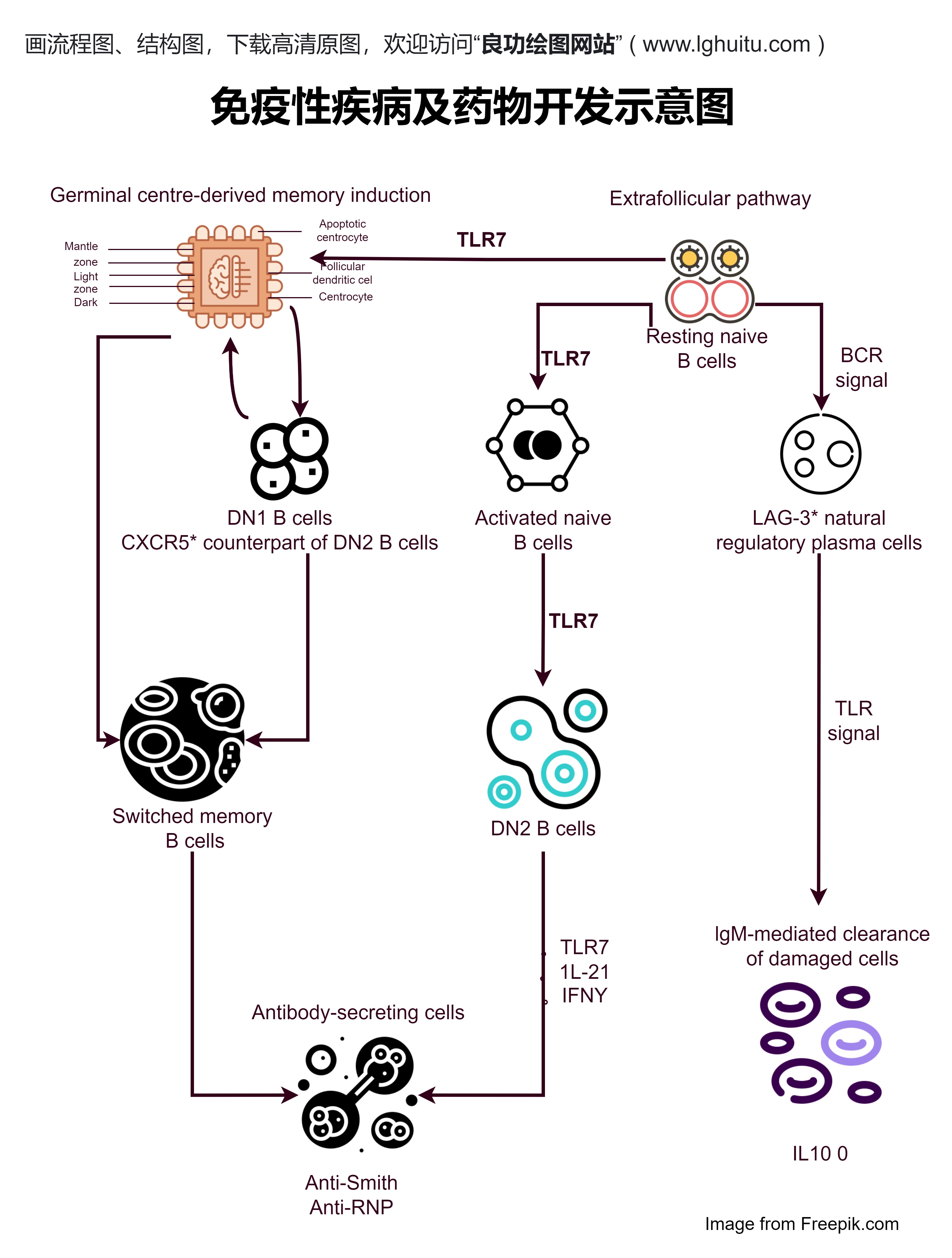
新药品的注册申报流程较为复杂,它通常包括药品临床前研究数据、临床试验数据、药品生产工艺、药品质量标准等多个方面的内容。这些内容需要通过专业的药品注册机构进行审查、批准,并最终决定药品能否进入市场。
新药品的注册申报流程可以分为以下几个主要步骤:准备阶段、申请提交阶段、审评阶段、批准与上市阶段。每个步骤都需要企业和科研人员精心准备,以确保申请顺利通过。
在准备阶段,企业需要进行药品的临床前研究。这些研究通常包括药理毒理学研究、药物化学性质分析、药物代谢动力学研究等。这些研究的结果将构成新药品注册申报的基础数据之一。企业还需要制定药品的生产工艺,确定药品的质量标准,并准备相关的临床试验计划。
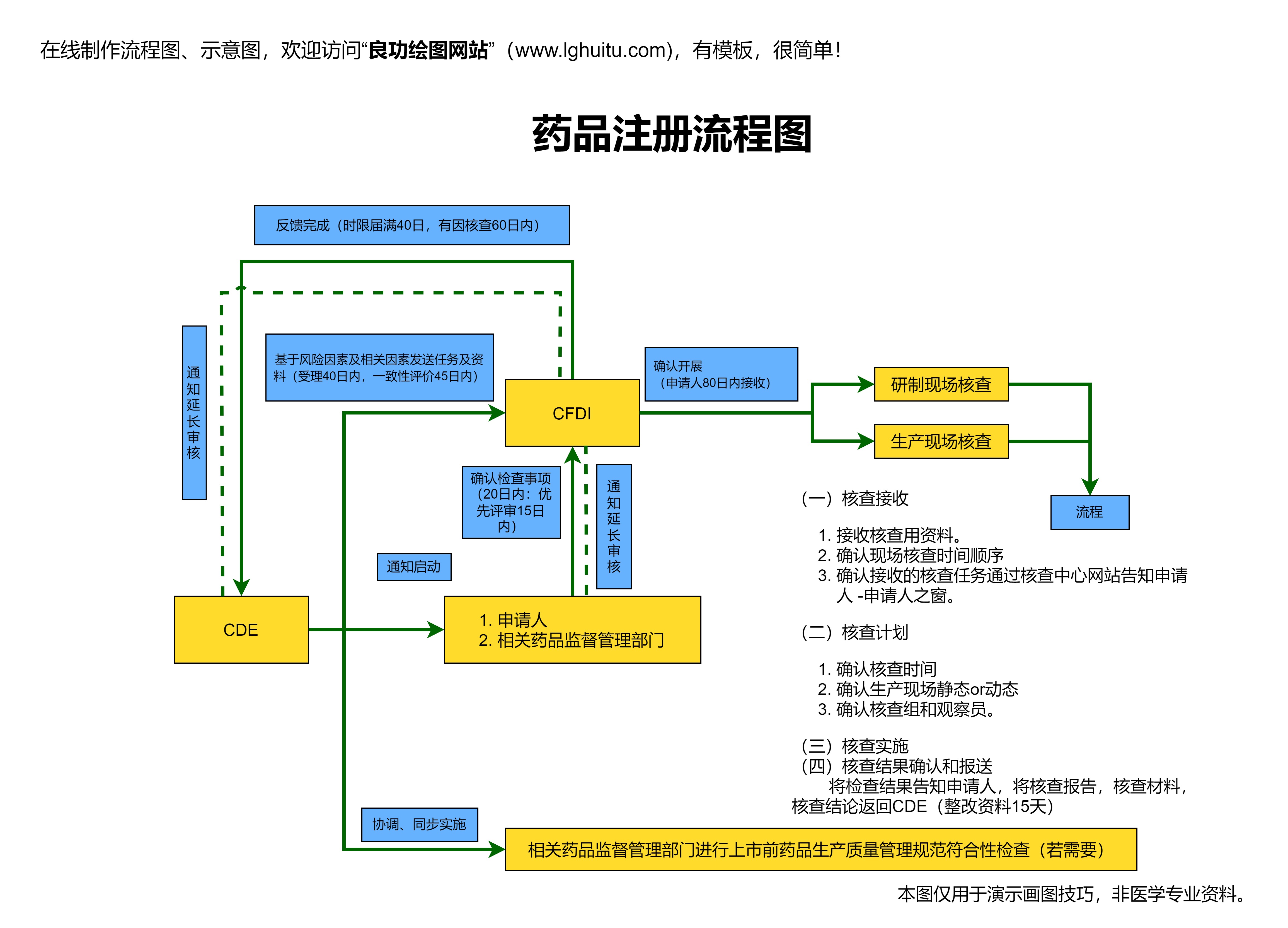
当所有的基础研究资料都准备齐全后,企业就可以向药品监管部门提交新药注册申请。在中国,药品注册申请通常需要向国家药品监督管理局(NMPA)提交。申请材料需要包括药品的基本信息、临床前和临床研究资料、药品生产工艺和质量控制标准等内容。申请文件的完整性和准确性是审批顺利与否的关键。
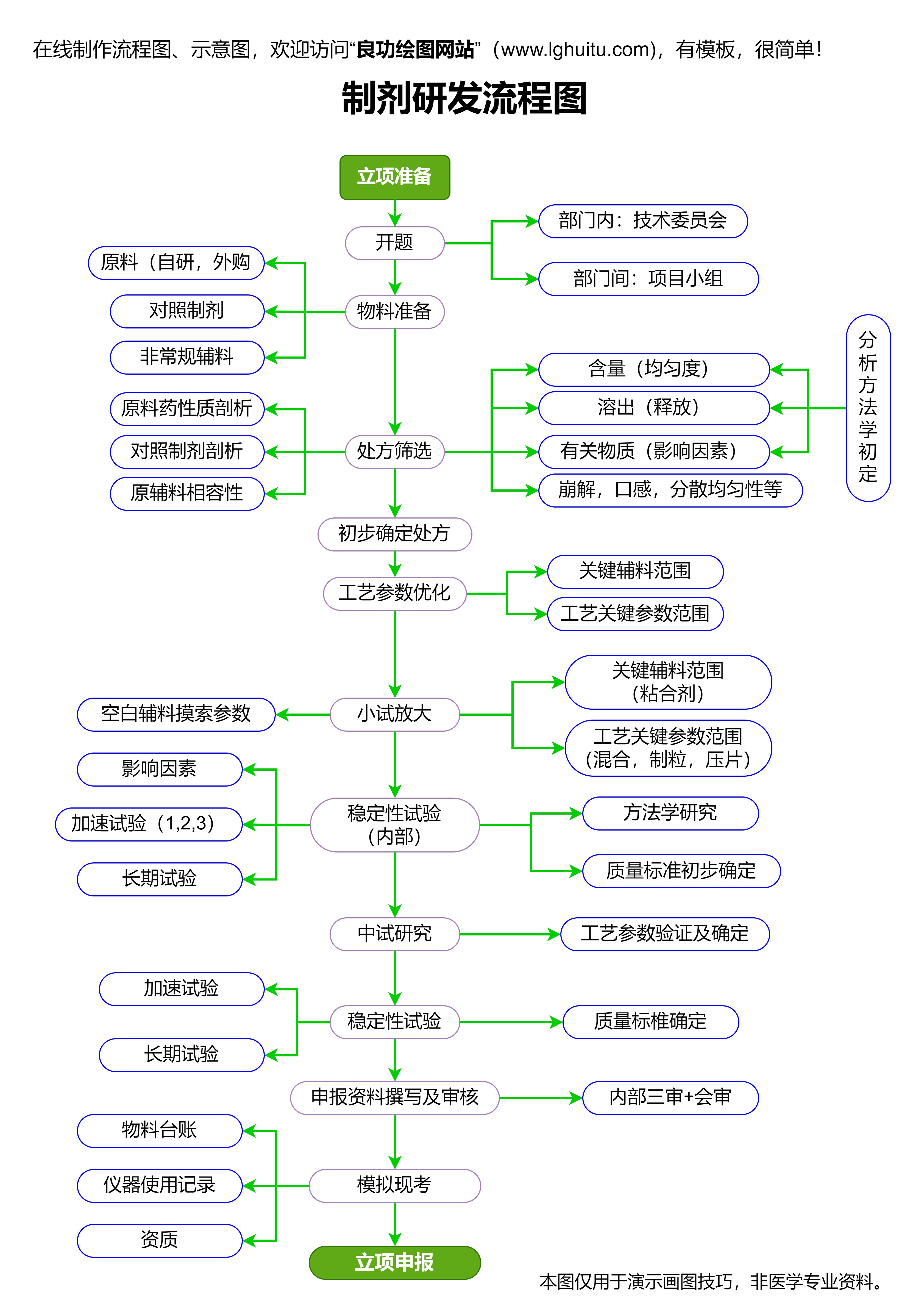
企业还需要根据药品的特性,选择适合的注册路径。对于一些创新药物,可以申请临床试验许可,并根据实际情况进行相应的临床试验。部分药物可以采用“加速审批”流程,以缩短注册周期,加快市场准入。
在提交申请后,药品监管部门将进行严格的审评。这一阶段通常由相关的专家委员会对药品的安全性、有效性、质量控制以及生产工艺等方面进行全面的审查。审评人员会对药品的临床试验数据进行仔细核查,确保药品在治疗疾病时能够达到预期的效果,并且不会对患者造成不必要的副作用。
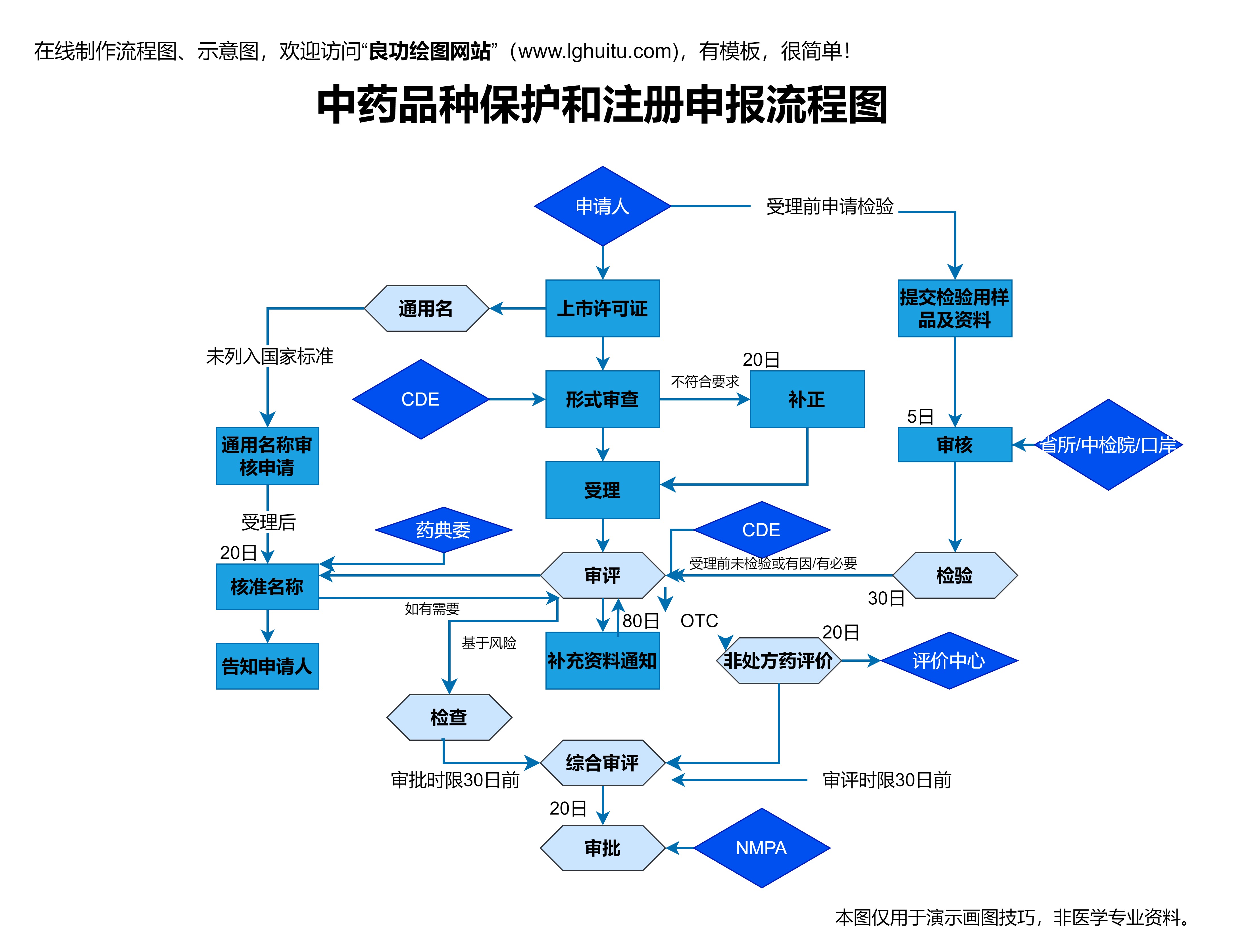
在审评过程中,可能会涉及到多轮的资料补充和修改。例如,专家会要求企业提供更多的临床数据或解释某些实验结果的原因。企业需要在规定的时间内提交补充资料,以确保审评工作能够顺利进行。
当所有审评工作完成后,药品监管部门将根据审评结果做出批准或不批准的决定。如果通过了审批,企业将获得药品注册批件,并可以正式进入市场。此时,药品可以进行生产,并进入市场销售。药品的上市后,还需要进行持续的安全监控和药物不良反应的跟踪,以确保药品在实际使用中仍然符合安全有效的要求。
尽管新药品注册申报是一个严格且充满挑战的过程,但它也是制药企业展现研发实力、进入市场的重要契机。对于药品研发团队来说,申报过程中会遇到许多挑战,如如何平衡研发的时间和成本,如何确保临床试验的科学性和可靠性等。
药品注册申报也提供了很多机遇。通过成功注册,药品不仅能够获得市场准入资格,还能够提高企业的品牌影响力,并为患者带来新的治疗方案。随着全球化的进程加速,药品的注册申报流程也在逐步与国际接轨,企业可以通过参加国际临床试验和注册,加速全球市场的扩展。
在新药品的注册申报过程中,企业需要关注多个方面的细节,以确保顺利通过审批。
药品注册申报是一个高度规范化的过程,任何环节的疏漏都可能导致申请失败或延迟。因此,企业需要严格遵循国家的药品注册法规与指南,确保所有提交的资料都符合规定。例如,药品的生产工艺必须符合GMP(药品生产质量管理规范)标准,临床试验必须遵守GLP(临床实验室规范)和GCP(临床试验规范)等相关标准。
临床试验数据是药品注册申报中最为重要的部分之一。企业需要提供充分的临床前研究和临床试验数据,证明药品的安全性和有效性。尤其是在创新药的注册申报中,企业需要提供比传统药物更多的临床试验数据,才能证明药品的创新性和市场价值。
在进行新药品注册申报时,企业应当提前对目标市场进行充分的调研,了解市场需求、竞争状况以及患者的接受度。这些调研结果不仅可以为药品注册申报提供参考,还能帮助企业在药品上市后制定科学的营销策略。
药品注册的过程可能会遇到许多不确定性,尤其是在初期的审批阶段。企业应当与药品监管部门保持密切联系,了解审批进度和审评意见,并在规定的时间内回应相关问题。这不仅能加速审批进程,还能够提升企业的注册成功率。
新药品注册申报是制药企业进入市场的必经之路。尽管这一过程复杂且充满挑战,但通过科学的准备和专业的操作,企业不仅能够顺利通过审批,还能在激烈的市场竞争中脱颖而出。未来,随着科技的进步和全球化的推进,新药注册申报的流程可能会越来越简化,但对药品的安全性、有效性和质量的要求始终不变。因此,企业在申报过程中必须时刻保持高度的专业性,确保每一个环节的合规性和严谨性,从而为患者提供更好的治疗方案,并实现自身的市场价值。