新药审批流程与审批时间,一直以来都是制药行业的焦点话题。新药的研发不仅需要突破重重技术难关,还要经历繁琐而复杂的审批程序,才能最终进入市场,造福患者。究竟新药审批是如何进行的?审批时间又是怎样计算的呢?今天,我们将带您走进新药审批的背后,揭开这道神秘的面纱。
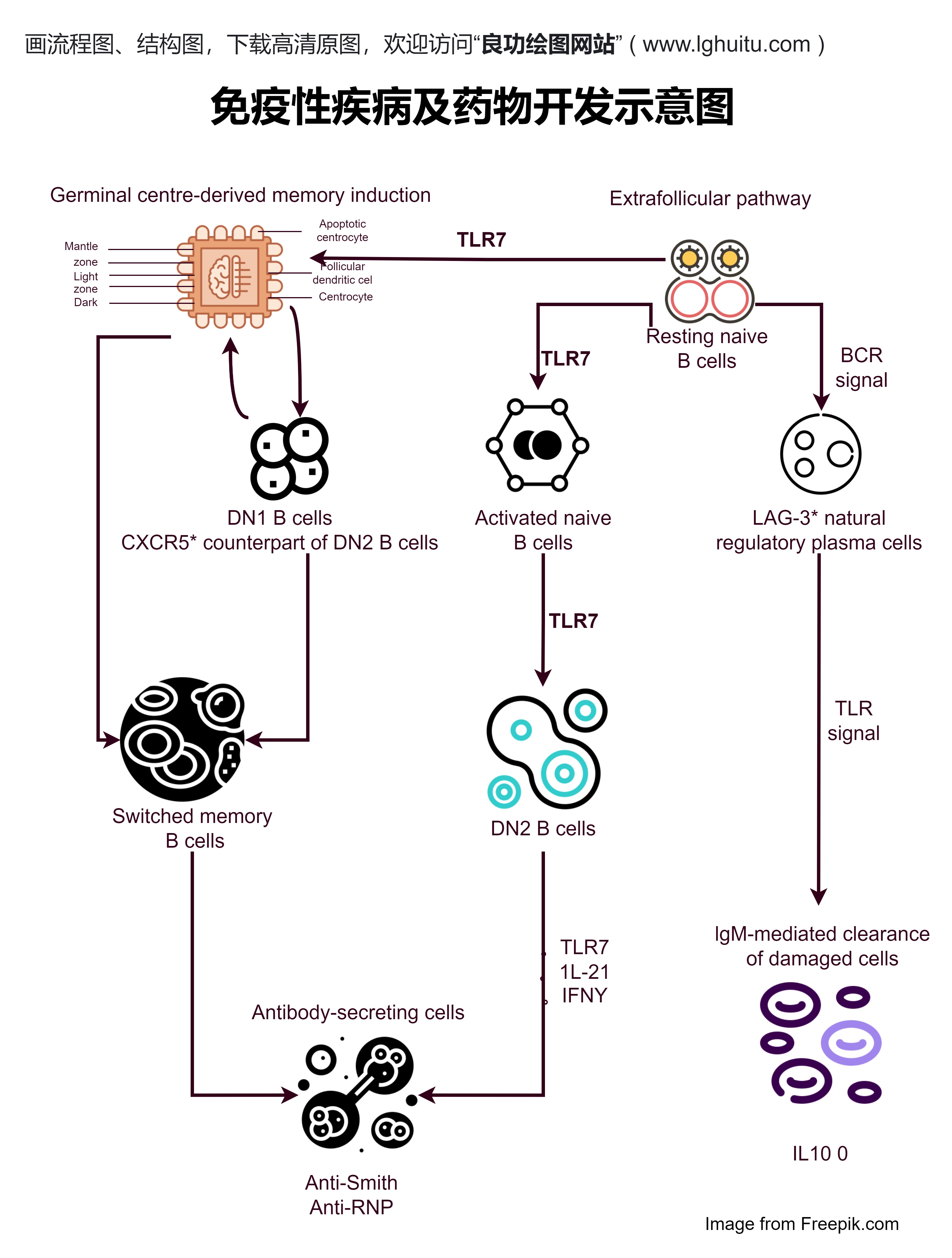
新药的审批流程一般分为几个重要的阶段,每个阶段都有其独特的要求和规定。研发公司需要提交药品研发的相关资料,证明新药的安全性、有效性和质量稳定性。这一阶段通常需要进行大量的临床实验和动物实验,以确保新药在投入市场后不会对患者造成不必要的风险。
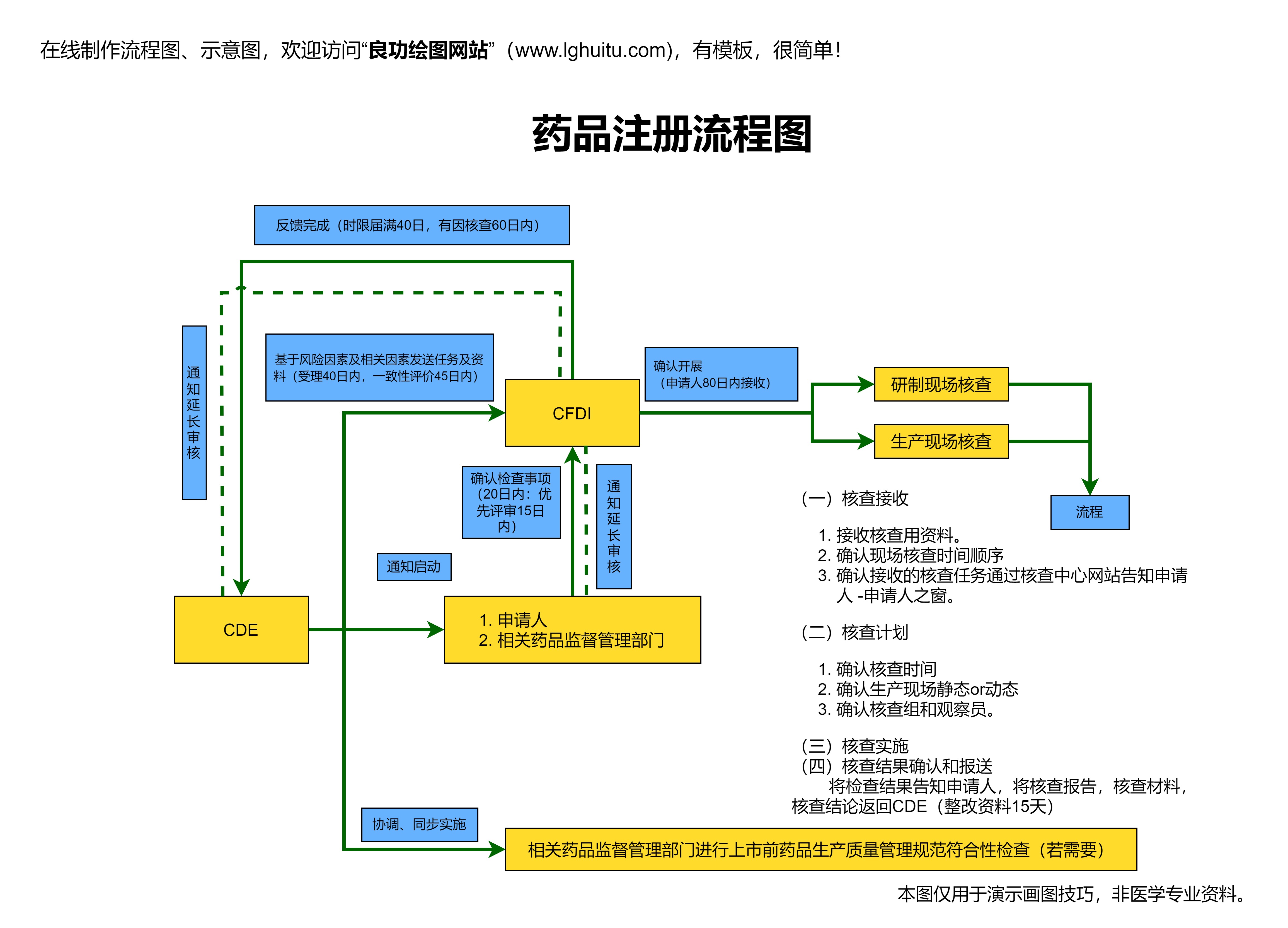
药品研发阶段:新药的研发从发现新的药物分子开始,到研发成功一款具备临床应用前景的药物,历时可能长达十年以上。研发团队需要首先在实验室环境中进行广泛的初步试验,验证药物的活性和潜在疗效。
临床试验阶段:一旦药物在实验室试验中取得一定的成功,研发公司便进入临床试验阶段。临床试验一般分为三期:
一期临床试验:主要测试药物的安全性,评估药物对人体的影响。通常在少量健康志愿者中进行。
二期临床试验:在较大的病人群体中,测试药物的疗效和副作用,为后期的广泛应用奠定基础。
三期临床试验:这一阶段是新药审批的关键,目标是确认药物的有效性和安全性,通常涉及更大规模的患者群体。
药品注册申请阶段:经过三期临床试验后,如果药物表现出良好的效果和可接受的安全性,研发公司就可以向国家药品监管机构提交药品注册申请。这一步骤包括提交大量的研究数据、临床试验报告以及生产工艺等详细资料。
审评阶段:药品监管机构收到申请后,会对药品进行详细审查,审查内容包括药物的临床数据、生产工艺、药品包装及标签等是否符合相关规定。如果所有资料都满足要求,审评专家会提出批准意见。此时,审批时间的长短与监管机构的审查效率密切相关。
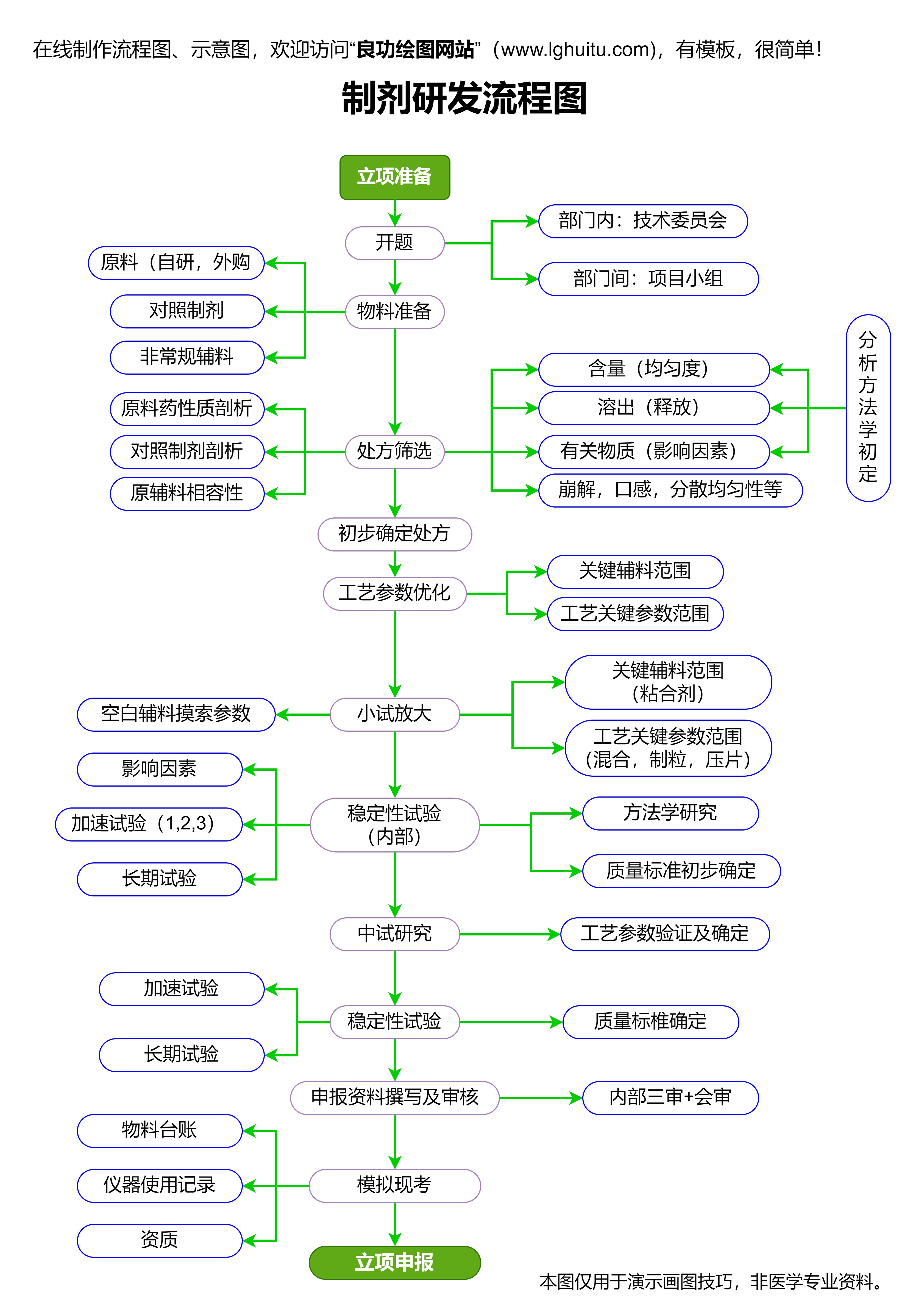
批准与上市:通过审查后,药品会被批准上市,并可以进入市场供患者使用。但上市后,药品仍然需要进行后续的药品监管和监测,确保其在长期使用中的安全性。
新药审批的时间框架受多种因素影响,其中最重要的因素包括药物的复杂性、临床试验数据的完备性、以及药品监管部门的工作负担。
药物的复杂性:不同类别的药物所需的审批时间差异很大。例如,治疗癌症、罕见病等领域的新药,通常需要更长的审批时间,因为这些药物的研发过程中,涉及到更为复杂的试验和风险评估。
临床试验数据的完整性:一个完整的临床试验数据集是新药审批成功的关键。如果临床试验数据不完整或存在缺失,审批时间可能会被延长,甚至可能影响药品的审批结果。因此,药品研发公司需要精心设计和执行临床试验,确保数据的准确性和可信度。
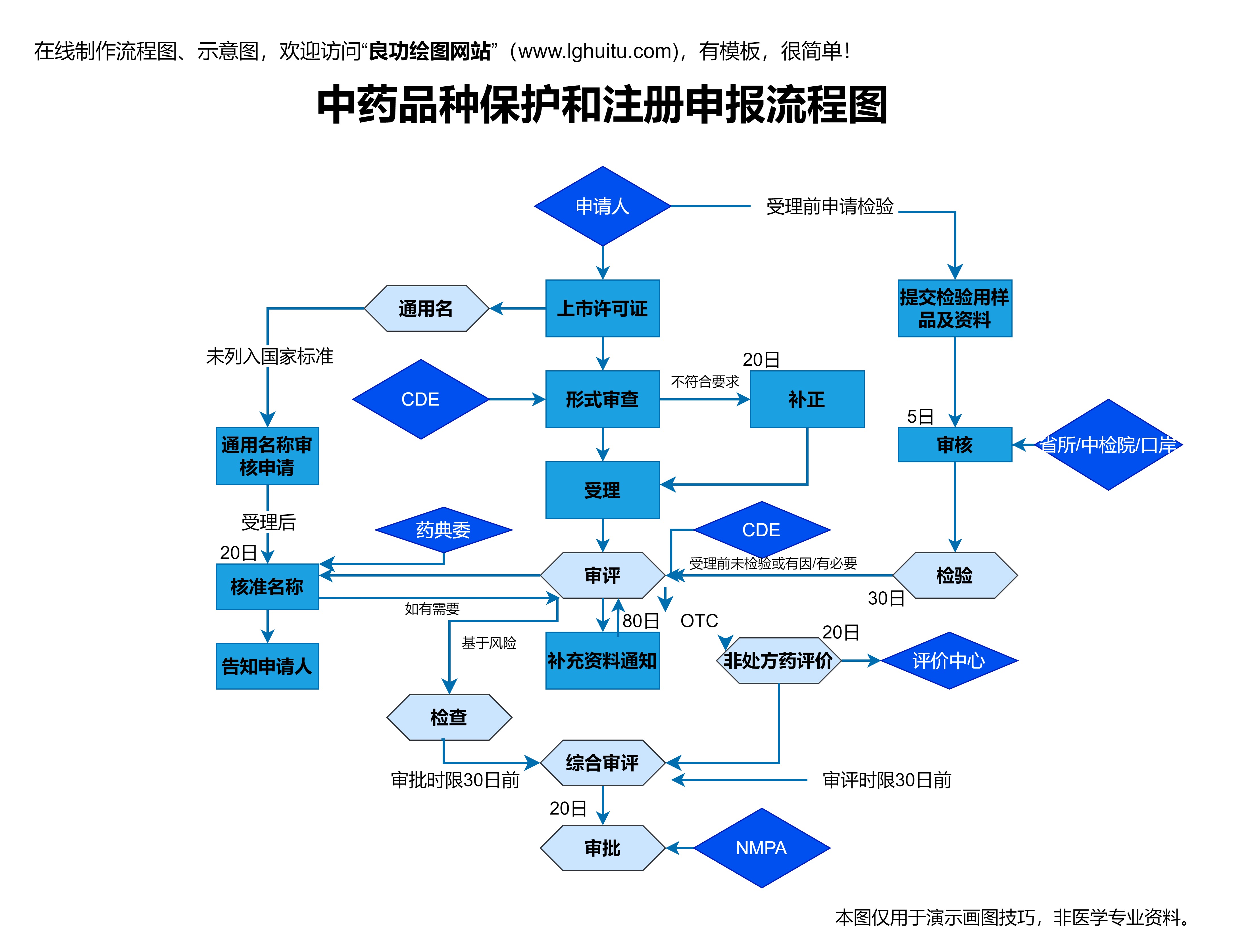
监管机构的工作负担:药品审批的速度还受到监管机构工作量的影响。当市场上有大量药品等待审批时,监管机构可能需要更长时间来审查每一项申请。这也是为什么一些国家设立了专门的快速审批通道,以加快对某些紧急药品的审批过程。
新药的审批时间与批准流程密切相关,每个环节都有可能影响药品的最终上市时间。因此,合理的审批流程和透明的审批时间对于制药行业、研发公司乃至最终的患者来说,都具有重要意义。
新药的审批时间不仅影响制药公司的资金和资源投入,还会对市场竞争产生重大影响。药品上市的延迟,往往意味着患者无法及时获得新疗法,而这可能导致疾病的治疗延误,甚至影响患者的生存机会。
患者的等待:新药审批的延迟,意味着患者可能错失最佳治疗时机。在一些急需新药的疾病领域,如癌症、艾滋病等,药物的审批时间尤为关键。每延长一天的审批,患者可能面临更多的治疗风险和生命威胁。因此,加速审批流程、缩短审批时间,对于提升患者的生存率和治疗效果至关重要。
企业的竞争力:对于制药公司而言,新药的上市时间直接影响其市场竞争力。药品上市的越早,企业就能抢占更多市场份额。竞争对手如果在同类药物上也有所突破,审批时间较长的公司可能会错失市场机遇,影响其收益和品牌影响力。因此,尽可能缩短审批时间,是制药公司追求的目标之一。

随着全球医药行业的快速发展,许多国家和地区都开始加快新药审批的速度,采用更加灵活的审批方式,尤其是在面临公共卫生危机时。例如,针对新冠疫情,各国监管机构实施了加速审批政策,允许部分药品通过紧急授权或快速审批程序进入市场。
优先审批与突破性疗法:很多国家在新药审批中设立了优先审批通道,特别是针对治疗重大疾病的药物。例如,FDA在美国设立了“突破性疗法”认证制度,对一些具有显著临床优势的新药,进行加速审批。
数据共享与国际合作:随着全球化进程的推进,国际药品监管机构之间的合作日益紧密。通过共享临床试验数据和审批经验,药品审批的效率得到了显著提高。各国药品监管部门的协调合作,有助于加快新药的跨国审批进程,推动更多创新药物进入市场。
技术手段的支持:随着人工智能、大数据等新技术的应用,药品审批过程中对数据分析和风险评估的能力不断提高。AI和大数据能够帮助审评专家更快速地筛选和分析临床试验数据,提高审查的效率和准确性。
未来,药品审批过程有望更加高效、透明和精准。随着全球药品监管体系的不断完善,审批流程将更加规范,审批时间也有望进一步缩短。对于药品研发公司和患者而言,这无疑是一个值得期待的好消息。通过不断优化审批流程,更多创新药物将能更早地进入患者的手中,为全球健康事业带来新的希望。