在现代制药行业中,研发一款新药无疑是一个庞大而复杂的系统工程。新药的研发从概念的产生,到实验室阶段的验证,再到最后的生产及上市,涉及了多个环节和层级的审批。特别是新药生产的申报审批程序,它不仅关乎新药是否能够顺利上市,更影响着药品的质量、市场竞争力以及企业的声誉。因此,理解和掌握新药生产申报审批程序,对于制药企业的成功至关重要。
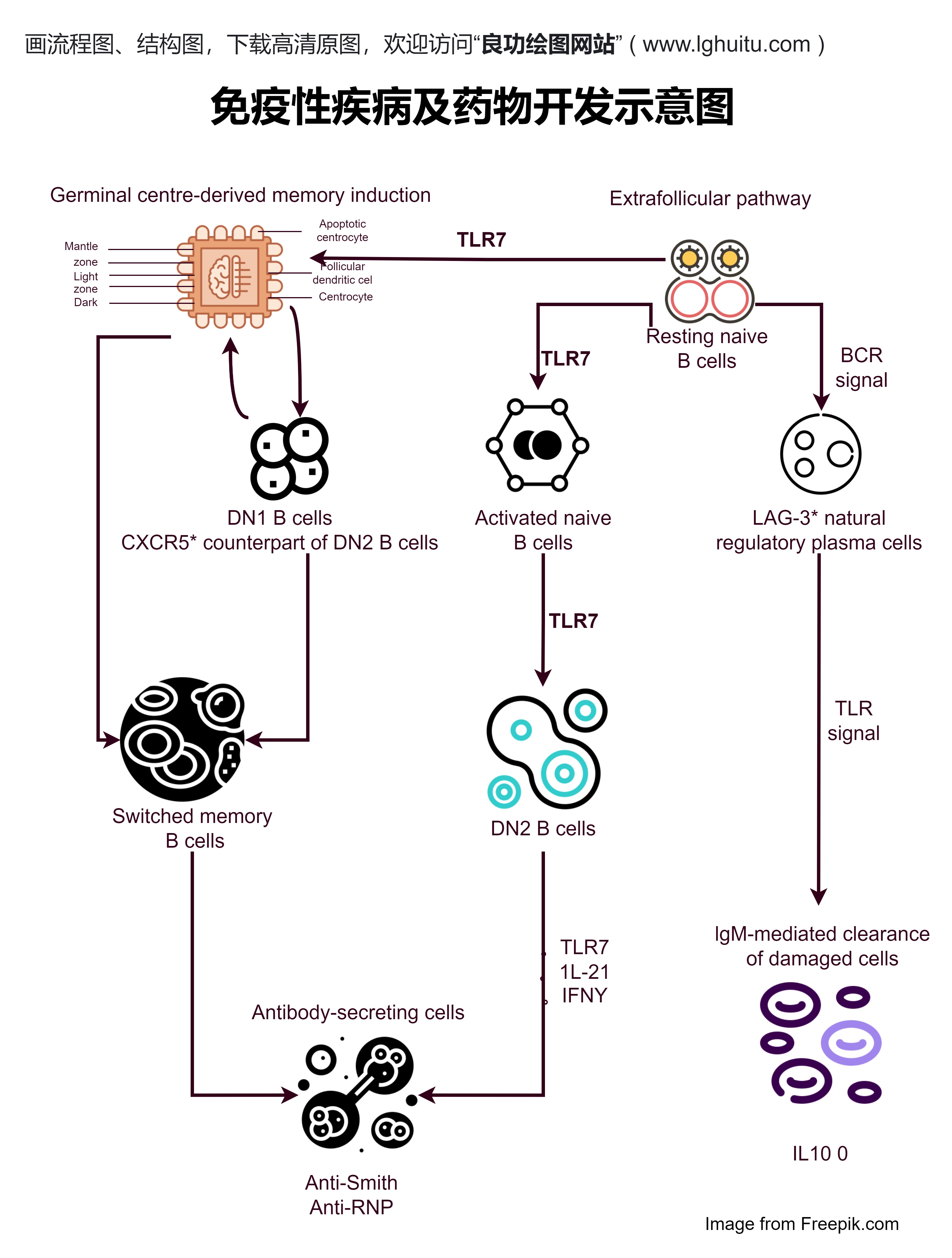
新药的生产不仅仅是一个技术性的工作,它还需要符合国家药品监管部门的严格要求。药品的安全性、有效性以及质量控制都是监管部门重点审查的内容。为了确保新药能够达到公众和市场的需求,国家设立了严格的申报审批制度,通过这一过程,确保所有上市药品都符合药品管理法的相关规定。
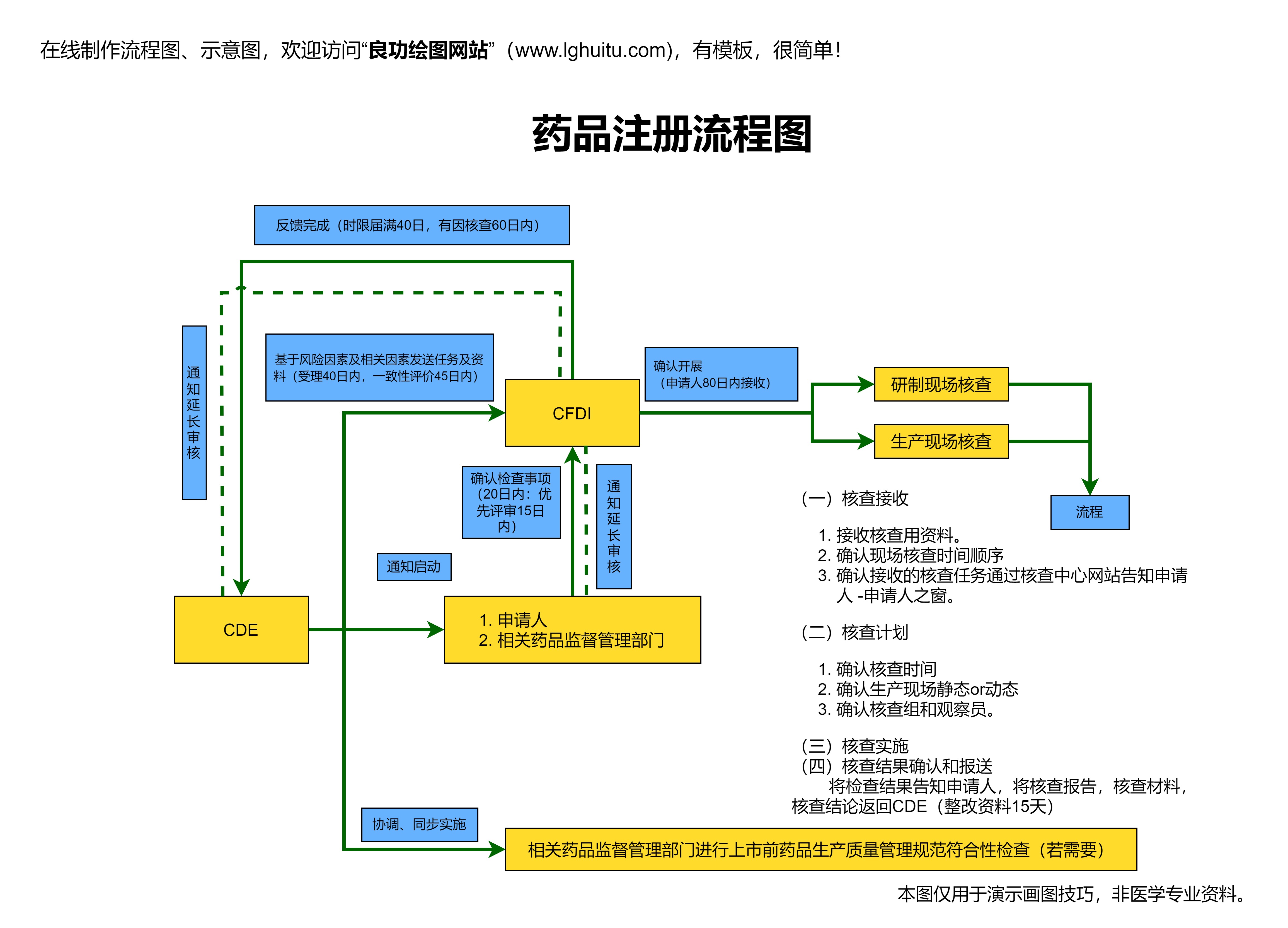
对于企业而言,掌握这一程序,了解如何进行药品生产申报,是顺利将新药推向市场的基础。只有在生产符合规定的情况下,企业才能在市场中占有一席之地,获得消费者的信任。
新药生产的申报审批流程一般包括以下几个重要步骤,每一步都充满挑战,企业必须谨慎操作,以确保顺利通过。
新药生产的申报需要企业在正式申请之前进行大量的准备工作。这包括药品的研发、临床试验、药品的生产工艺设计以及质量标准的制定等。这些准备工作不仅是药品质量的保障,也是申报过程中的必备文件材料。
在准备好所有相关资料后,企业需将新药生产申报材料提交给国家药品监督管理局(药监局)。这些材料通常包括药品的化学成分、生产工艺、临床试验数据、质量控制标准等。药监局会对这些材料进行初步审查,评估药品是否符合上市的基本条件。
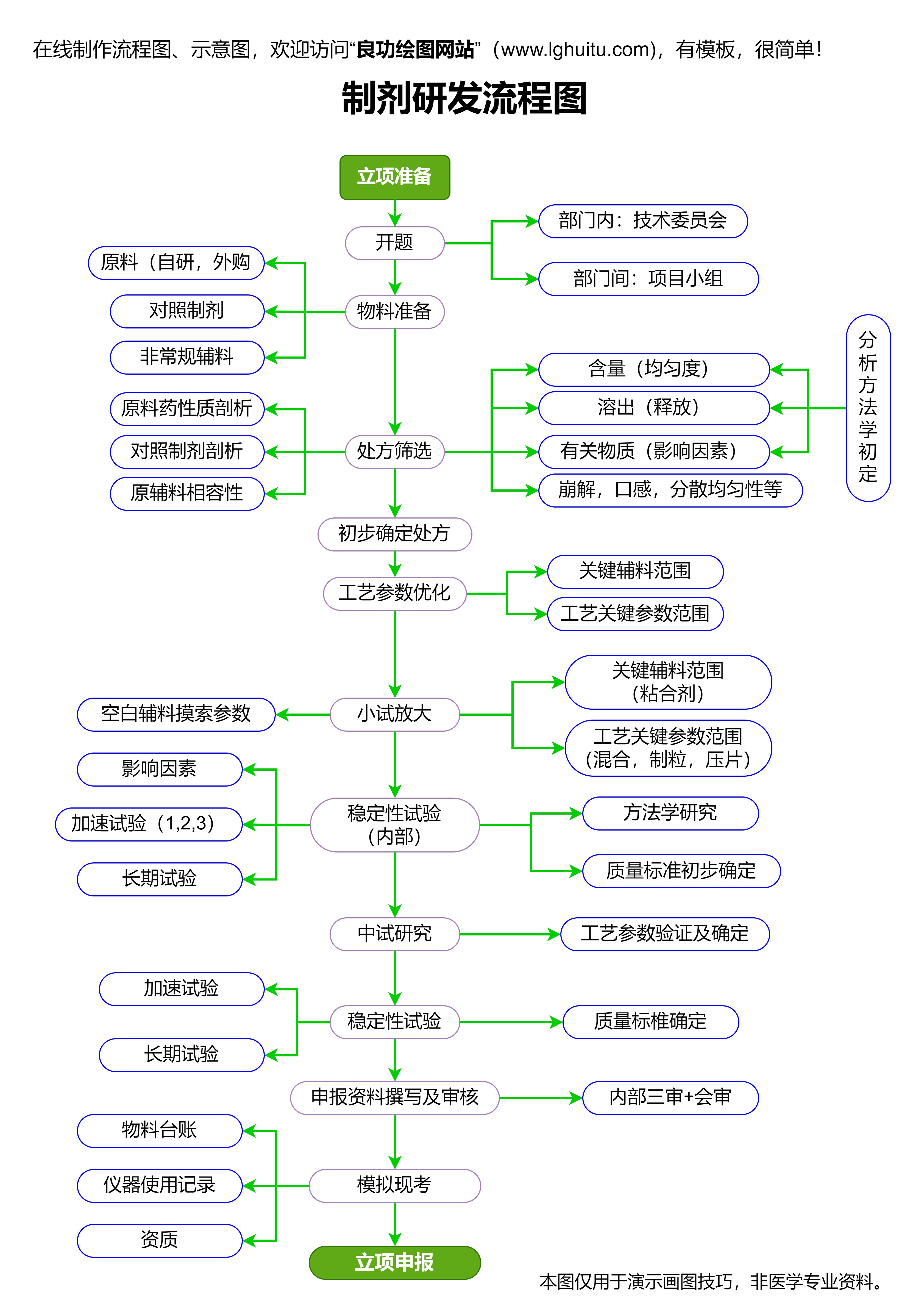
在收到申报材料后,药监局会组织专家进行技术审评。这一环节是审批过程中最为关键的部分,审评专家会对药品的临床数据、生产工艺、稳定性研究等进行全面评估,确保药品的安全性和有效性。
如果技术审评通过,药监局将派遣相关人员对企业的生产现场进行实地检查。这一环节的目的是验证企业是否具备药品生产所需的条件,包括设施的安全性、生产设备的合规性、操作人员的资质等。只有通过现场验证,企业才能获得生产许可。
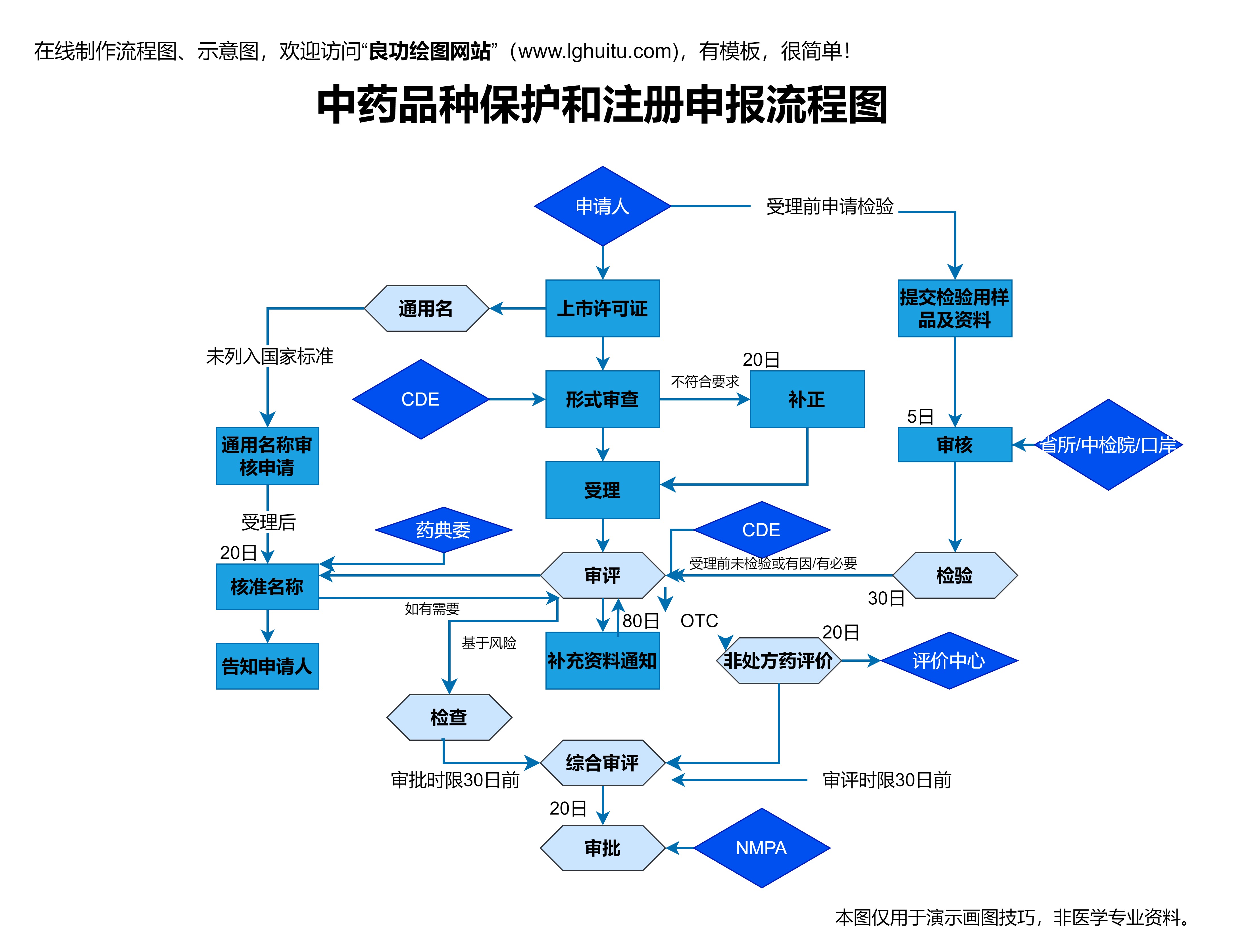
经过以上几个环节的审查,如果一切符合要求,药监局将颁发新药生产批件。这意味着该药品已经获得了正式的生产和销售许可,企业可以按照规定开始大规模生产,并将药品推向市场。
尽管新药生产的申报审批程序已经相对成熟,但在实际操作过程中,企业仍然会遇到各种挑战。审批材料的准备需要大量的人力和物力,特别是在新药临床试验和稳定性研究方面,企业需要投入大量资源进行验证。药监局对申报材料的审核标准严格,任何一个细节上的疏漏都可能导致审批过程的延误或失败。
现场检查环节也是企业的一大挑战。很多企业在实际生产中可能存在某些不符合标准的操作流程或者设施,这就要求企业在申报前要对生产环境进行全面的自查和整改,确保符合规定。
在新药申报审批过程中,制药企业往往会遇到一些具体的问题和挑战。了解这些问题并制定相应的应对策略,能够大大提高申报的成功率。
申报材料的完整性和准确性是审批能否顺利通过的关键。一些企业在提交材料时,往往存在资料不全或者数据不规范的情况,这将直接影响审批进程。为避免这种情况,企业需要在申报前充分准备,确保每一项资料都符合药监局的要求。
应对策略:企业可以通过聘请专业的药品注册咨询公司来协助准备申报材料,确保材料的合规性和完整性。提前与药监局沟通,了解具体的审批要求,并对照清单逐项核实。
新药的临床试验数据是审批过程中最为重要的依据之一。如果临床试验数据不足或者未按规定进行,审批可能会被拒绝。因此,企业必须确保临床试验数据的充足,并且试验设计符合国家药品注册的相关要求。
应对策略:在临床试验阶段,企业应聘请经验丰富的临床研究专家进行指导,确保数据的科学性和严谨性。提前做好多中心、多阶段的临床试验,以便提供足够的安全性和有效性数据。
生产设施的合规性是药品生产申报中的重要环节。如果企业的生产设施不符合标准,现场检查很可能未能通过。为避免这种情况,企业必须投入足够的资金进行生产线的建设和设施的升级改造。
应对策略:企业应该严格按照药监局的标准进行生产设施的建设,特别是无菌生产环境、设备的维护和生产操作的规范化管理。定期进行内部审查和自我评估,确保符合药品生产的各项要求。
新药生产审批通常需要较长时间,有时甚至可能因审查过程中的延误而导致市场机会的错失。为了缩短审批时间,企业需要提前做好各项准备,并在申报过程中及时跟踪进展。
应对策略:企业应与药监局保持良好的沟通,了解申报审批的最新进度,并及时提供额外的补充材料。在申请过程中,定期检查文件是否齐全,确保审批的高效进行。
新药生产申报审批程序是制药企业进入市场的必经之路,它不仅影响企业的市场拓展,也关乎药品的质量和消费者的健康安全。制药企业只有深入了解这一流程,并在实践中不断优化自身的申报策略,才能确保顺利通过审批,实现药品的市场化。

随着全球制药行业的不断发展,越来越多的新技术和新理念被应用到新药的研发与生产中,药品审批的标准和程序也在不断完善。未来,企业应加强与监管部门的合作,提升自身的申报能力,不断提高新药上市的成功率。在这一过程中,透明化、高效化的审批程序将有助于推动行业的整体进步,创造更多造福社会的优秀药品。