新药研发的过程是医学科学中最为复杂的环节之一。它不仅涉及到科研人员的智慧与勤奋,也需要整合来自各方的资源与技术力量。一个新药从最初的构思到最后的上市,经历的步骤繁多,每一步都充满了不确定性和挑战。这个过程也正是推动现代医学进步、拯救无数生命的源泉。

新药研发的第一步是药物发现。这一阶段的核心任务是通过科学研究发现具有潜力的药物分子,通常是在已知的疾病机制基础上,通过筛选大量的化学物质、天然产物或者生物分子来寻找具有治疗作用的候选药物。在这一阶段,科研人员会应用高通量筛选技术、计算机辅助药物设计等前沿技术,迅速锁定潜在的药物分子。
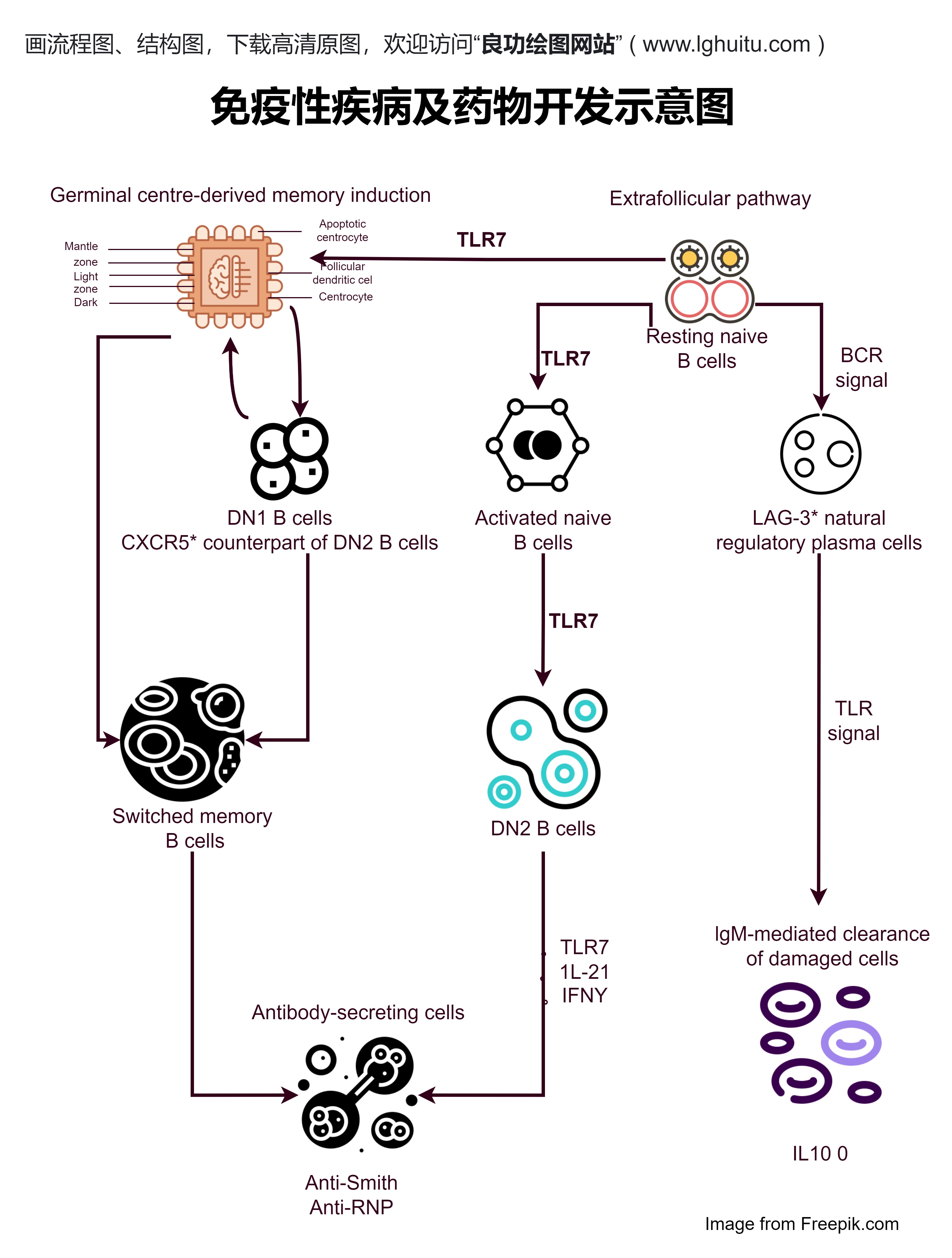
药物发现不仅仅是找到一个“有效”的分子那么简单。科研人员需要对分子的结构、性质、稳定性等多方面进行详细研究,确保它们具备足够的药理活性和选择性。特别是在靶向药物研发中,选择合适的靶点对于药物的效果至关重要。因此,药物发现往往需要涉及到生物学、化学、药理学等多个学科的紧密合作。
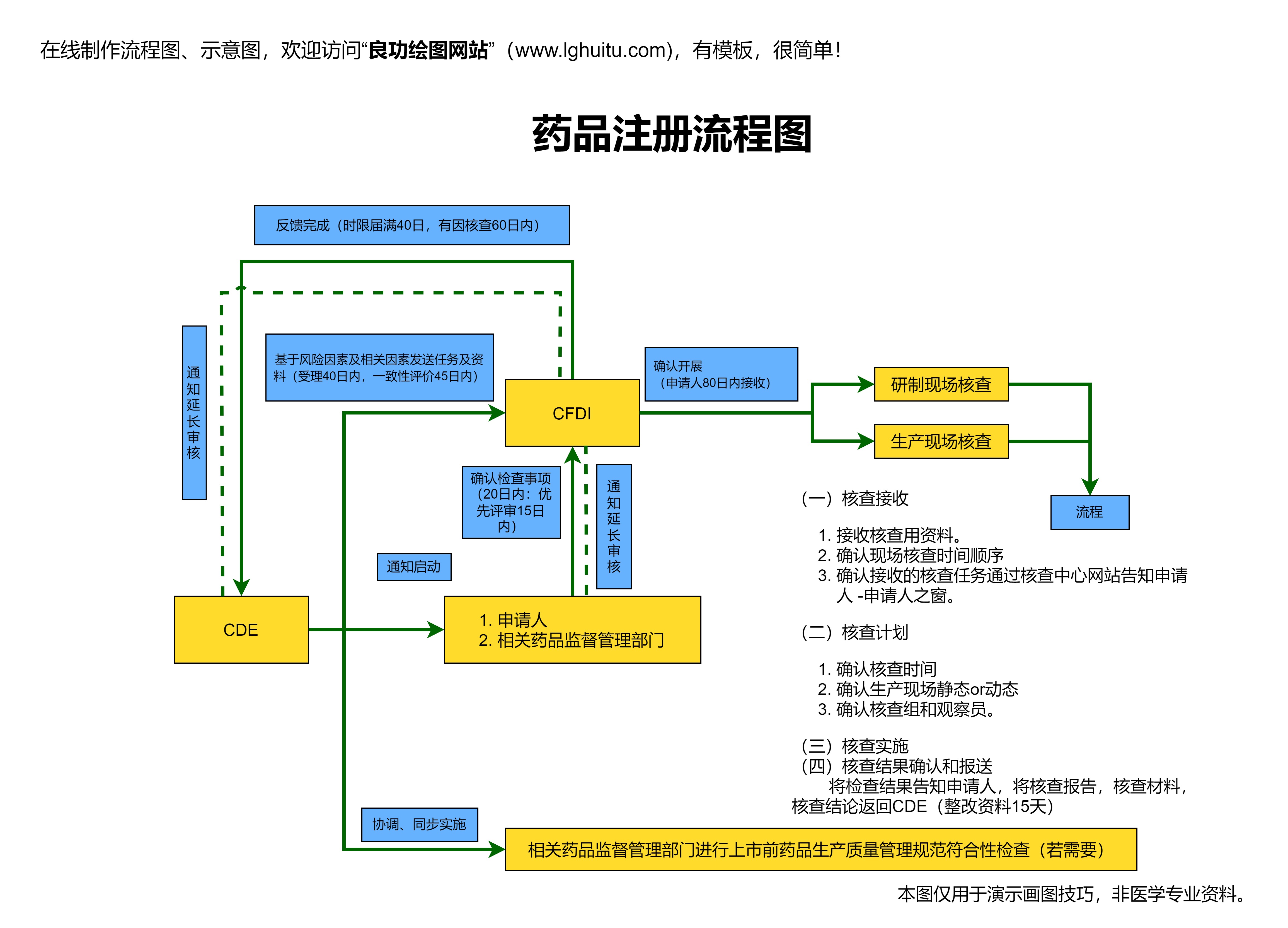
在完成药物发现后,接下来进入的是药物的前临床研究阶段。前临床研究的主要任务是评估药物的安全性、有效性和药代动力学特性。此阶段通常会通过动物实验来模拟药物在人类体内的作用。研究人员会测试药物的毒性、吸收、分布、代谢和排泄等关键参数,以确保药物在临床试验中的安全性。
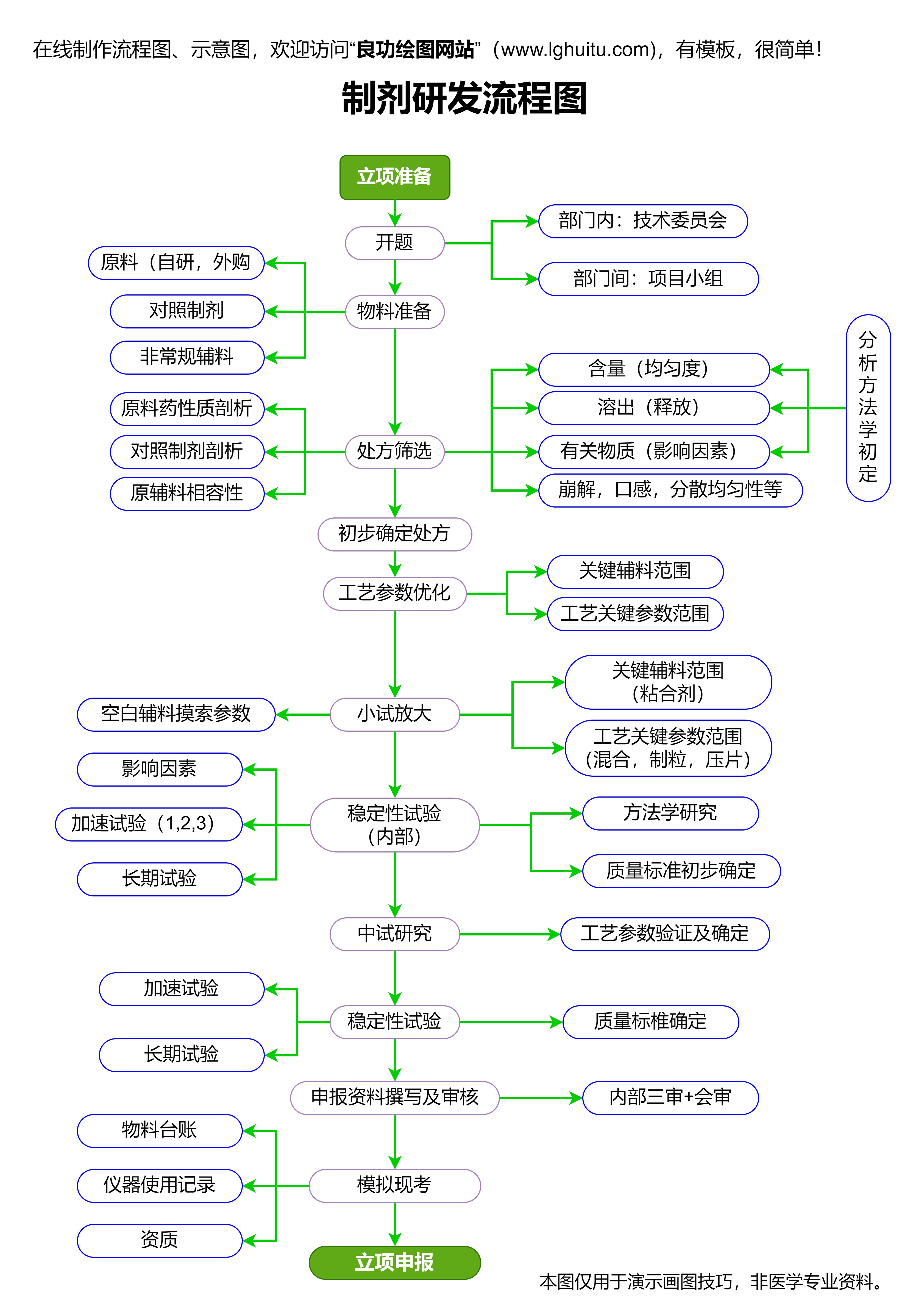
在前临床研究阶段,药物的剂量选择也尤为重要。过高或过低的剂量都可能影响药物的疗效,甚至引发严重的不良反应。因此,确定合适的剂量范围是前临床研究的核心目标之一。
当前临床研究成功并获得了足够的科学数据后,药物便可以进入临床试验阶段。临床试验是新药研发中最为关键的部分,也是对药物进行全面验证的阶段。临床试验通常分为三个阶段:I期、II期和III期,每一个阶段都旨在回答不同的问题。
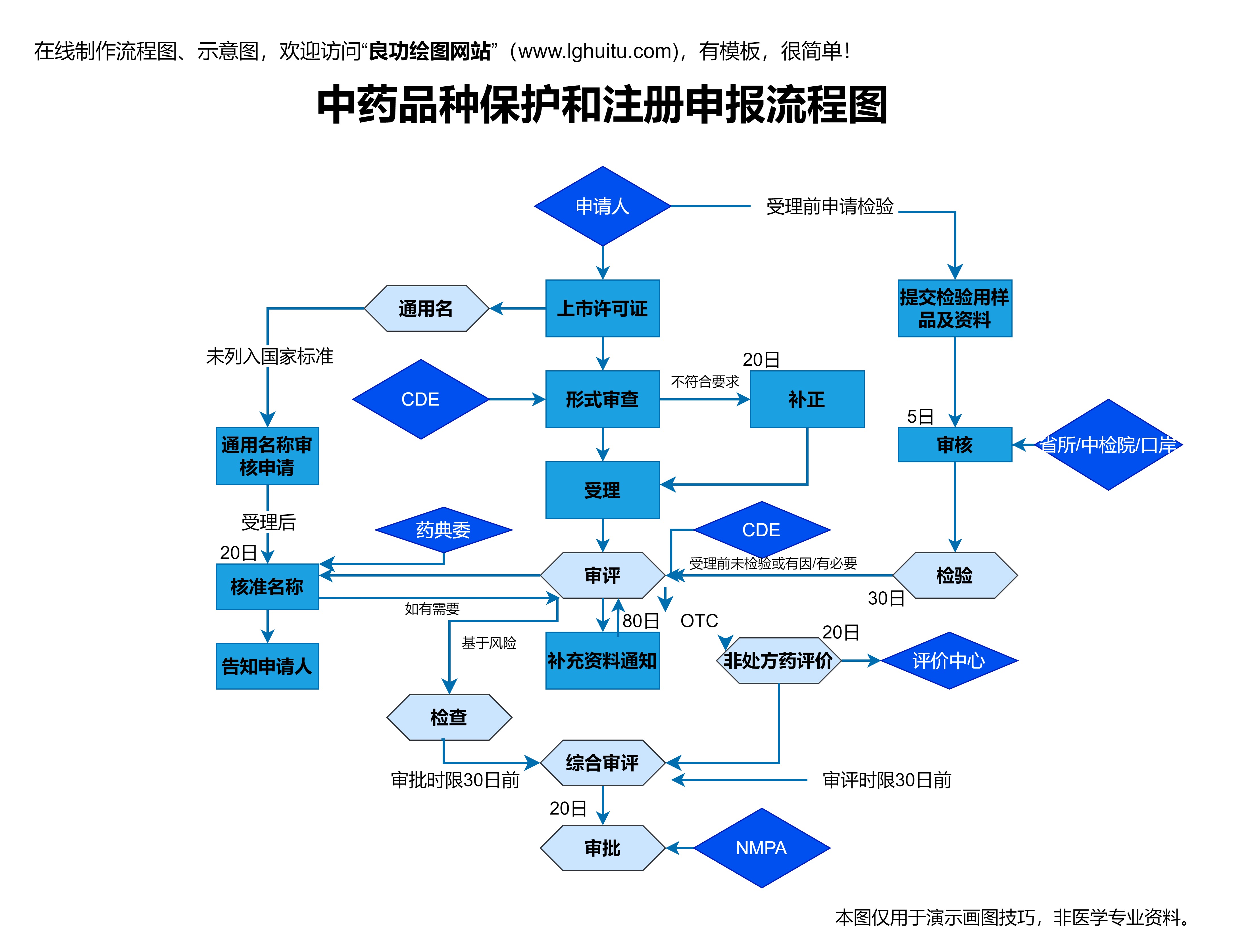
在I期临床试验中,研究的主要目的是评估新药的安全性、耐受性及药代动力学特性。此阶段的试验对象通常是健康志愿者,通过对少数人群的试验,观察药物是否会引起任何不良反应,并确定药物的最大耐受剂量。I期临床试验是新药研发中最为基础也是最为严格的阶段,它为后续的临床试验奠定了基础。
接下来的II期临床试验则聚焦于评估药物的疗效。在II期试验中,药物将被给到特定的患者群体,这些患者通常是患有某种疾病的人。研究人员通过这一阶段来进一步验证药物的有效性和最优剂量,并监测药物在不同患者群体中的反应。II期临床试验也会对药物的副作用和不良反应进行详细记录,确保药物的安全性。
当II期临床试验结果显示药物具有显著疗效且副作用在可控范围内时,新药便会进入III期临床试验。III期临床试验是新药研发过程中最为严格和耗时的一个阶段,它通常需要大规模的患者参与,并涉及多个临床中心进行多国多中心的临床试验。这一阶段的核心目的是在更广泛的患者群体中验证药物的疗效、安全性以及长期的效果和耐受性。III期临床试验的成功为药物上市提供了坚实的数据支持。
通过III期临床试验后,若药物的疗效和安全性都得到充分验证,药品制造商便可以向药品监管部门提交上市申请。经过相关机构如FDA(美国食品药品监督管理局)或EMA(欧洲药品管理局)的审查与批准,药物便可以正式进入市场,进入到广泛使用的阶段。
即使药物上市后,研发过程并未结束。上市后的药物仍然需要进行持续的监控和评估,这就是所谓的IV期临床研究(或称为上市后研究)。此阶段的主要目的是监测药物在长期使用中的不良反应、药效以及可能的药物相互作用。药物上市后的监测和研究,确保了公众的安全使用。
新药研发是一个循序渐进、不断验证的过程。从药物发现到临床应用,每一个环节都至关重要。它不仅需要科研人员的智慧和耐心,更需要全行业的通力合作。随着科技的不断进步和创新方法的应用,未来的新药研发将会更加高效、精准。