近年来,中国医药行业持续创新,不断推动着全球医药领域的进步。随着国家对医药行业的政策调整和完善,药品的研发、注册、审批流程变得更加高效,行业发展空间逐步扩大。2020年,中国出台了新版《药品注册管理办法》,并推出了其电子版,成为了促进医药产业腾飞的关键文件之一。对于制药企业而言,这一政策意味着不仅注册程序更加简化,审批效率也大幅提高,同时还能够在更短时间内进入市场,拓展国内外的市场份额。
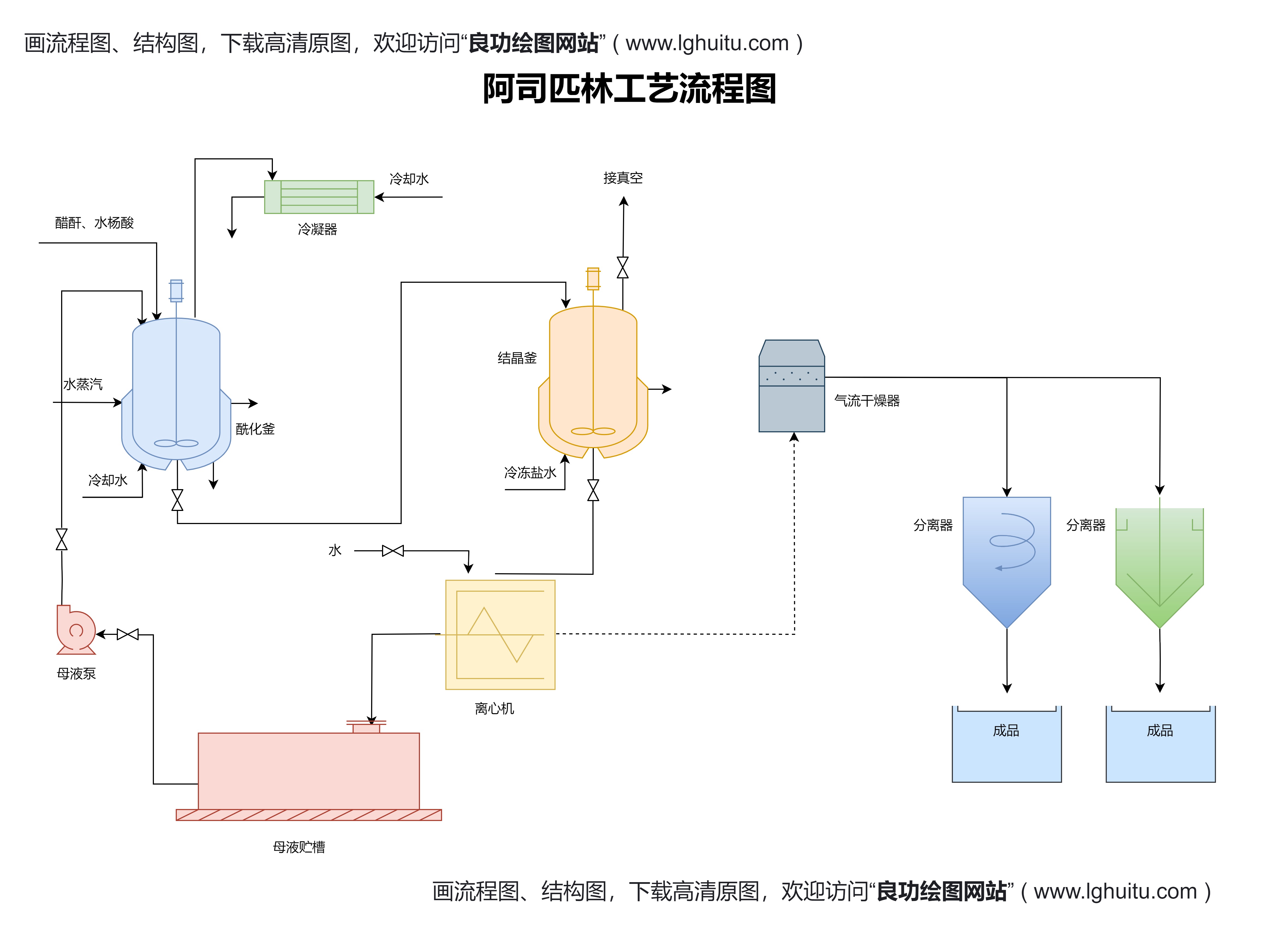
《药品注册管理办法2020》电子版对药品注册制度进行了大规模改革。在药品注册的审批流程上,电子版的推出让企业可以随时随地获取最新的政策信息与相关审批进度,极大提高了注册效率。这一举措不仅简化了企业的工作流程,也使得信息传递更加透明。企业能够实时掌握药品注册的各项进展,及时解决遇到的困难,减少了由于信息滞后造成的沟通成本和时间成本。
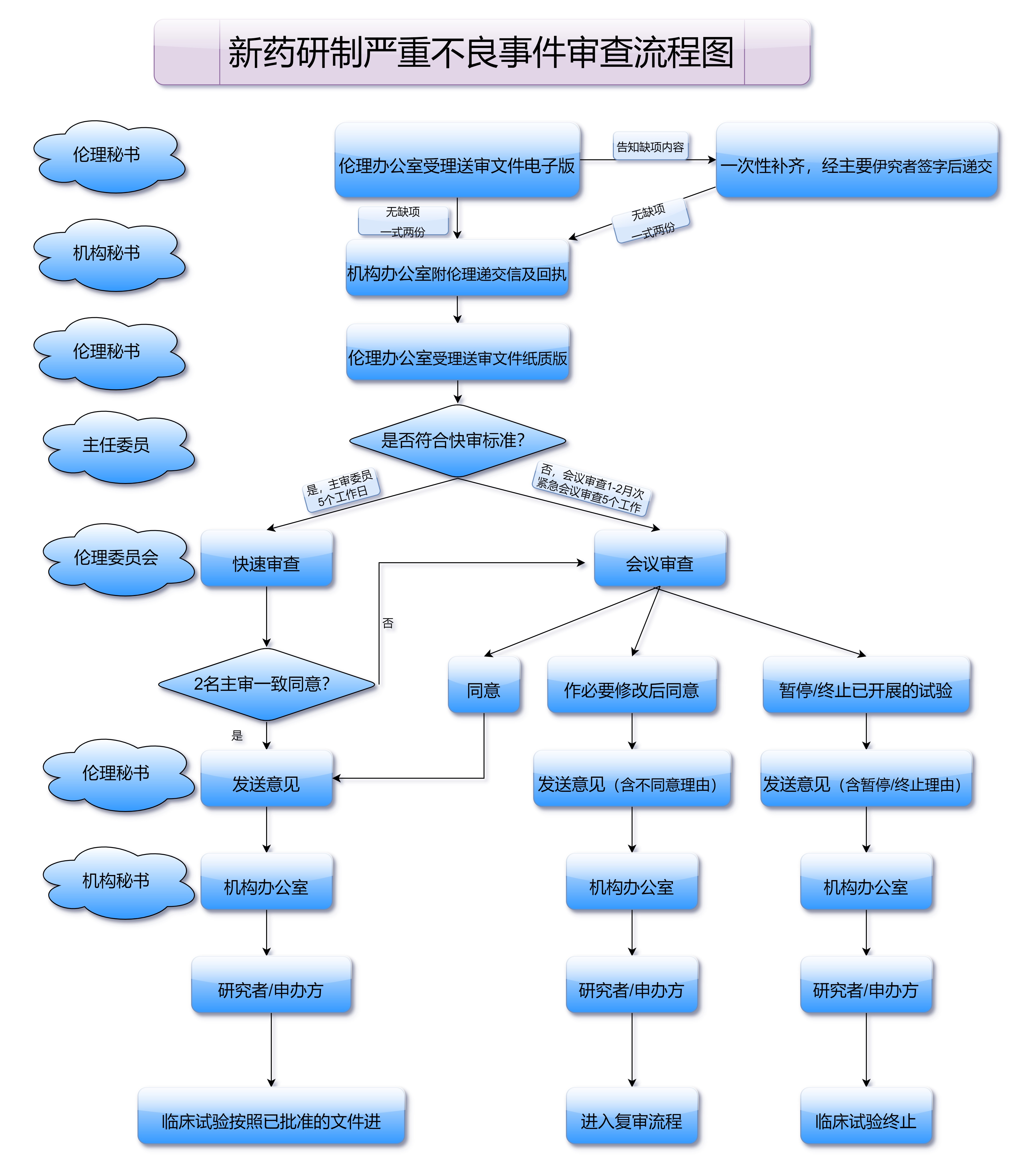
新版管理办法特别注重了药品研发与审批的并行性。在过去,药品研发和注册审批常常是割裂的,企业往往在研发的同时无法明确了解审批的要求,造成不必要的浪费。而新的管理办法强调了研发与审批流程的同步进行,使得企业能够在研发过程中更加明确注册要求,从而提高研发的精准性与针对性。这一创新性改革不仅为药品注册开辟了新的路径,也让医药企业可以更快地将创新药品推向市场,为患者带来更好的治疗选择。

值得一提的是,电子版的《药品注册管理办法2020》不仅加强了国内市场的监管,还着眼于国际化发展。随着中国医药产业的迅速崛起,越来越多的企业希望能够将产品推向全球市场。新版管理办法针对药品的境外注册与国际认证做出了相应规定,帮助中国药品走向世界。这一政策的出台,不仅提升了中国医药品牌的国际竞争力,也促进了全球药品流通的更加公平与高效。
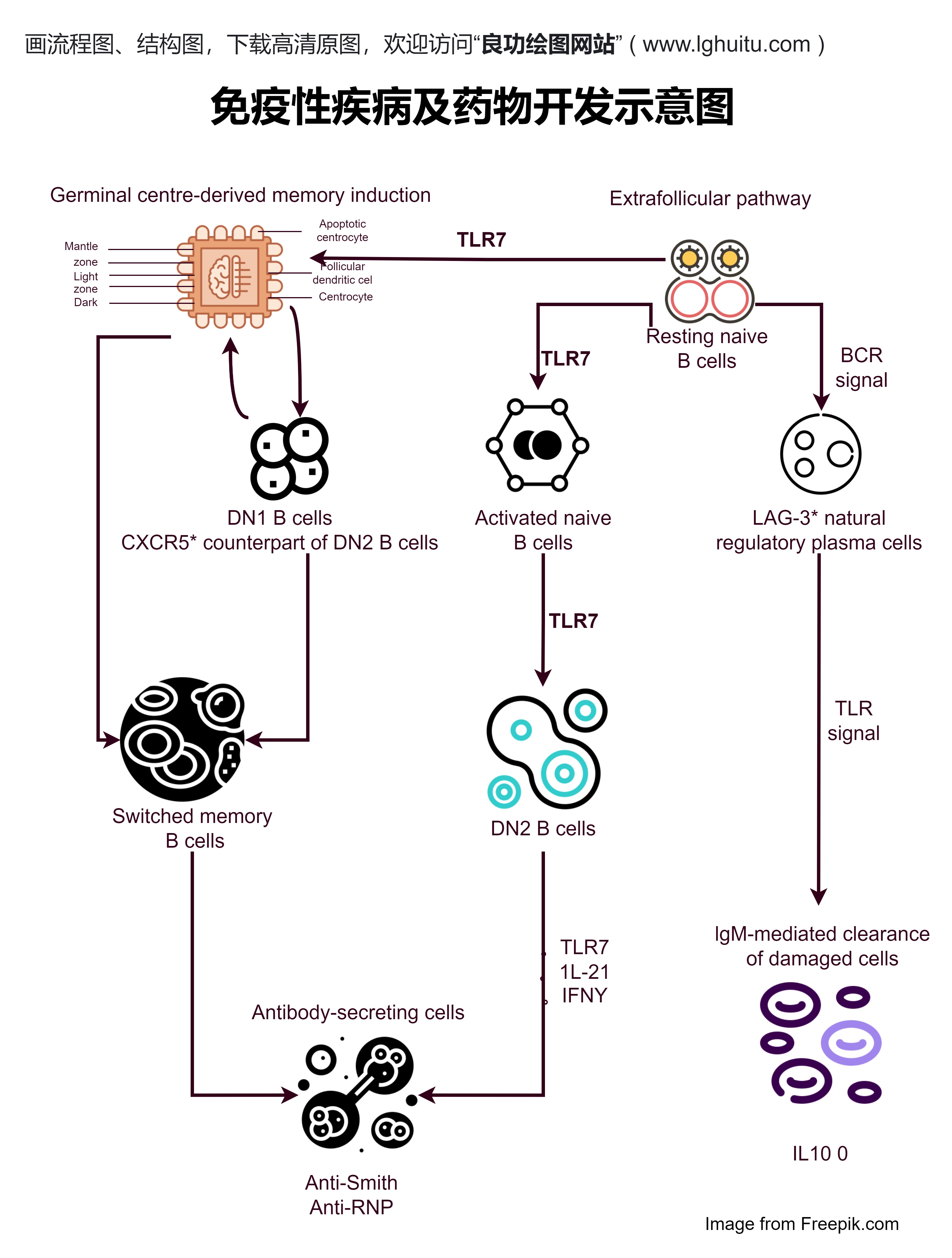
新办法的另一大亮点是它在推动创新药物审批方面的巨大改革。过去,创新药物的审批往往需要经历漫长的等待时间,制药公司在这期间付出的成本和精力可想而知。而新版办法明确表示将对于创新药物审批给予优先审查,通过加速审批机制帮助创新药物更快进入市场。这一政策的实施,不仅为制药企业带来了更多的机会,也让患者能够更早受益于全球前沿的治疗方法。
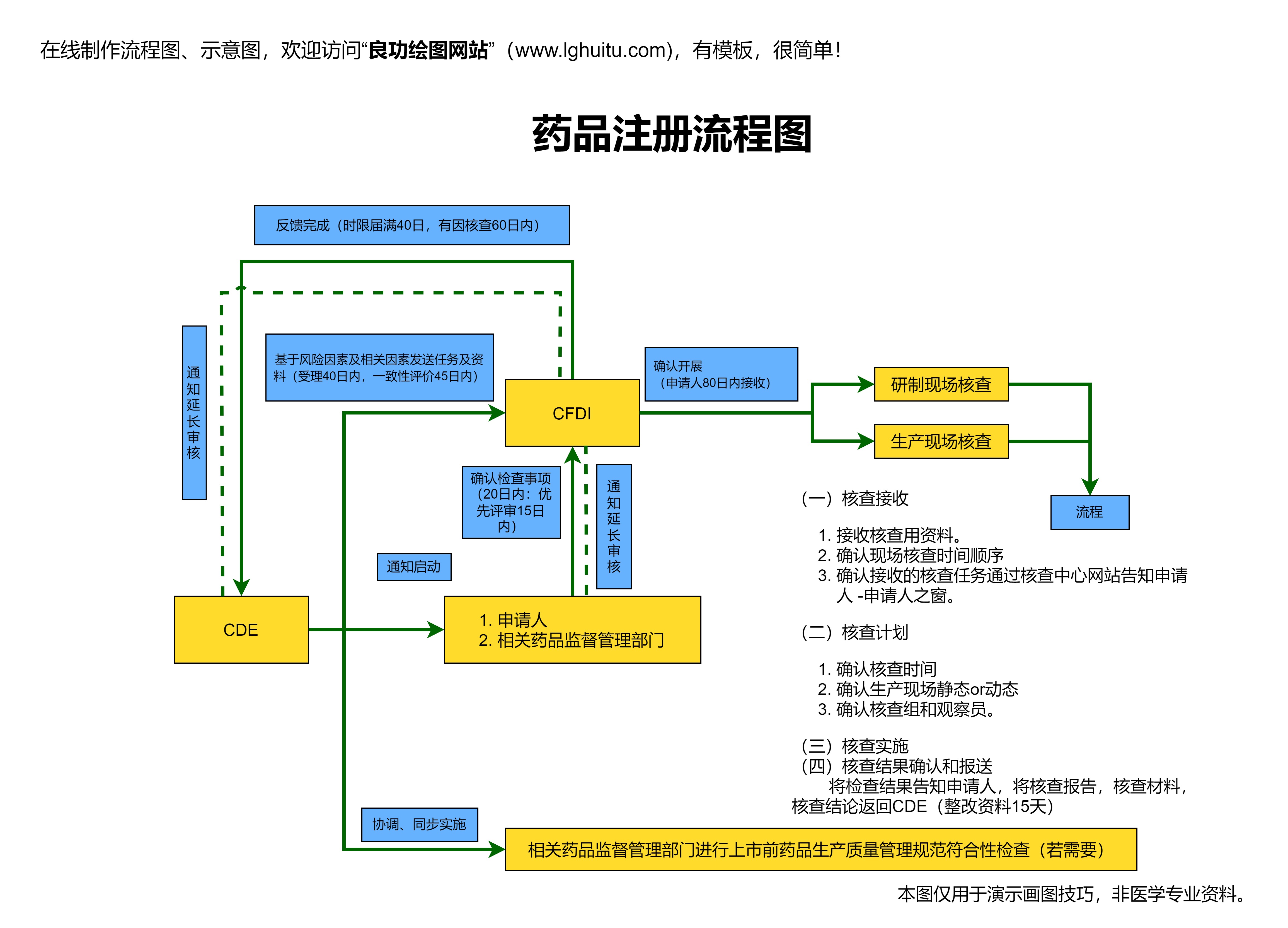
《药品注册管理办法2020》电子版的出台,对于药品注册企业来说,意义非凡。政策的全面改革使得药品注册流程更加清晰、简化,审批时间缩短,企业的负担得到有效减轻。这一办法还增加了药品质量的管理要求,强化了对药品生产全过程的监管,确保了药品的安全性和有效性。企业不仅要满足注册时的相关要求,还要在上市后继续进行药品的跟踪监测,以确保药品的质量始终符合标准。
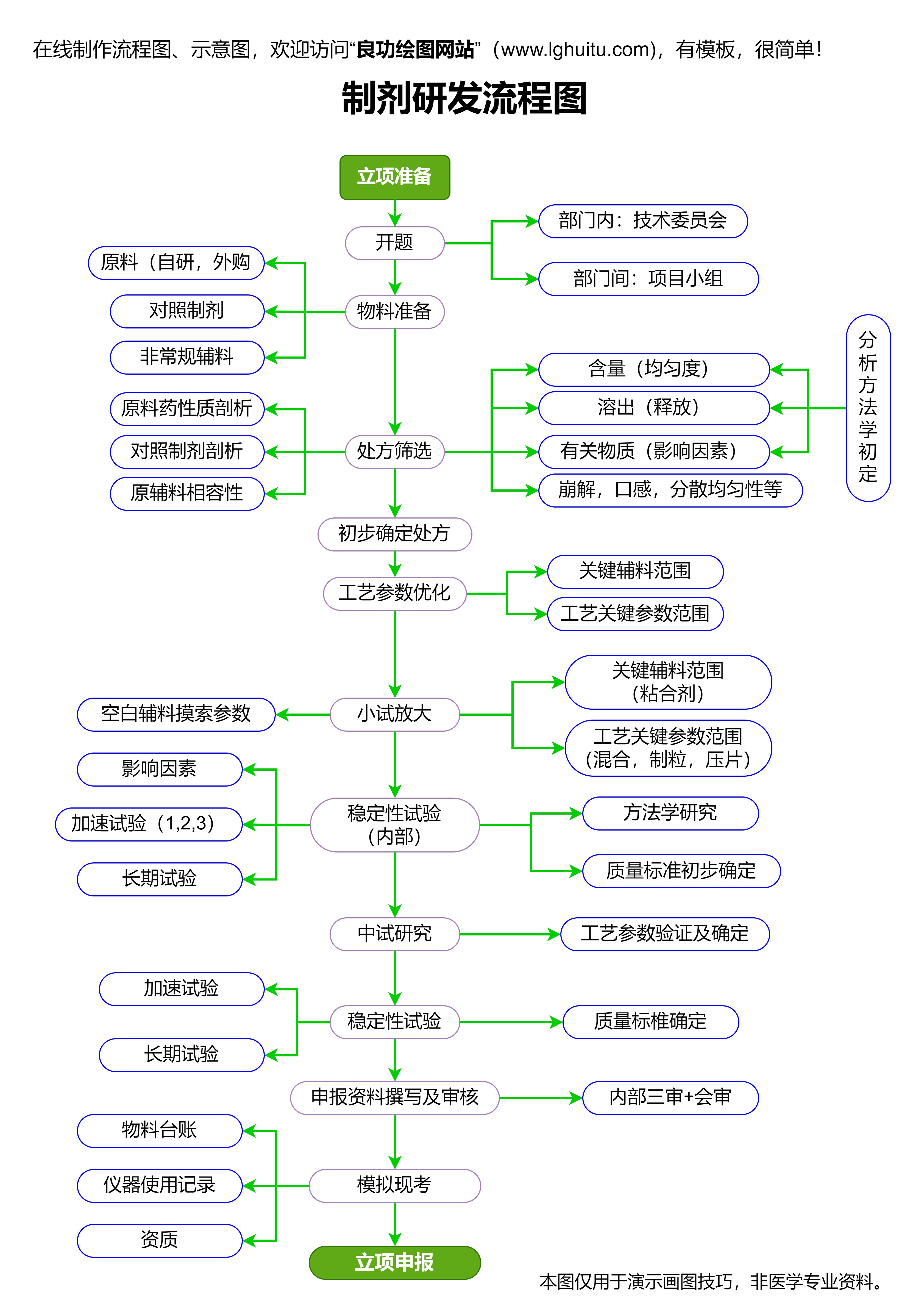
对于研发机构来说,2020年新版药品注册管理办法提供了更多的支持与保障。办法对于新药的研发路径进行了明确的指导,并且加强了与科研机构的合作。这意味着,研发人员能够更清晰地了解从研发到上市的全流程要求,提高研发效率和研发水平。而且,办法明确了药品研发中对于试验数据的要求,保障了药品的临床试验结果和实际效果,确保每一款药品都能够在科学、合规的基础上推向市场,造福患者。
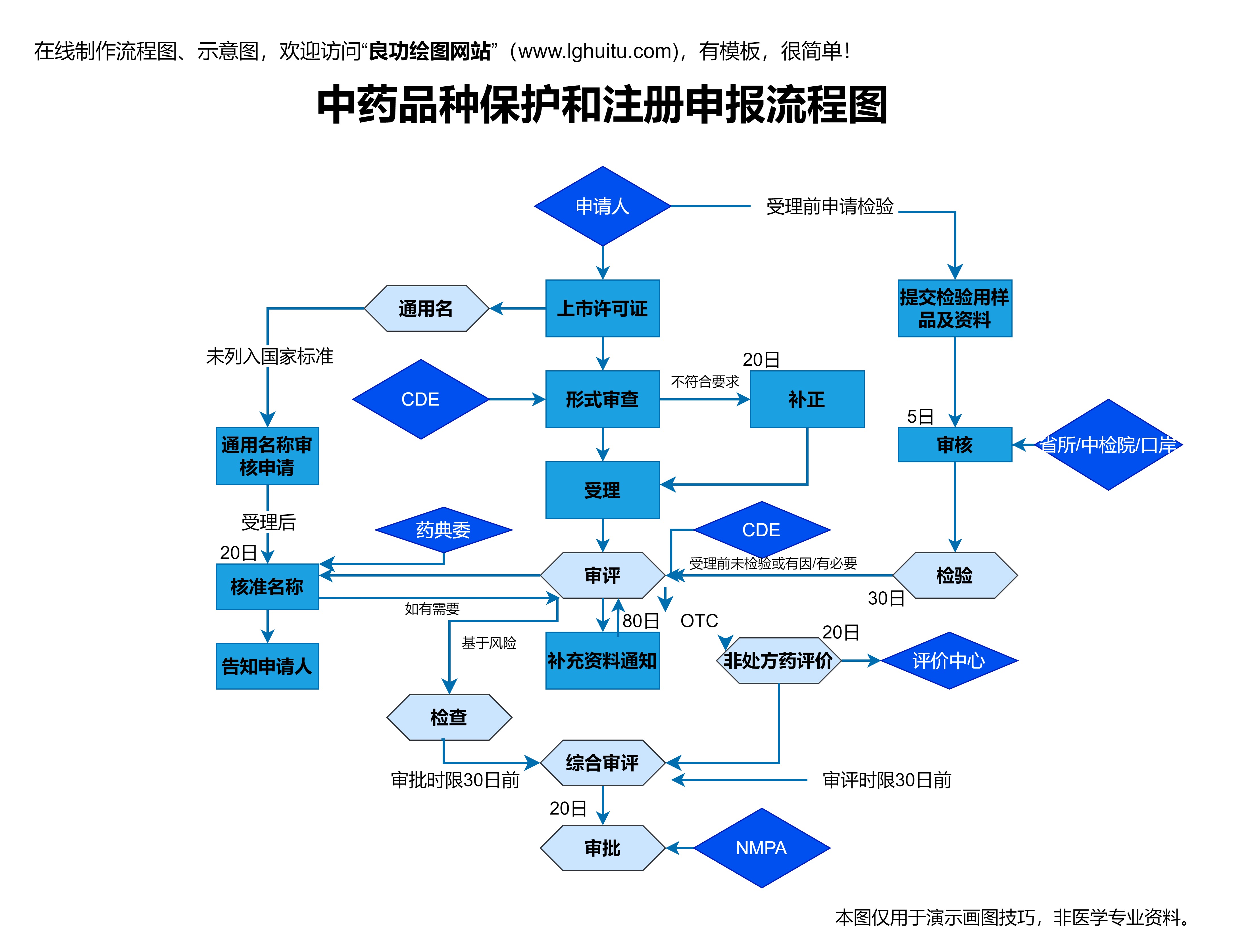
值得关注的是,办法的推行并非仅限于简化审批流程,还涉及到药品的质量控制与监管。随着技术的不断进步,药品的生产工艺逐渐趋向高精度与高效能。新办法在这一背景下,特别重视对药品生产过程的监管,推动生产设备和工艺的现代化升级,确保药品生产环节不出现疏漏,最终保证药品的质量与安全。
对于药品企业而言,这也意味着新办法对于整个行业的结构性调整提出了更高的要求。企业需要更加注重内部管理和技术创新,推动企业的升级和转型。随着国内外市场竞争的加剧,企业不仅要具备足够的科研和生产能力,还要善于利用新政策中的机会,提升自身的市场竞争力。
药品注册管理办法2020电子版的推出,也对药品的广告宣传提出了严格的要求。新的规定强调,药品广告必须严格遵守国家药监局的相关法规,不得虚假宣传或夸大药品效果。这一措施旨在保障消费者的知情权,防止不良商家通过虚假广告误导消费者,确保药品市场的公正性与透明度。
总结而言,《药品注册管理办法2020》电子版的推出,是中国药品管理领域的一项重大战略部署。它不仅帮助医药企业提升了注册效率和审批速度,还在加强药品质量控制、推动创新药物的快速上市等方面发挥了积极作用。政策对于药品广告和市场监管的严格要求,也有助于维护行业的健康发展。未来,随着政策的进一步落实与优化,医药行业将迎来更加广阔的发展机遇,企业也能够借此政策春风,向更高的目标迈进。