药品注册管理办法属于什么?这是许多人在关注药品市场时常常提出的问题。作为一项涉及公众健康和安全的法规,药品注册管理办法不仅规范了药品的研发、生产和销售流程,还通过确保药品的质量与疗效,有效保障了公众的生命安全。可以说,药品注册管理办法是药品管理体系中的“法律基石”。

药品注册管理办法的核心目标是确保新药及仿制药符合国家的安全、有效和质量要求。具体而言,这一办法对药品注册的程序、标准、要求等方面进行了明确的规定,为药品研发和市场准入提供了法律框架。无论是创新药、仿制药,还是疫苗、诊断试剂等特殊药品,都必须按照相关规定进行注册和审批,才能合法上市。
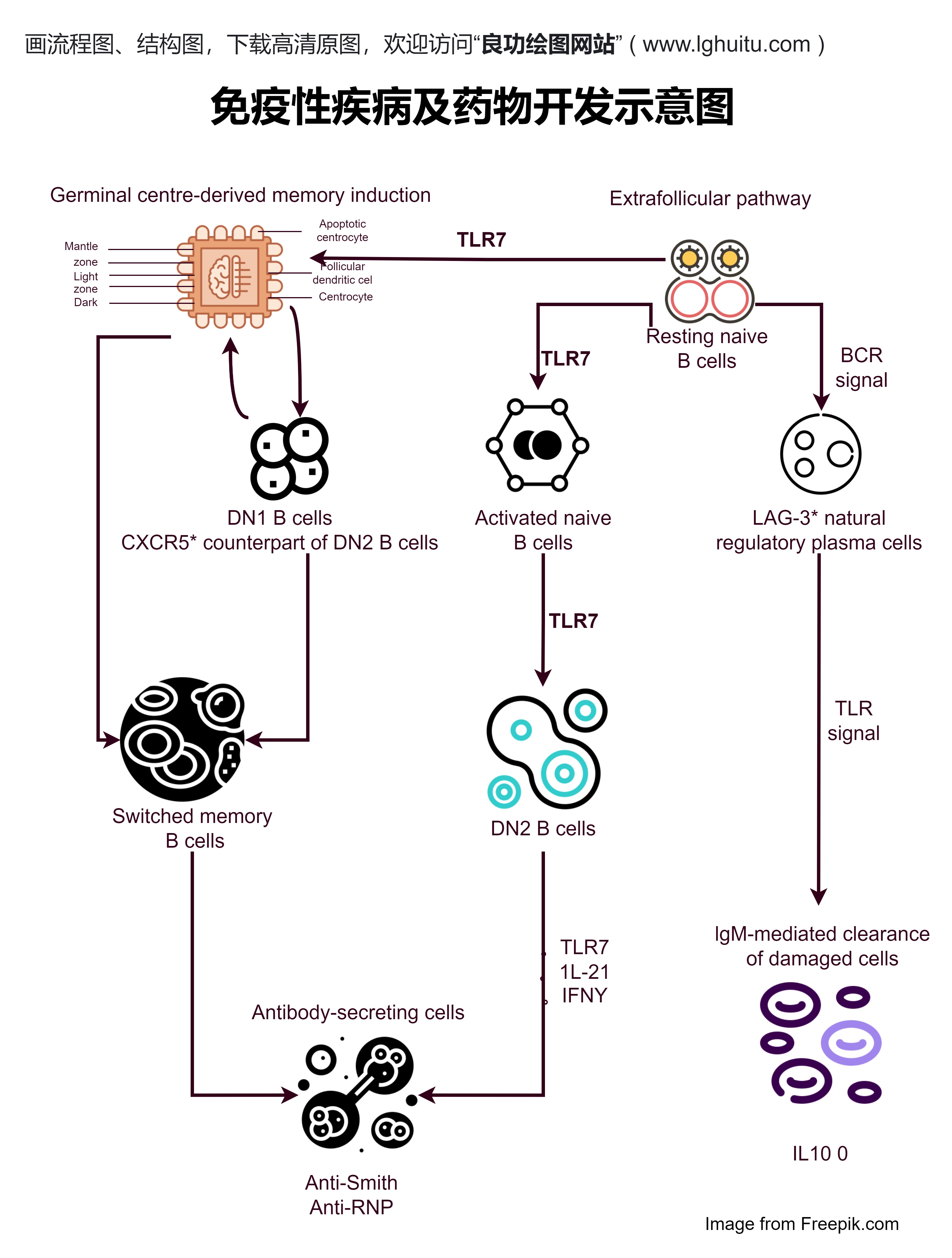
药品注册管理办法设定了严格的药品审批流程。在这一流程中,药品生产企业必须提交详细的药品研究资料、临床试验数据以及生产工艺等信息,证明药品的安全性和有效性。为了保证这些信息的真实性和可靠性,药品监管部门会组织专家进行审核。审核过程中,专家组会根据药品的临床效果、毒理研究数据、生产工艺的合规性等方面进行综合评估,确保每一种药品都符合相关的法律标准。
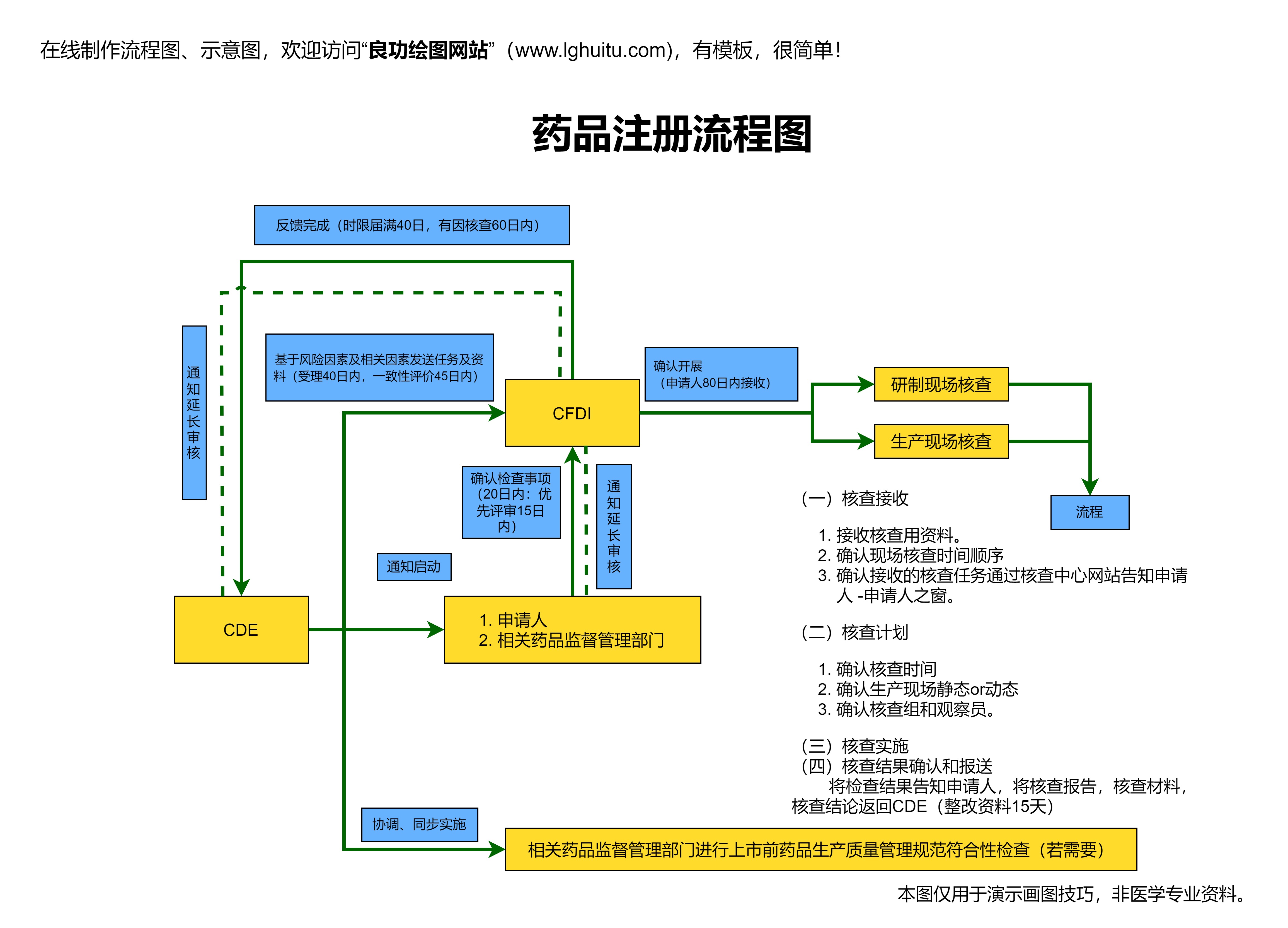
药品注册管理办法也明确规定了不同类别药品的注册要求。对于普通药品,一般要求通过基础的临床试验来证明其有效性与安全性。对于某些特定的药品,如生物制品、疫苗等,由于其特殊性,注册要求会更加严格。生物制品的生产工艺涉及到细胞培养、蛋白质提取等复杂过程,必须在严格的质量控制下进行。而疫苗则需要进行更加严密的临床试验,确保在不同人群中的免疫效果与安全性。
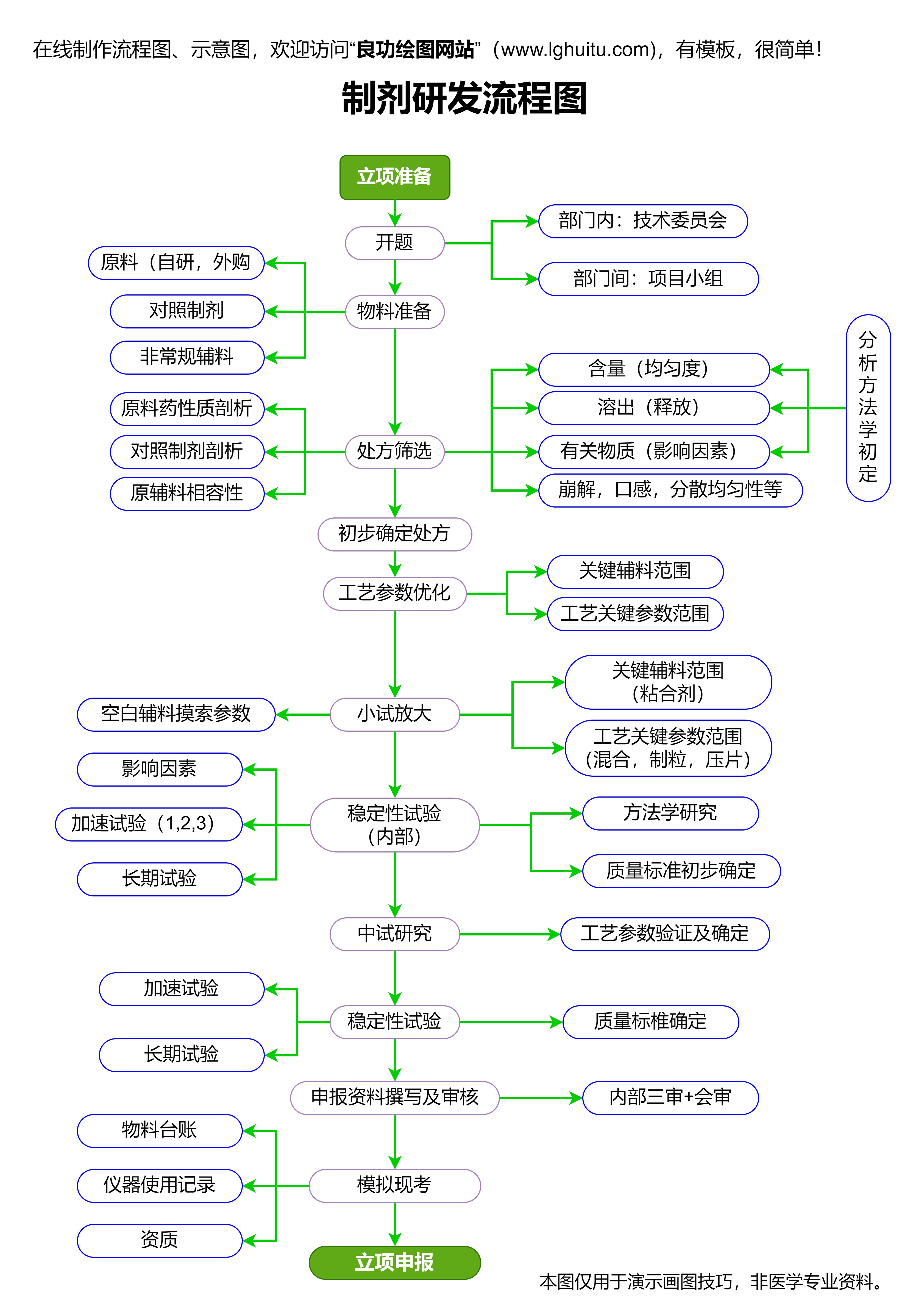
在此基础上,药品注册管理办法还对药品的注册时限做出了规定,要求药品审批过程必须在一定期限内完成。这一规定旨在缩短药品从研发到上市的时间,让广大患者能够尽早受益于新药的治疗效果。与此这一办法也加强了对药品质量的全程监控,确保从研发、生产到销售的每个环节都符合法律规定,杜绝任何潜在的安全隐患。
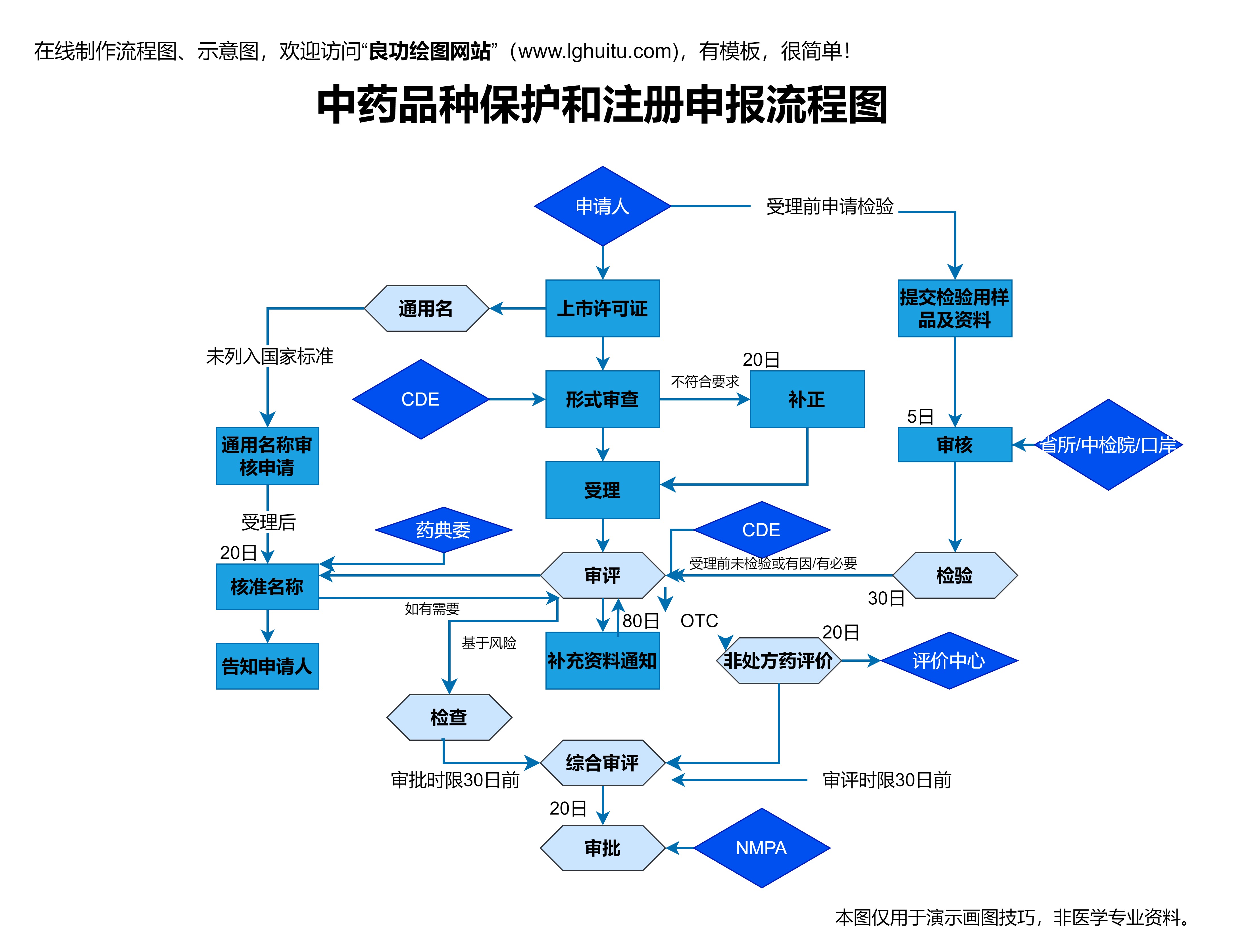
药品注册管理办法的实施,不仅对于国内药品生产企业提出了更高的要求,也为国际药品进入中国市场提供了清晰的指南。在全球化的今天,跨国药品企业必须了解并遵循中国的药品注册要求,才能在中国市场顺利开展业务。因此,药品注册管理办法也起到了促进国际合作、加强全球药品交流的作用。
药品注册管理办法的进一步完善和实施,不仅仅是法律层面的进步,它对整个药品行业的发展也具有深远的影响。随着药品注册管理办法的不断优化,药品的研发速度、市场准入的效率以及药品监管的严格程度都得到了显著提升。尤其在近年来,国家对药品注册制度的改革不断深入,力求通过更加科学、合理的管理方式来提高药品市场的透明度和公正性。
其中,药品注册管理办法在推动药品创新方面起到了重要作用。随着科技的不断进步,新药研发逐渐成为药品行业发展的重要方向。而药品注册管理办法则为新药的研发和注册提供了有力保障。通过简化部分注册流程和优化审批程序,国家鼓励更多创新药物的研发,特别是在抗癌药物、抗病毒药物等关键领域的突破。与此国家还通过设立药品注册绿色通道,支持创新药品尽早进入临床阶段,尽早为患者提供更好的治疗选择。
对于仿制药的管理,药品注册管理办法也提出了明确要求。在过去,仿制药往往因为缺乏创新而受到一定的偏见。随着国内药品市场的需求日益增加,仿制药逐渐成为了补充市场空缺和满足患者需求的重要选择。药品注册管理办法通过明确要求仿制药必须满足与原研药相同的质量和疗效标准,使得仿制药的市场地位逐步提升,并且推动了药品价格的合理化。
与此药品注册管理办法的实施对于保障患者安全、提升药品质量具有重要意义。通过严格的药品注册制度,国家能够有效控制药品的质量风险,从源头上杜绝了低质量药品的进入市场。这不仅减少了药品安全事故的发生,也提高了患者的用药信心。对于患者而言,他们可以更加放心地使用那些经过严格审批的药品,不必担心药品的疗效和安全性问题。
药品注册管理办法不仅是对药品研发、生产和销售的规范化管理,它更是国家保障公众健康的法治举措。在全球化进程加速、药品市场不断扩展的背景下,药品注册管理办法的完善与实施将继续发挥着至关重要的作用。通过这一管理办法,国家不仅确保了药品市场的健康有序发展,还推动了药品行业的技术进步和创新,最终实现了保障人民健康、促进社会发展的战略目标。
药品注册管理办法的深远意义,必将随着时代的发展而不断展现出新的活力,成为中国药品行业迈向国际化、创新化的重要基石。