在药品行业中,药品的注册管理是确保药品安全有效的关键环节。作为药品注册管理的一部分,掌握相关政策法规、注册流程及相关管理办法是每一位药品管理人员必备的基础知识。而《药品注册管理办法》则是其中最为重要的一部法规。为了帮助您更好地掌握药品注册相关的内容,本文将为您详细解析《药品注册管理办法》的相关试题及答案,助力您的学习和备考。
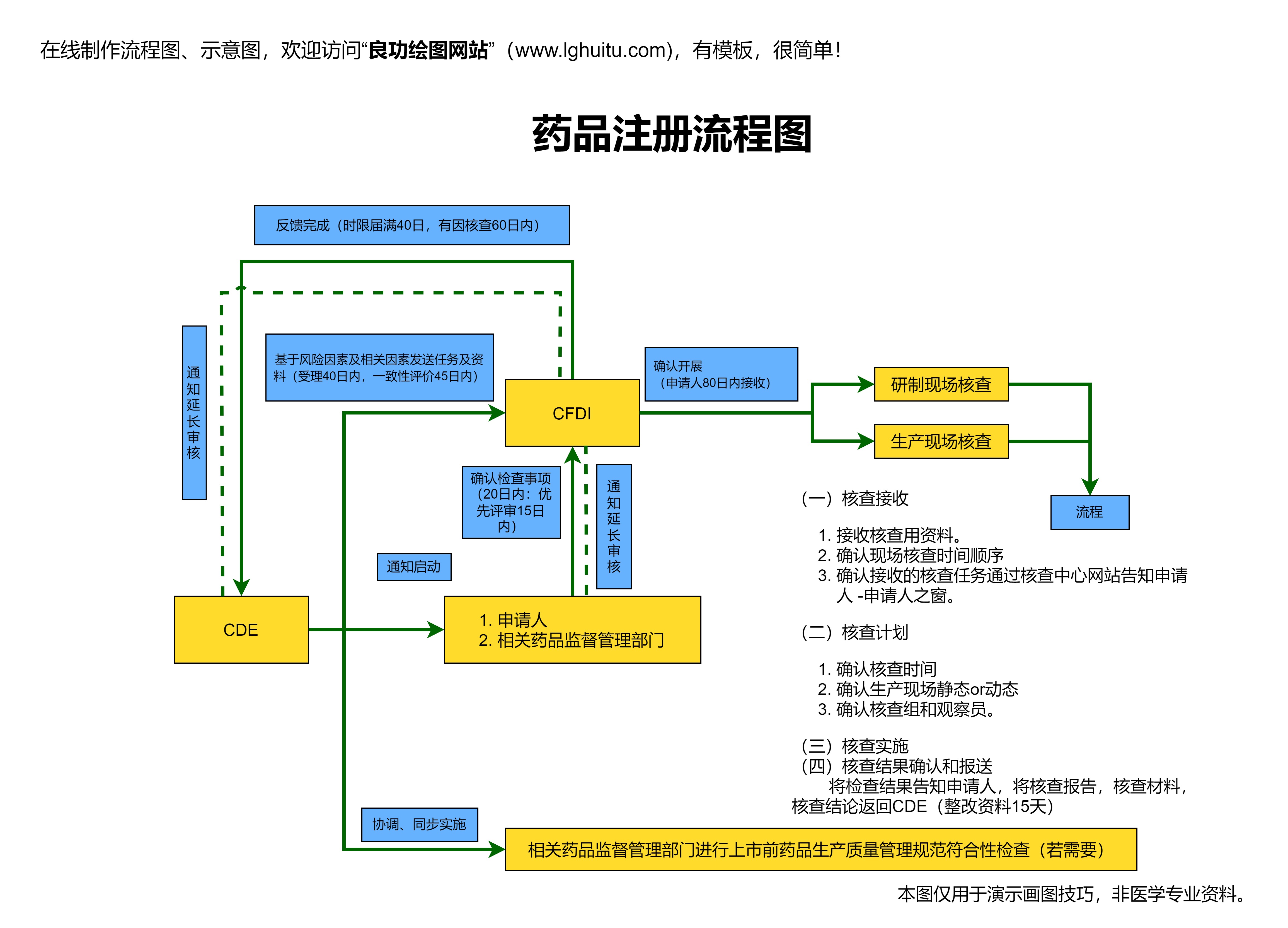
《药品注册管理办法》是由国家药品监督管理局制定的法规,旨在规范药品注册的管理,保障药品的质量、安全与疗效。根据该办法的要求,药品注册是药品上市销售前的必要步骤,所有药品必须经过注册审批,才可合法生产和流通。
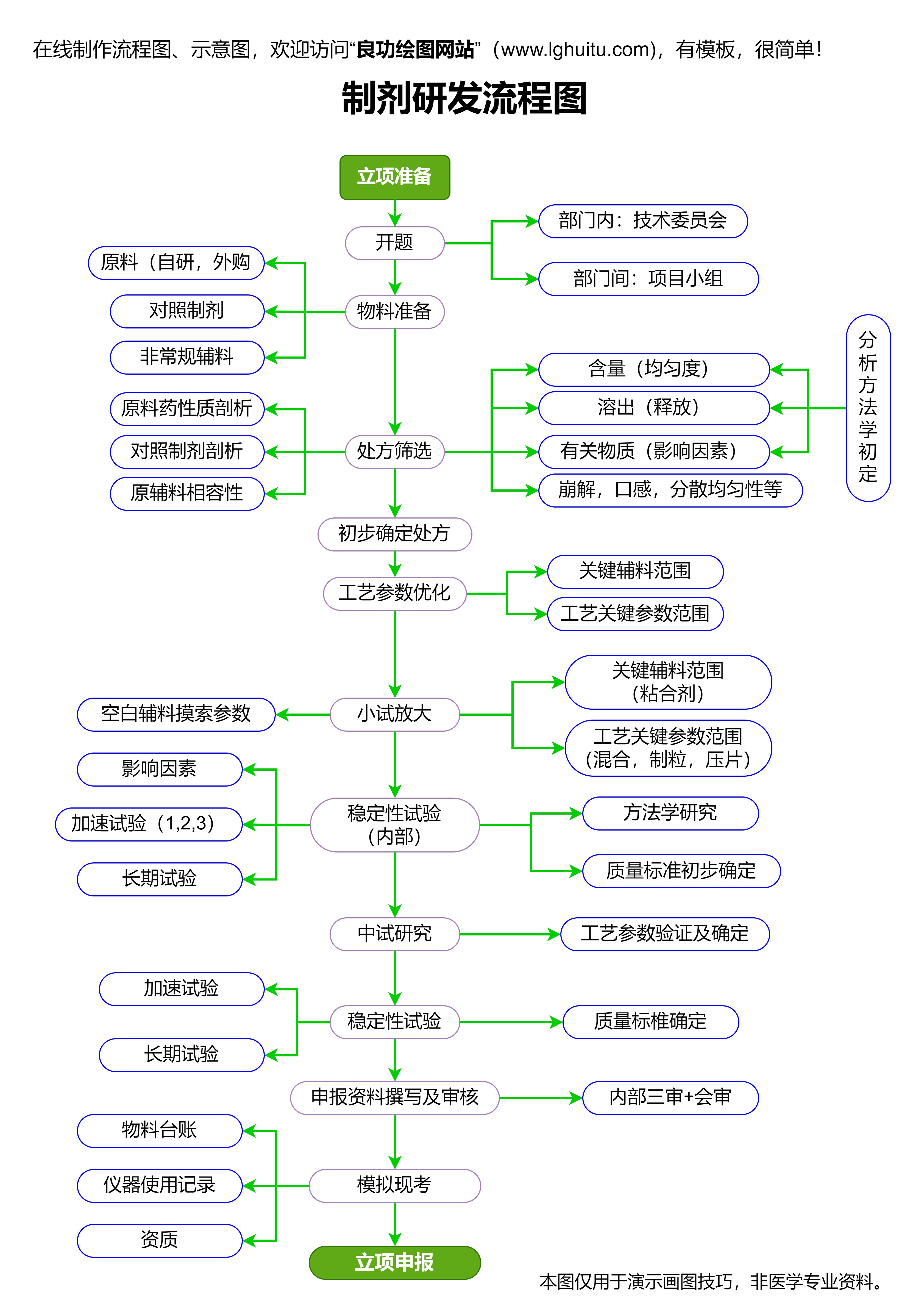
注册工作由药品监督管理部门负责,而药品注册申请则需要提交给相关的药品监督机构。药品注册过程包括药品的临床试验、质量控制、标签设计等一系列环节,涉及多个专业领域,要求申报者具备扎实的专业知识与技能。
在备考《药品注册管理办法》相关考试时,常见的试题类型包括选择题、判断题、简答题以及案例分析题。以下是几道常见的试题类型,帮助您了解考试内容与形式。
试题:根据《药品注册管理办法》,药品的注册审批程序包括哪些主要环节?
答案:A。根据《药品注册管理办法》规定,药品的注册审批程序包括临床试验、药品质量控制和申请资料的审核等环节。每个环节都对药品的质量、安全和疗效提出了严格要求。
试题:药品注册的审批机构只能由国家药品监督管理局来负责。
答案:B。药品注册的审批机构不仅仅由国家药品监督管理局负责,还包括省级药品监督管理局等相关地方机构。在不同的审批环节,可能由不同的管理部门负责。
试题:简述药品注册申请时,药品生产企业应提交的主要资料。
答案:药品生产企业在申请药品注册时,应提交以下主要资料:药品的质量标准、生产工艺、临床试验数据、药品的标签和说明书、稳定性研究报告等。资料齐全并符合要求,是药品注册审批顺利通过的前提。
在实际操作中,药品注册过程不仅复杂,而且涉及的法规、政策多且细致。因此,在备考时,理解每一项规定的背景和实施意义至关重要。为了确保药品注册的合规性,企业不仅要具备相关的专业知识,还要保持对法规的敏感性,确保每一项细节都做到位。
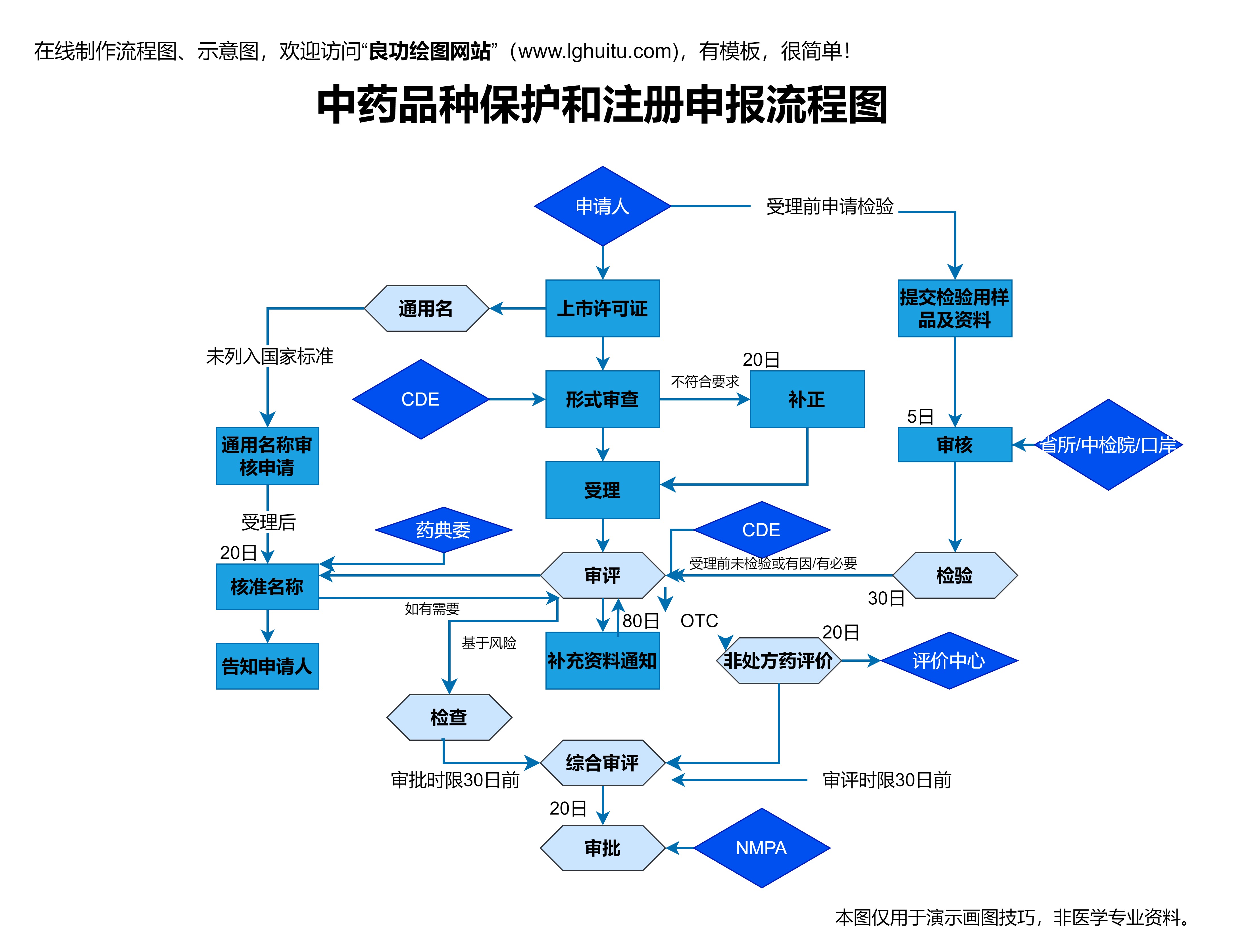
很多考生在备考《药品注册管理办法》时,最常遇到的难点通常是药品注册的审批程序及各类细则。这些内容涉及到药品研发、生产、质量控制等多个环节,需要考生具备较强的理解能力和记忆力。在这一部分的备考中,掌握考试重点,了解每一环节的具体要求,帮助考生更加高效地备考。
在了解了《药品注册管理办法》相关试题的基础上,我们接下来将深入分析该管理办法的关键内容,帮助您更好地掌握考试要点。
药品注册的基本流程包括三个主要环节:申请、审核与批准。
申请:药品生产企业需要向药品监管部门提交药品注册申请,并提供必要的注册资料。这些资料包括药品的生产工艺、质量标准、临床试验数据、稳定性数据等,目的是确保药品的安全性和有效性。
审核:在收到申请后,药品监管部门会对申请资料进行审核,确保其符合国家的药品注册标准。审核过程包括对药品的质量控制、生产环境、临床试验等内容进行全面评估。
批准:通过审核后,药品监管部门会颁发药品注册证书,批准药品上市销售。此时,药品才能正式进入市场流通。
药品注册资料的质量直接影响到药品能否顺利通过审批。根据《药品注册管理办法》,药品注册资料需要满足以下要求:
真实性:所提交的资料必须真实可靠,不得存在虚假或不实的信息。
完整性:资料需要齐全,包括药品的各项技术资料、临床试验报告、药品质量控制标准等。
合法性:所有提交的资料必须符合国家相关法律法规的要求,确保药品注册的合法合规。
在药品注册过程中,临床试验是必不可少的环节。根据《药品注册管理办法》,药品的临床试验必须严格按照国家规定进行,并在经过伦理委员会批准的机构内开展。临床试验的目的主要是评估药品的安全性和有效性,同时确保药品的风险可控。
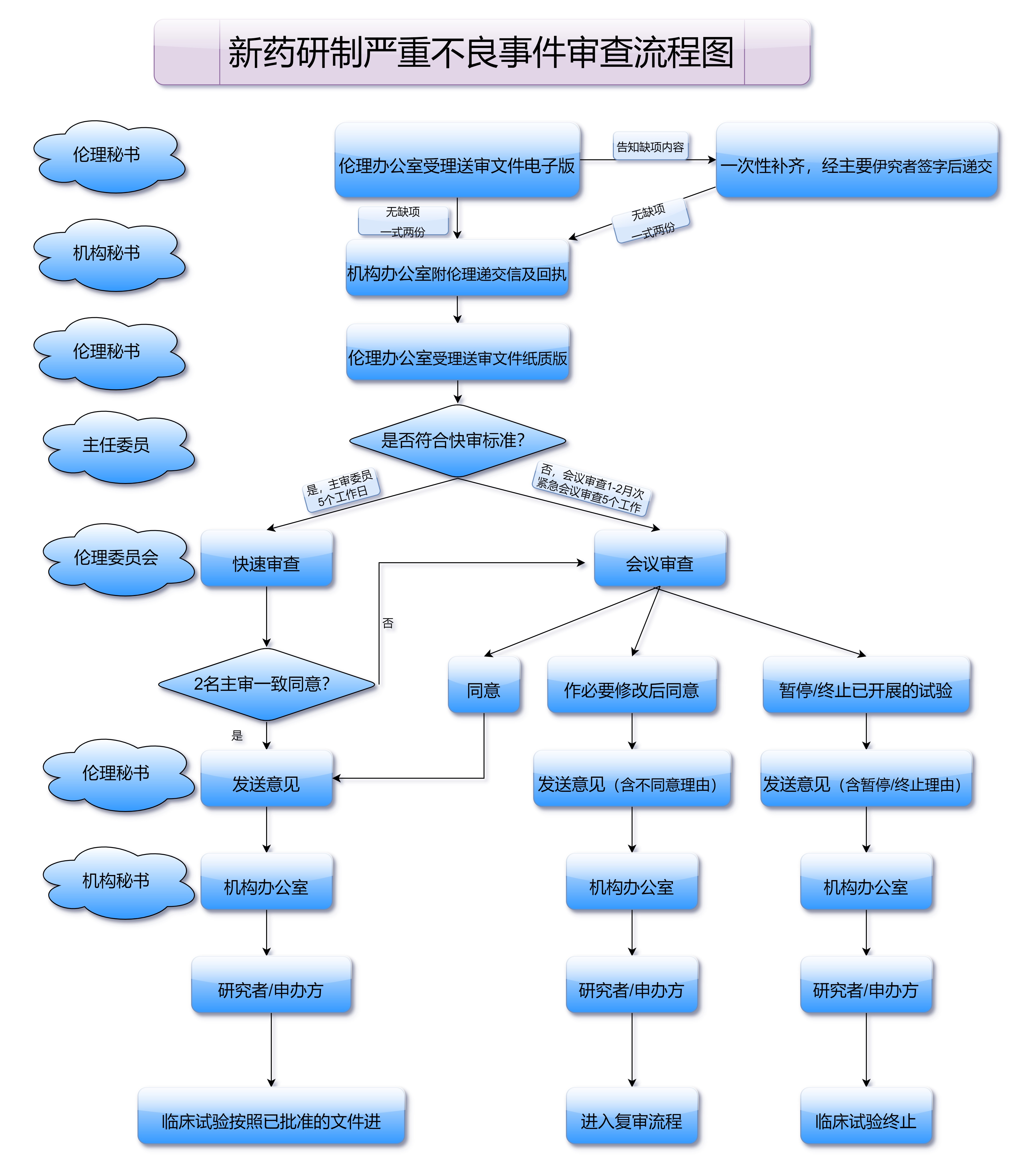
药品注册的审批时限是许多考生关注的一个重点。根据《药品注册管理办法》规定,药品的注册审批必须在规定的时限内完成,确保药品可以及时投入市场。在实际操作中,审批时间可能会受到申请资料的完善程度、审批流程的复杂性等因素的影响,因此企业在提交注册申请时要确保资料的完整性和准确性。

随着国内外医药行业的快速发展,药品注册管理也在不断优化和完善。未来,药品注册管理的重点将不仅仅放在审批环节上,更加注重药品的质量监控和市场监管。尤其是在全球化背景下,药品注册管理将面临更加复杂的国际化挑战。
通过对《药品注册管理办法》的试题及答案解析,相信大家对于药品注册的相关知识有了更深刻的理解。无论是备考考试还是从事药品注册管理工作,掌握相关法规和操作流程是非常重要的。希望通过本文的学习,能够帮助您在药品注册的道路上走得更远,顺利通过相关的考试或工作挑战。