随着我国医药行业的不断发展和改革,药品的质量安全问题越来越受到重视。为加强药品生产企业的规范管理,确保人民群众的用药安全,国家出台了《药品生产监督管理办法》(以下简称《办法》)。2020年,随着国家对药品行业的严格要求,《药品生产监督管理办法2020试题》成为了各大药品生产企业及从业人员备考的重要内容。它不仅是行业的法律依据,更是药品生产管理工作中的指南。
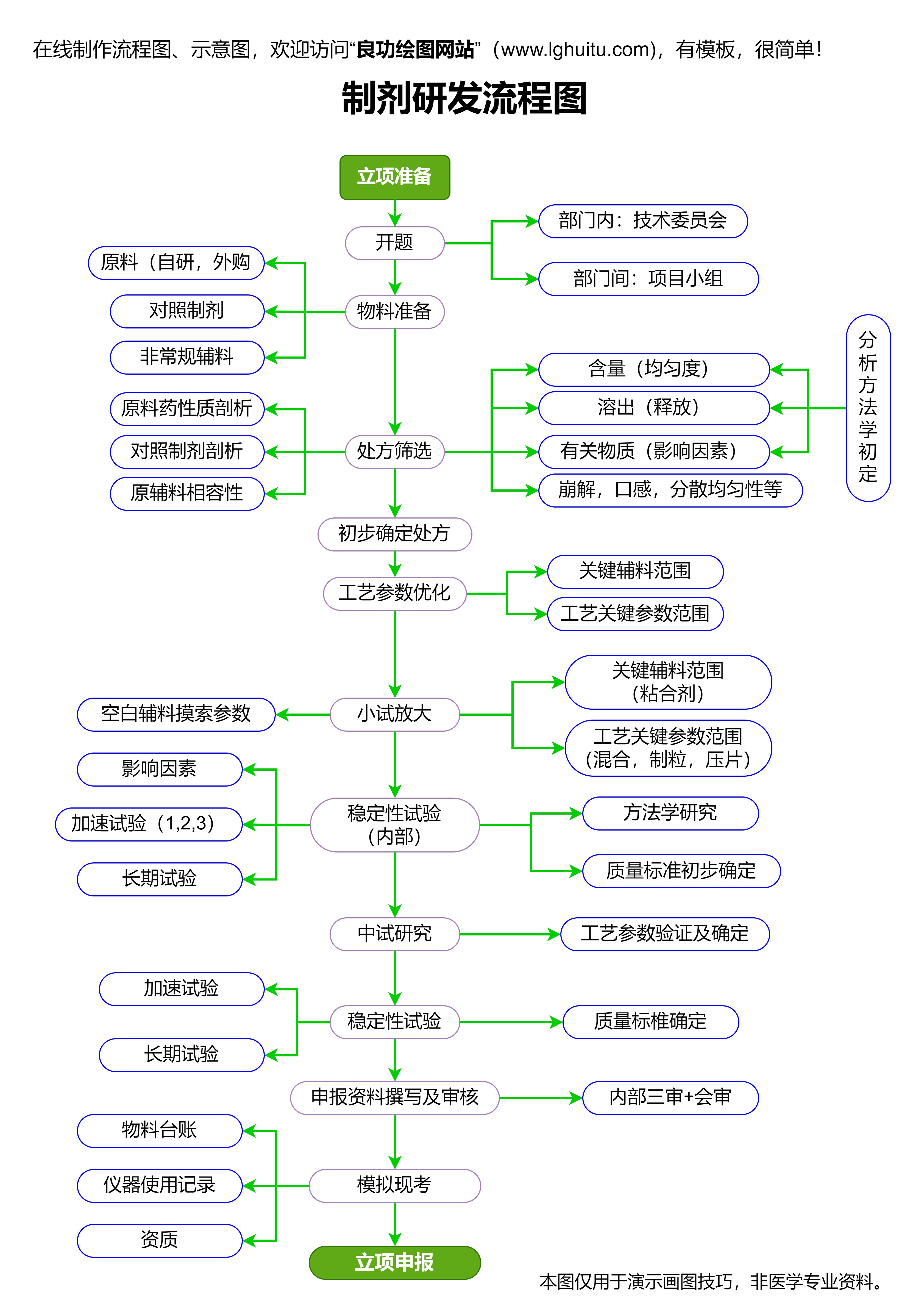
《办法》从多个维度对药品生产提出了严格的要求,特别是在生产许可、设施条件、质量管理体系等方面。《办法》明确规定了药品生产企业需要建立完善的质量管理体系,并通过认证以确保其生产的药品符合标准。法规对药品生产过程中的每一个环节进行规范,确保生产全过程的可追溯性。这些条款的实施无疑提高了药品生产的透明度和监管力度。
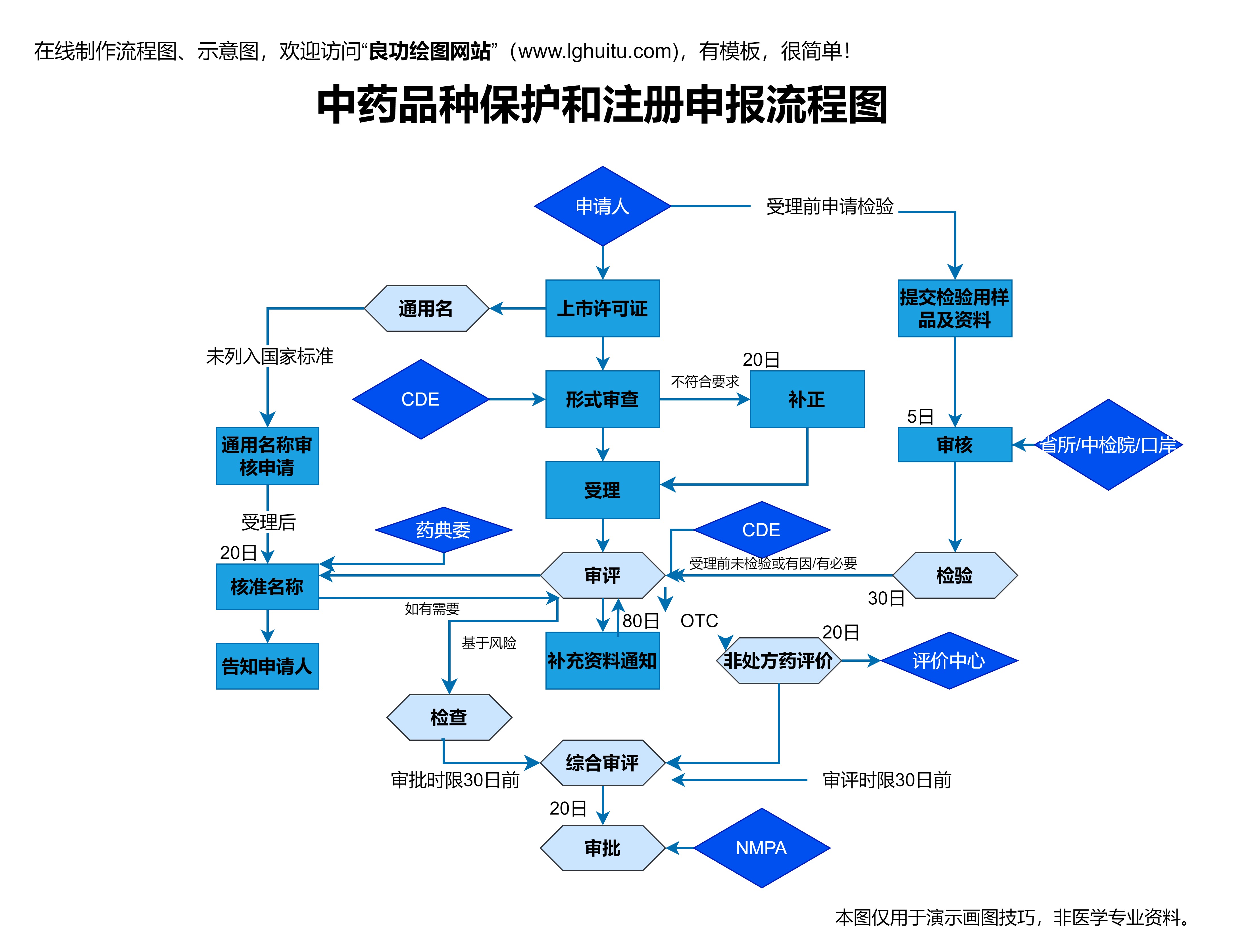
对于广大药品生产企业来说,掌握《办法》中的关键考点至关重要。企业需要通过专业培训和考试,确保所有从业人员都能了解法规的内容,并按照要求执行。尤其是药品生产管理者、质量管理人员、设备维护人员等,需要深入理解《办法》中的相关规定,确保生产过程符合质量管理的基本要求。
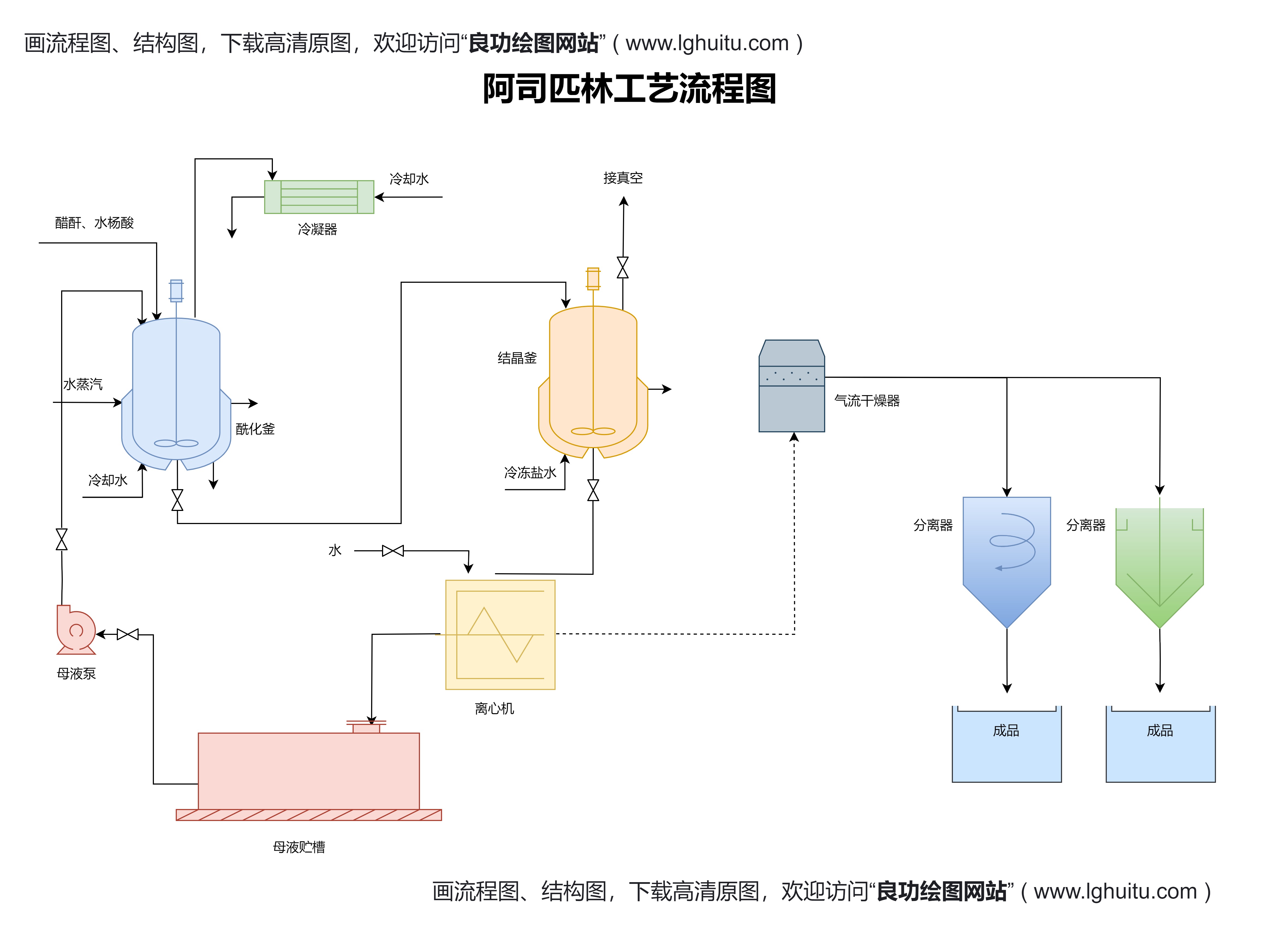
在《药品生产监督管理办法2020试题》中,考题往往围绕法规的核心内容展开,例如药品生产许可、质量控制要求、设施管理、生产记录、药品包装和标签等方面。考生必须理解这些规定的深层意义和具体操作要求,才能在实际工作中有效应对各种挑战。考试不仅是对从业人员知识水平的检验,也是提升企业整体合规能力的重要手段。
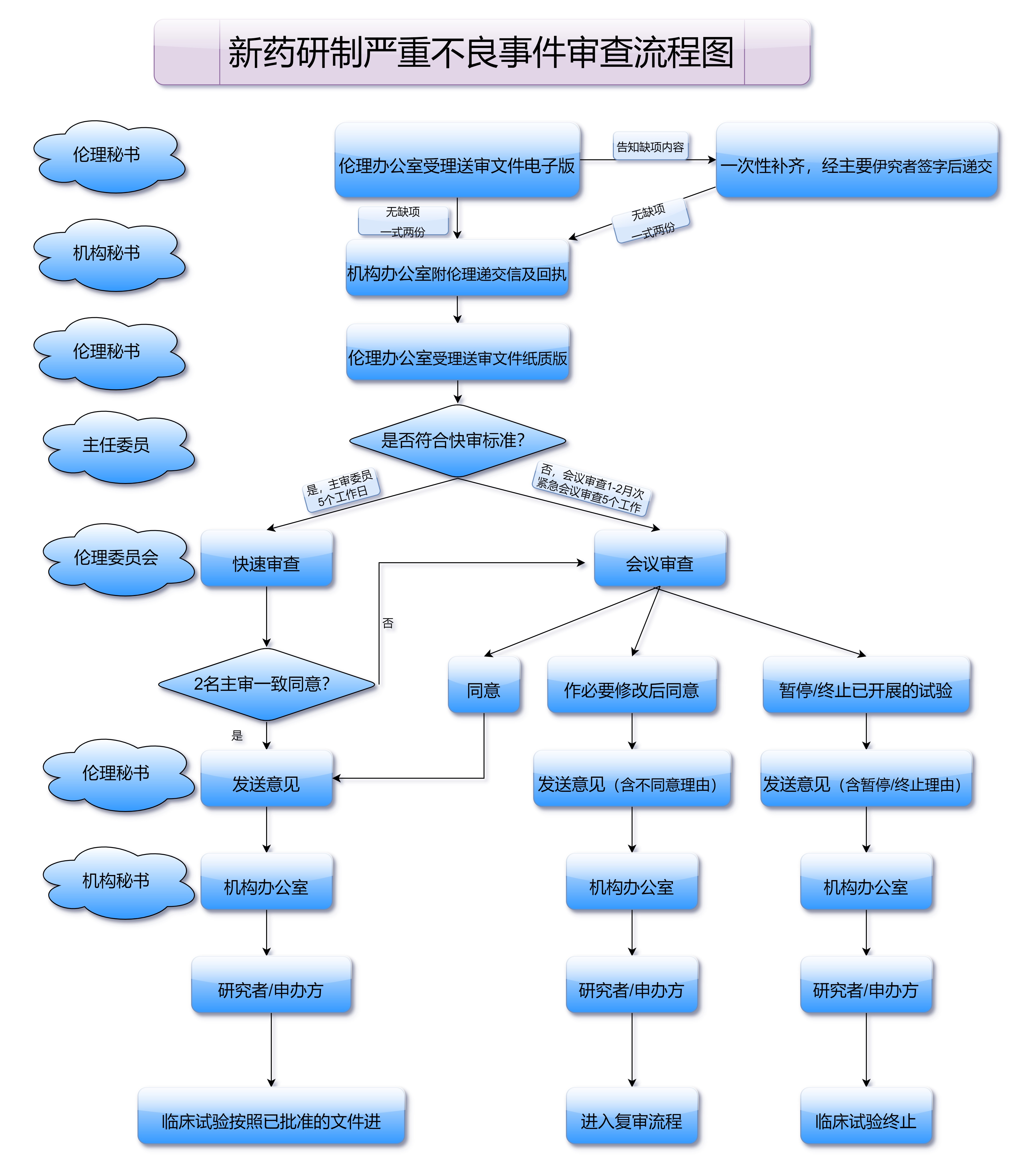
企业在备考《药品生产监督管理办法2020试题》时,可以通过模拟试题、案例分析、法规解析等多种方式进行准备。特别是在对法规条文的深刻理解上,企业可以通过集体讨论和专家讲解来加深对条款的把握,确保企业员工在实际操作中不会因知识盲点而导致合规风险。

除了考试方面,药品生产企业还应关注如何在日常运营中落实《药品生产监督管理办法2020》的相关要求。法规的实施不仅仅是为了满足考试的要求,更重要的是确保企业在实际生产中严格遵守规定,避免因违规操作带来的法律责任与经济损失。
在《办法》发布后,许多药品生产企业已经开始着手调整自己的生产管理体系,以符合新的监管要求。在生产许可方面,企业需要重新申请生产许可证,并接受相关部门的审查。这一过程包括对生产场地、生产设备、人员资质、管理流程等的全面审核。企业必须确保各项设施设备符合规定的标准,并配备符合要求的专业人员。只有这样,才能顺利获得新的生产许可,继续合法生产。
企业需要建立健全的质量管理体系。质量控制是药品生产的生命线,任何质量安全问题都可能导致严重后果。因此,《办法》对药品生产中的质量管理提出了严格要求。企业必须通过实施GMP(药品生产质量管理规范)来确保生产过程中的每一个环节都得到有效控制。这包括原料采购、生产工艺、质量检测、包装储存等各个环节的质量把控。
《药品生产监督管理办法2020》还强调了药品生产过程中的透明度和可追溯性。企业需要完善药品生产记录,并确保每一批次药品都能够追溯到具体的生产环节。这一要求不仅有助于提高药品的质量控制,也能在出现问题时快速定位源头,进行有效处理。因此,药品生产企业在日常运营中,需要建立完备的记录管理系统,确保所有生产数据的准确性和完整性。
随着《办法》实施的深入,药品生产企业的合规成本也逐渐增加。尽管如此,这些要求对于提升药品行业整体的安全性和信誉度具有重要意义。企业应通过加大培训力度、强化内部管理、完善质量控制体系等方式来应对新的法规要求。在合规的道路上,虽然挑战重重,但只要企业能够全力以赴,便能够为社会提供更加安全、有效的药品产品。
《药品生产监督管理办法2020试题》不仅是药品生产企业从业人员必备的考试内容,更是企业管理者需要深入理解和遵守的法规。通过认真学习和准备,企业不仅能够顺利通过考试,还能提升整体的生产管理水平,确保药品质量安全,为公众的健康保驾护航。