在现代医学不断发展的今天,药品的研发和上市是一个复杂且严格的过程。药品的从无到有,涉及多个环节,每一步都关乎着公众的健康和安全。从最初的药物发现,到最后的上市推广,每一个环节都需要经过严格的筛选和审核。药品从研发到上市的流程究竟是怎样的呢?我们将为大家详细解析这一流程的每一个环节,帮助您更好地理解制药行业的复杂性与挑战。

药品的研发之路,从药物的发现开始。这是一个漫长且充满挑战的阶段,涉及到大量的基础研究、临床前试验以及大量的试验数据收集。药物发现的第一步是对目标疾病的深入研究,分析疾病的机理、病因以及治疗现状。科学家们会基于现有的药理学、基因组学等信息,筛选出潜在的药物靶点,并在此基础上进行化合物的筛选和优化。
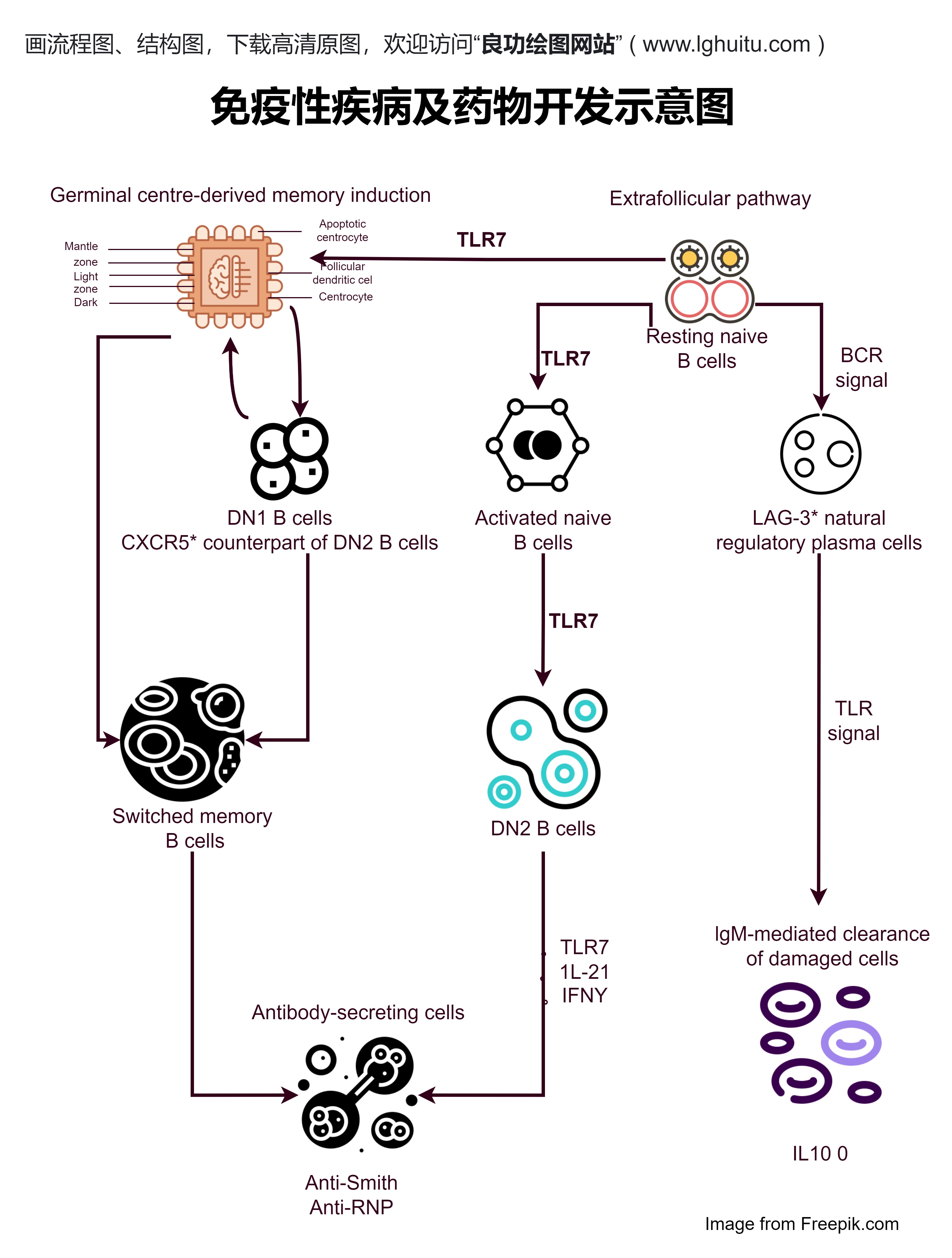
在这一阶段,药品研发团队会利用多种技术手段,包括计算机模拟、实验室测试等,寻找具有治疗效果的化学成分,开展前期的药理学研究和动物实验,为后续的临床研究奠定基础。
2.临床前研究(PreclinicalStudies)
当药物发现并确认具有潜力后,接下来就是进行临床前研究。临床前研究的主要目的是评估药物的安全性和初步疗效。这一阶段通常会使用动物模型进行药物的毒性、药代动力学(药物在体内的吸收、分布、代谢和排泄过程)和药效学研究。通过这些研究,可以初步了解药物的剂量范围、潜在副作用以及治疗效果。
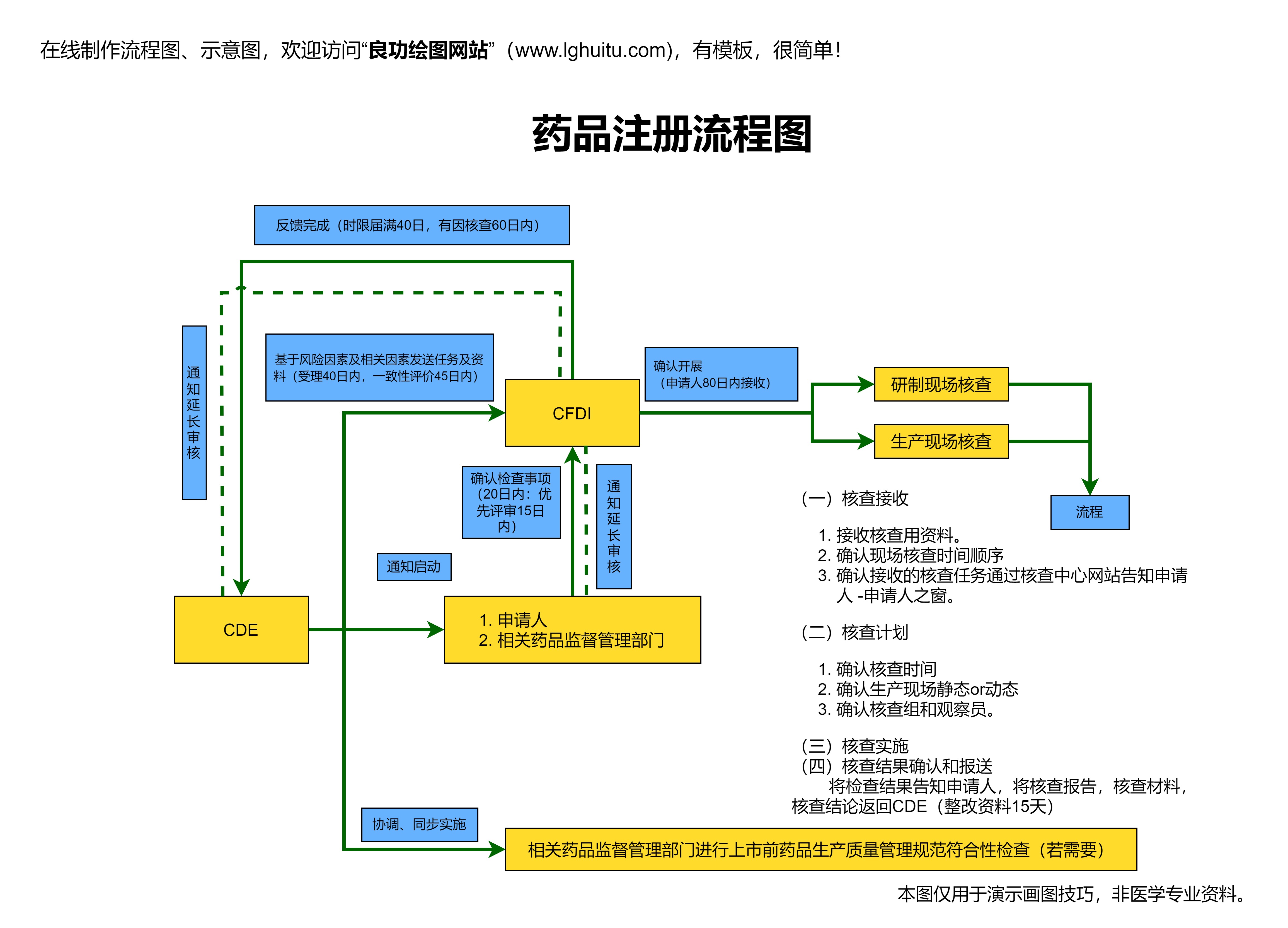
在这个阶段,研究团队需要对药物进行多项测试,如急性毒性、慢性毒性、致癌性等方面的测试,以确保药物在进入人体临床试验之前能够保证基本的安全性。
临床试验是药品研发中至关重要的一步,也是药物上市前的关键环节。临床试验一般分为三期,每一期的目标不同,依次推进药物的安全性和有效性评估。
第一期临床试验(PhaseI):这一阶段主要是在少量健康志愿者身上进行,旨在评估药物的安全性、药代动力学特性以及最佳剂量。由于参与者大多数是健康人,试验的风险相对较低。
第二期临床试验(PhaseII):在第二期临床试验中,药物会在少量的病人群体中进行,主要目标是评估药物的疗效、副作用及最适用的治疗方案。这一阶段,研究者会探索不同剂量下的药物效果,找到最优剂量。
第三期临床试验(PhaseIII):这是药物临床试验中最重要的一步,通常会招募成百上千的患者进行大规模的对照研究。此时,研究者的目标是全面评估药物的长期疗效与安全性,特别是不同患者群体中的疗效差异。第三期试验成功后,药物便进入申请上市的阶段。
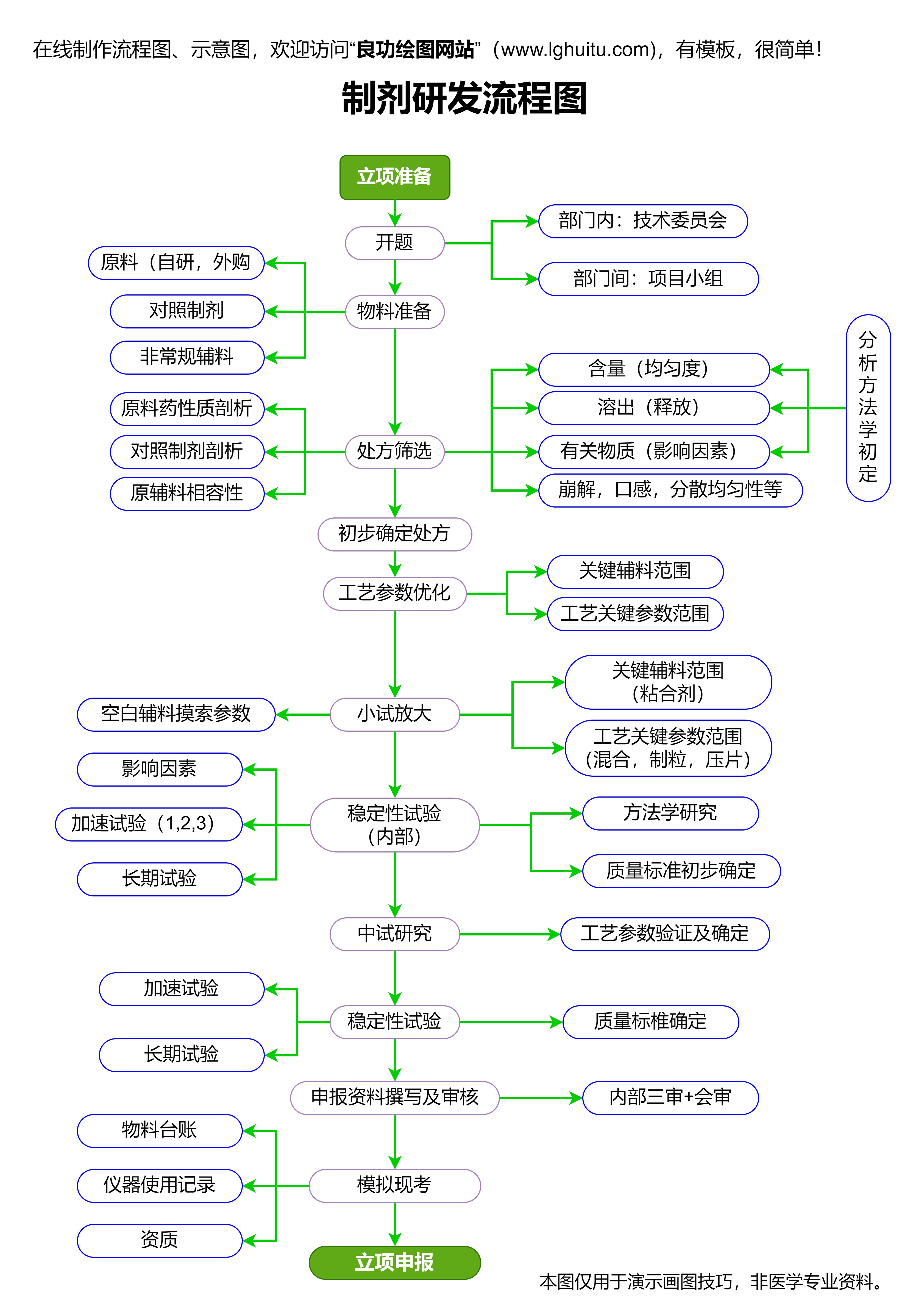
当临床试验数据表明药物具备一定的安全性和有效性后,研发公司就会向各国药品监管机构(如中国的国家药品监督管理局,NMPA;美国的食品药品监督管理局,FDA)提交申请,申请药品的上市许可。这一阶段被称为药品审批阶段。
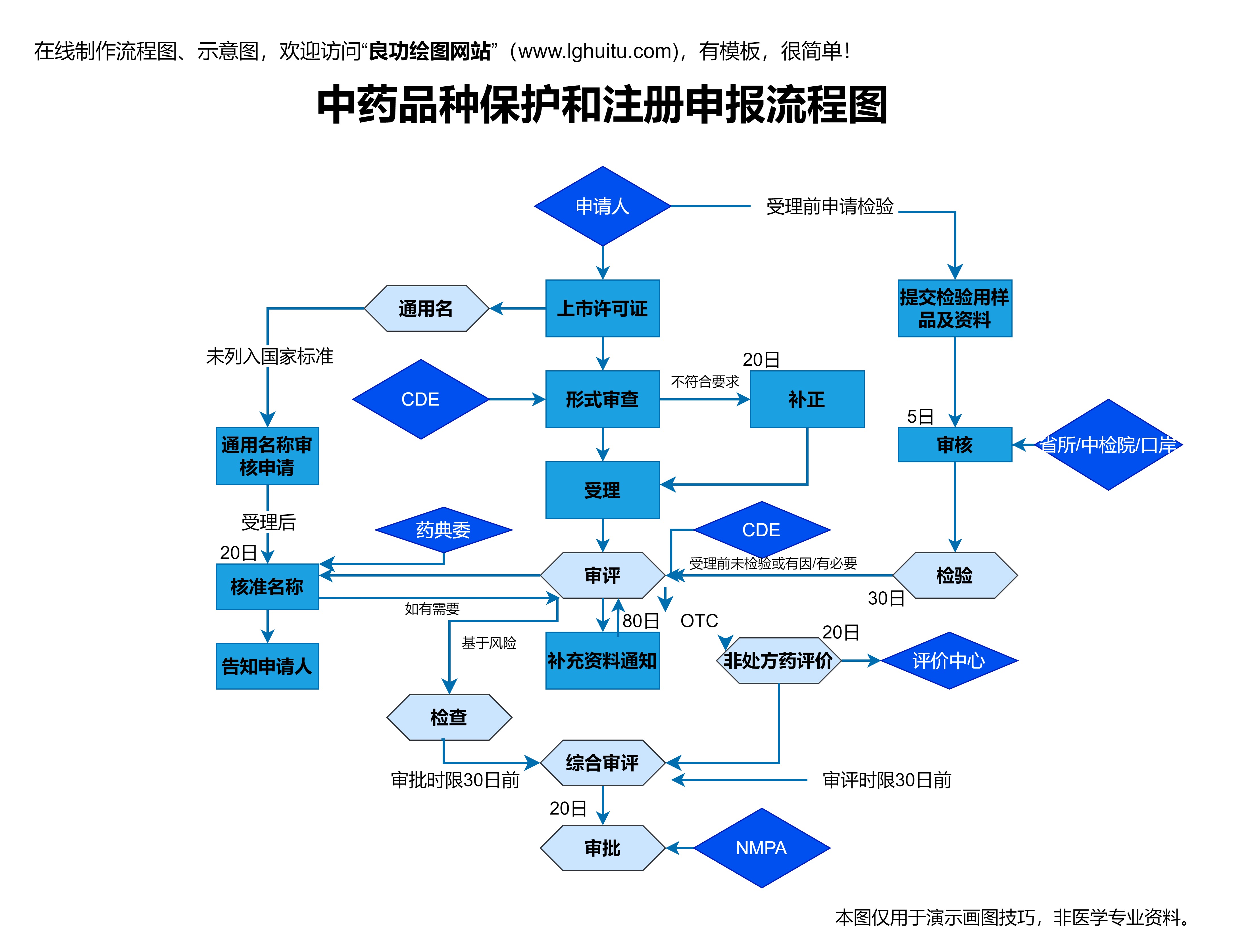
监管机构会对药物的临床试验数据、生产工艺、质量控制等进行全面审核。如果一切符合规定要求,监管机构将授予药物上市许可,药物正式进入市场。
5.药品上市后的监测(Post-marketingSurveillance)
即使药品上市后,研发公司和监管机构依然需要进行持续的安全性监控。这是因为临床试验通常是在相对控制的环境下进行的,而上市后的药物会在更广泛的人群中使用,可能会出现一些预料之外的副作用。因此,药品上市后会进行不间断的监测,确保药物的长期安全性。
药品研发和上市的过程充满了挑战和复杂性,每一个环节都不可忽视。在这个漫长的过程中,科学家们不仅要不断攻克技术难题,还要面对无数的不确定性。正是这一系列严格的流程,确保了我们能够使用安全有效的药物来对抗疾病,保障公众健康。
6.药品的商业化(Commercialization)
药品成功上市之后,商业化的过程也同样不可忽视。商业化不仅仅是药品的生产和销售,还包括市场推广、医生和患者教育、渠道管理等多个环节。药品研发公司需要通过市场调研,了解患者的需求和偏好,制定出合适的定价策略、推广方案和销售网络。
药品公司还需要与医院、医生、保险公司等建立紧密合作关系,确保药品能够在医疗体系中得到广泛应用。通过精准的市场推广和广泛的临床应用,药品才能真正发挥其治疗作用,造福更多的患者。
7.药品的定期复审与更新(PeriodicReview&Updates)
药品上市后,并非一劳永逸。随着时间的推移,药品的疗效可能会受到新研究成果的影响,而药品的安全性也可能会随着更多的临床数据得到进一步验证。因此,药品需要定期进行复审。
定期复审的目的是对药品的长期使用情况进行回顾,评估药品的治疗效果与副作用之间的平衡。在这一过程中,可能会发现一些新的适应症、新的副作用或者对药物的剂量进行调整。如果需要,监管机构可以要求药品公司更新药品的说明书,或者对药品进行重新评估。
8.药品专利保护与仿制药市场(PatentProtection&GenericDrugs)
药品的研发需要投入大量的资金和人力,因此制药公司往往会通过申请专利来保护其研发成果。在药品的专利期内,药品公司拥有对该药物的独占权,其他公司无法生产和销售同样的药物。随着专利期的到期,仿制药公司可以进入市场,生产价格较低的仿制药。
仿制药的出现使得药品的价格更具竞争力,为更多患者提供了治疗选择。对于制药公司来说,如何在专利期内赚取足够的利润,同时在仿制药上市后仍然保持竞争力,是一个重要的挑战。
9.未来药品研发的趋势(FutureTrendsinDrugDevelopment)
随着科技的不断进步,药品研发也在发生巨大的变化。基因疗法、细胞疗法、精准医学等新兴技术不断涌现,为药品研发开辟了新的方向。人工智能、机器学习等技术的应用,也大大提高了药品研发的效率和精准性。
未来,药品研发将更加注重个体化治疗,针对不同患者的基因特征和病理特征,开发出更加精准的药物。随着这些技术的发展,药品研发的流程也将更加高效、安全,为全球患者带来更多治疗选择。
药品研发和上市是一个复杂且严谨的过程,涵盖了从基础研究到临床试验,再到药品上市后的持续监控等多个环节。每一步都充满挑战,但正是这些环节的严格把控,保证了药品的安全性和有效性。随着科技的进步和行业的不断发展,未来的药品研发将更加精准和高效,为全球患者带来更多的治疗希望。