药物开发是一个充满挑战和机遇的漫长过程。从最初的发现阶段,到最终药物上市,每一个环节都需要科学家们经过数年的努力和无数次实验才能成功实现。在这一过程中,药物经历了四个主要阶段:发现与研发、临床前研究、临床试验和上市后监测,每一阶段都至关重要。
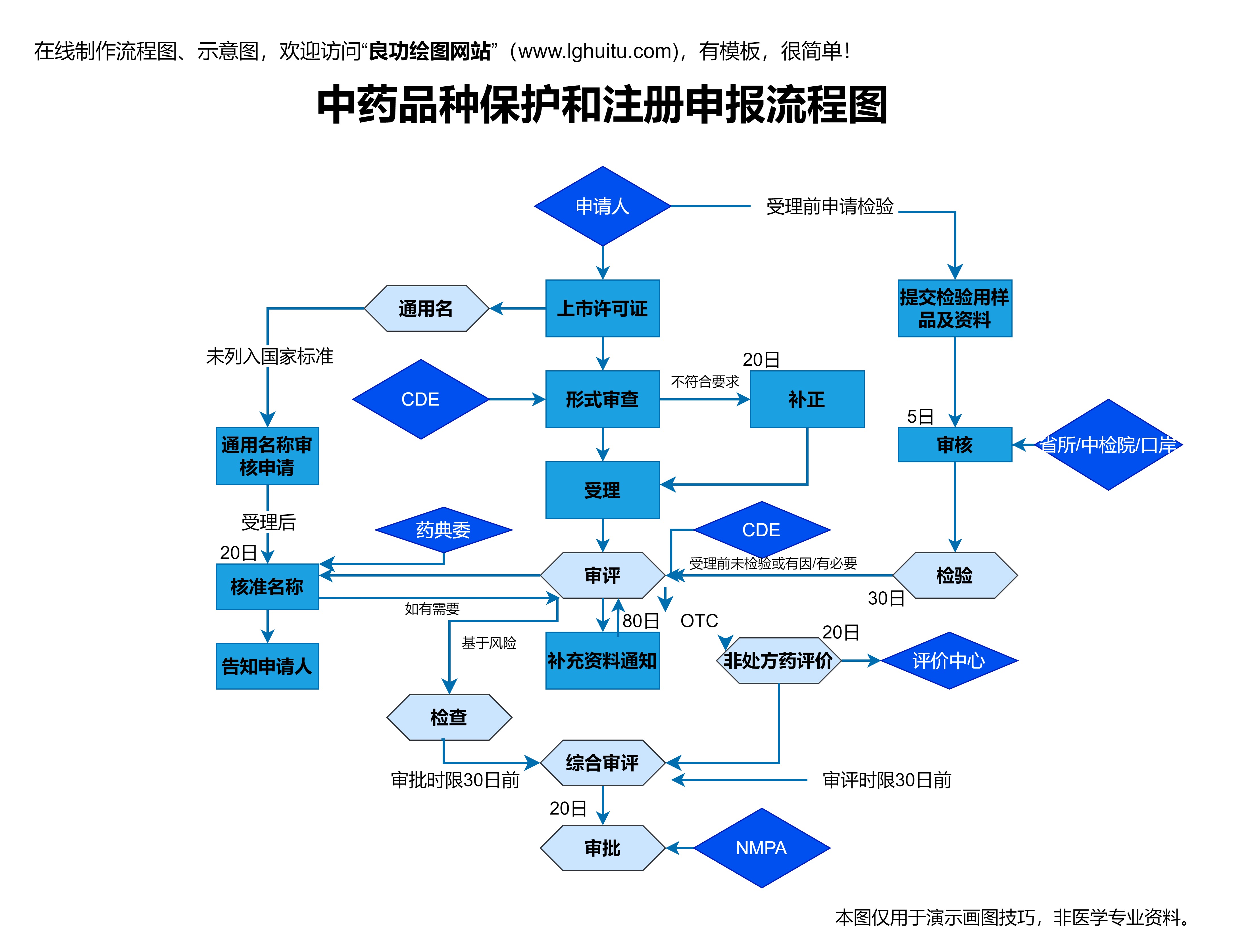
药物开发的第一步是药物的发现与研发。这个阶段主要包括从化学、植物学、动物学等多个领域寻找潜在的药物候选分子。科学家通过对各种疾病的深入研究,了解疾病的机制、原因和病理学,进而锁定具有治疗潜力的靶点。这一过程通常需要几年的基础研究和实验验证。
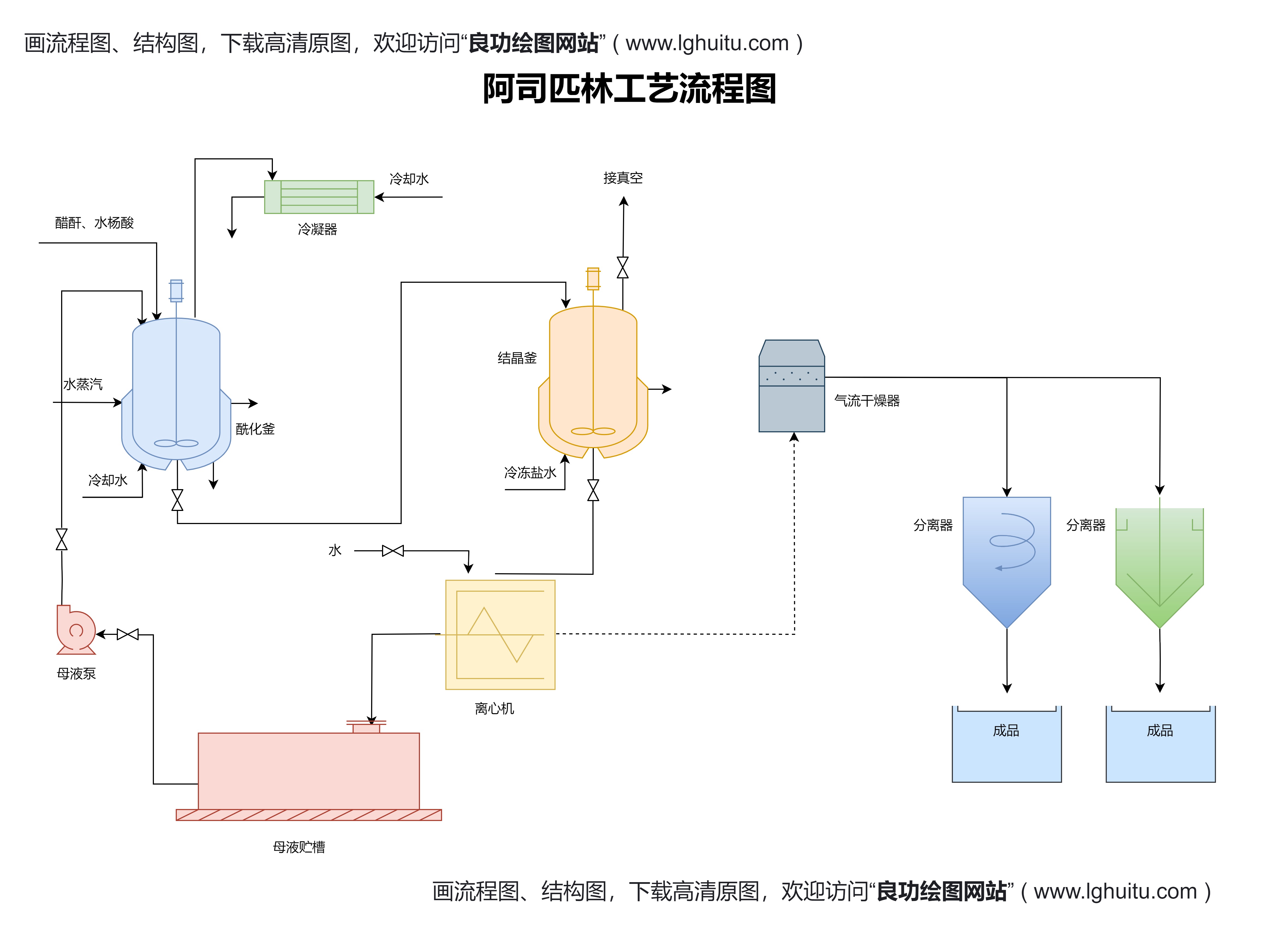
药物研发的核心在于发现一个有效且安全的候选分子。在这个阶段,研究人员会进行大量的实验室工作,筛选出能够与疾病靶点产生有效作用的化合物。常见的药物发现方法包括高通量筛选、分子对接、结构生物学研究等。这些方法帮助研究人员找到了对抗某些疾病的“钥匙”,并为下一步的药物设计奠定基础。
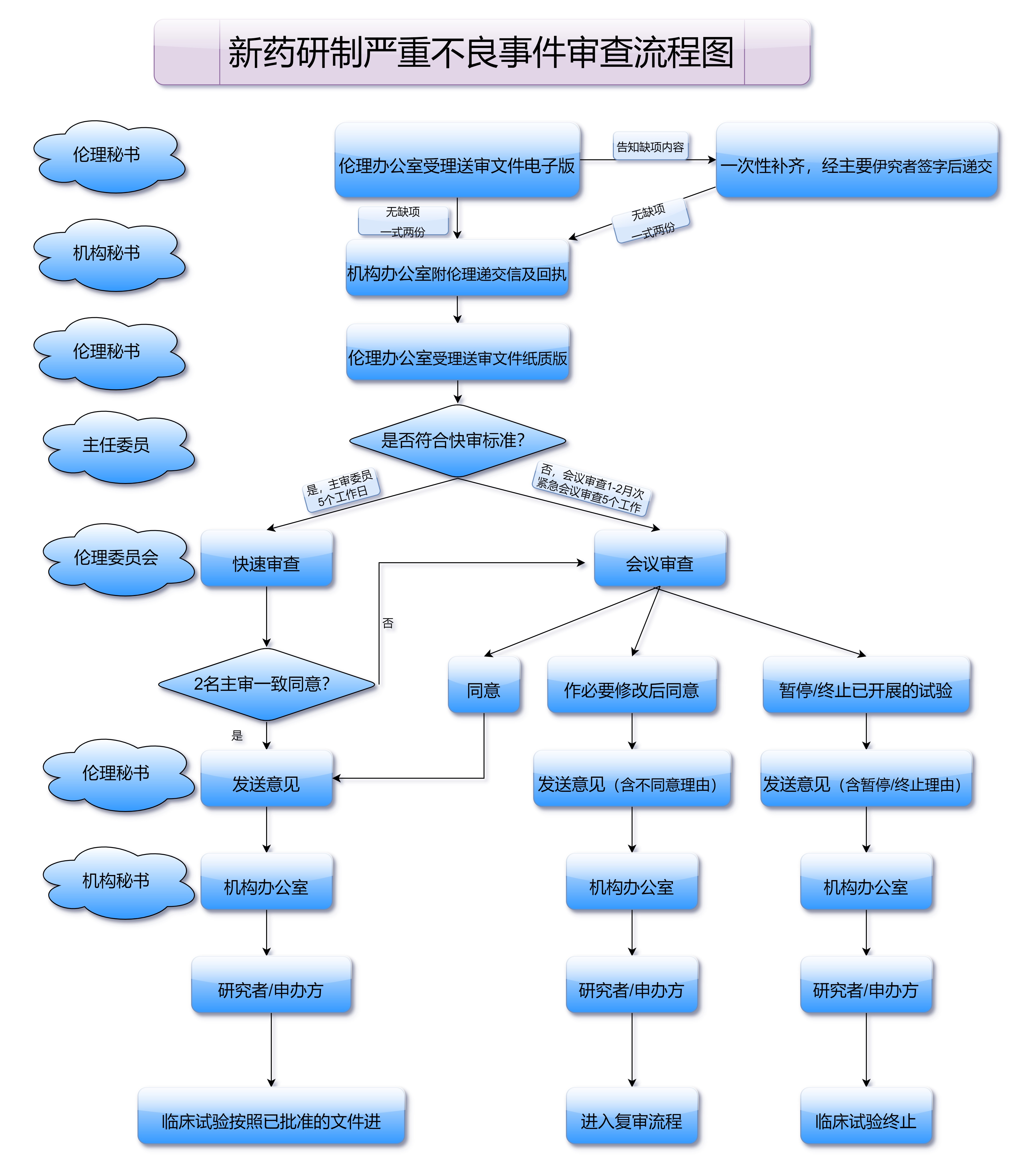
在发现阶段,除了候选药物的筛选与优化外,药物的毒性、溶解性和稳定性等方面也会进行初步评估,以确定其是否具有成为药物的潜力。如果这一阶段的研究结果表明该候选药物有可能达到预期效果,且具备基本的安全性,它将进入临床前研究阶段。

临床前研究是药物开发的第二个阶段,通常涉及在实验室和动物身上进行的研究。这个阶段的主要任务是进一步验证药物的安全性和有效性。临床前研究的目标是通过实验室的细胞实验、动物实验等多种方式,全面评估候选药物的药理学、毒理学、药代动力学(即药物在体内的吸收、分布、代谢和排泄)等关键指标。
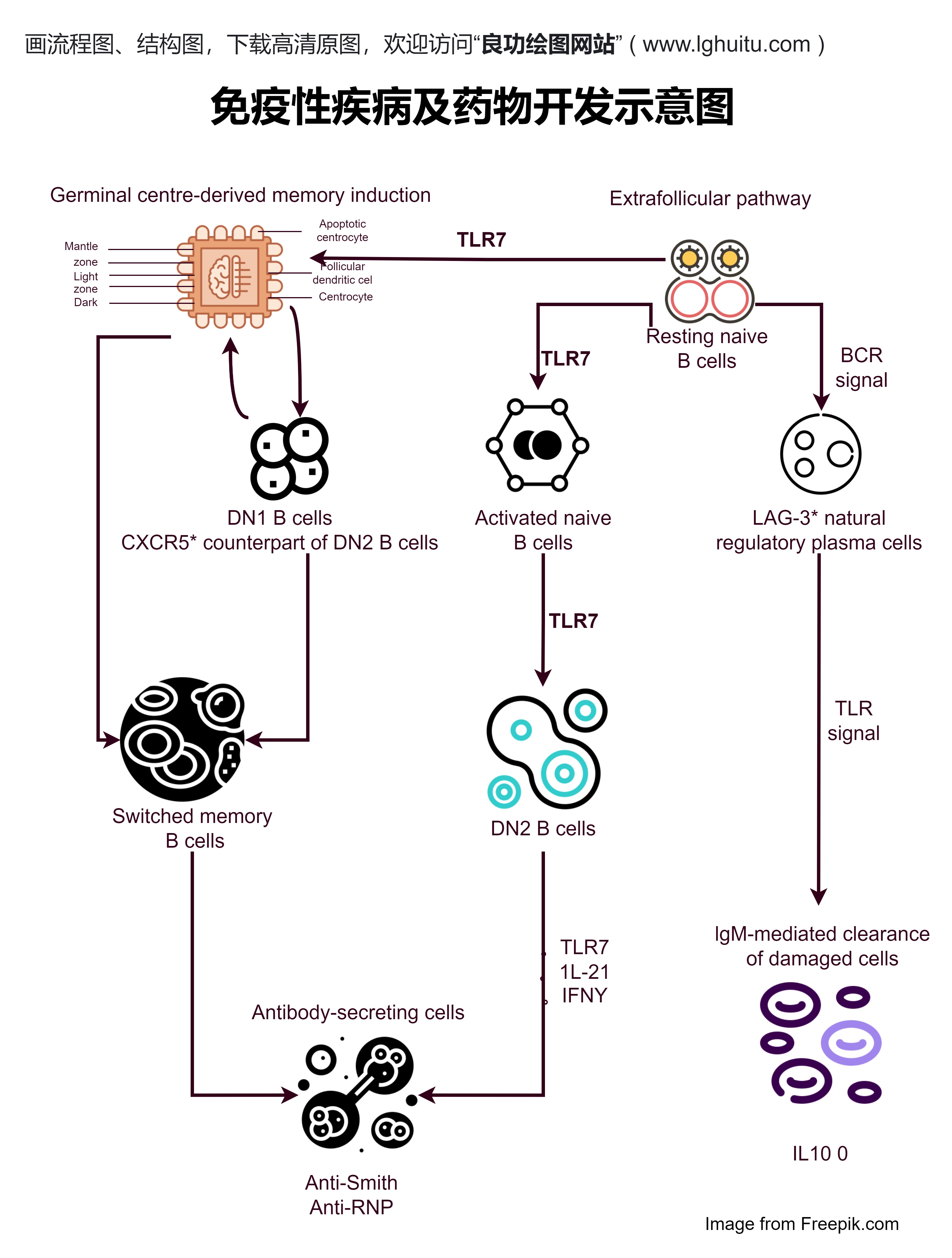
在这一阶段,研究人员通过动物模型模拟人类的生理环境,评估药物在体内的表现。这些实验帮助科学家了解药物是否能在体内有效地达到治疗靶点,药物的剂量范围是否安全,是否存在毒副作用,以及药物在体内的稳定性等。
临床前研究阶段的成功与否决定了药物能否顺利进入临床试验阶段。如果药物在临床前研究中表现出良好的效果,且没有严重的副作用,它便会被批准进入临床试验阶段,开始在人类身上进行实验。
临床试验是药物开发中最为关键的阶段之一。在这一阶段,候选药物将正式进入人体实验,经过三期临床试验验证其疗效和安全性。临床试验通常分为三个主要阶段:I期、II期和III期。
I期临床试验是药物进入人体实验的首次尝试,通常涉及少量健康志愿者(20-100人)。这一阶段的主要目的是测试药物的安全性、耐受性和药代动力学特征。科学家将通过监测志愿者的反应,来评估药物在人体内的代谢情况以及可能的副作用。
II期临床试验的参与者通常会增加到100人以上,且这部分人群中大多数为患有相关疾病的患者。在这一阶段,研究的重点是评估药物的疗效和副作用。药物的剂量、使用频率等问题会在此阶段得到进一步的优化。
III期临床试验是规模最大的临床试验,通常涉及几百到几千名患者。该阶段的目标是全面验证药物的疗效和安全性,并与现有治疗方法进行对比。在此阶段,药物的副作用以及长期使用的影响也将得到充分评估。如果第三阶段的临床试验成功,药物便可以向监管机构申请批准上市。
药物上市后监测,又称为IV期临床试验,标志着药物研发过程的最终阶段。虽然药物已经获得批准上市,但仍需要继续对其进行监测,确保其在实际使用中的安全性和疗效。上市后监测的主要任务是通过收集大量患者的使用数据,评估药物在广泛人群中的长期效果和罕见副作用。
这一阶段主要通过药物不良反应的报告系统、流行病学研究以及对患者健康记录的分析来进行。药品的真实世界效果和安全性可能与临床试验中的结果不同,因此,上市后监测非常重要,它帮助监管机构及时识别潜在的药物问题,并采取相应的措施,如修改药品说明书、限制使用范围、甚至撤回药品。
药物开发的四个阶段是一个复杂而细致的过程。每个阶段都在确保药物最终能够安全有效地造福患者方面发挥着至关重要的作用。随着科技的不断进步,药物开发的效率和成功率也在逐步提高,但无论如何,药物的研发都需要经过严格的科学验证和监管,确保每一款上市的药品都能为患者带来真正的福祉。