药物研发是一个庞大且繁复的系统工程,它涉及到多个领域的紧密合作与高度集成,从药物的初步发现、临床前研究到最终的临床试验,每一个环节都至关重要,影响着新药能否顺利上市。药物研发不仅是科学家的挑战,更是技术与创新的博弈。为了帮助大家更好地理解药物研发的复杂过程,本文将通过药物研发流程图来一一解读这一过程的每个关键节点。
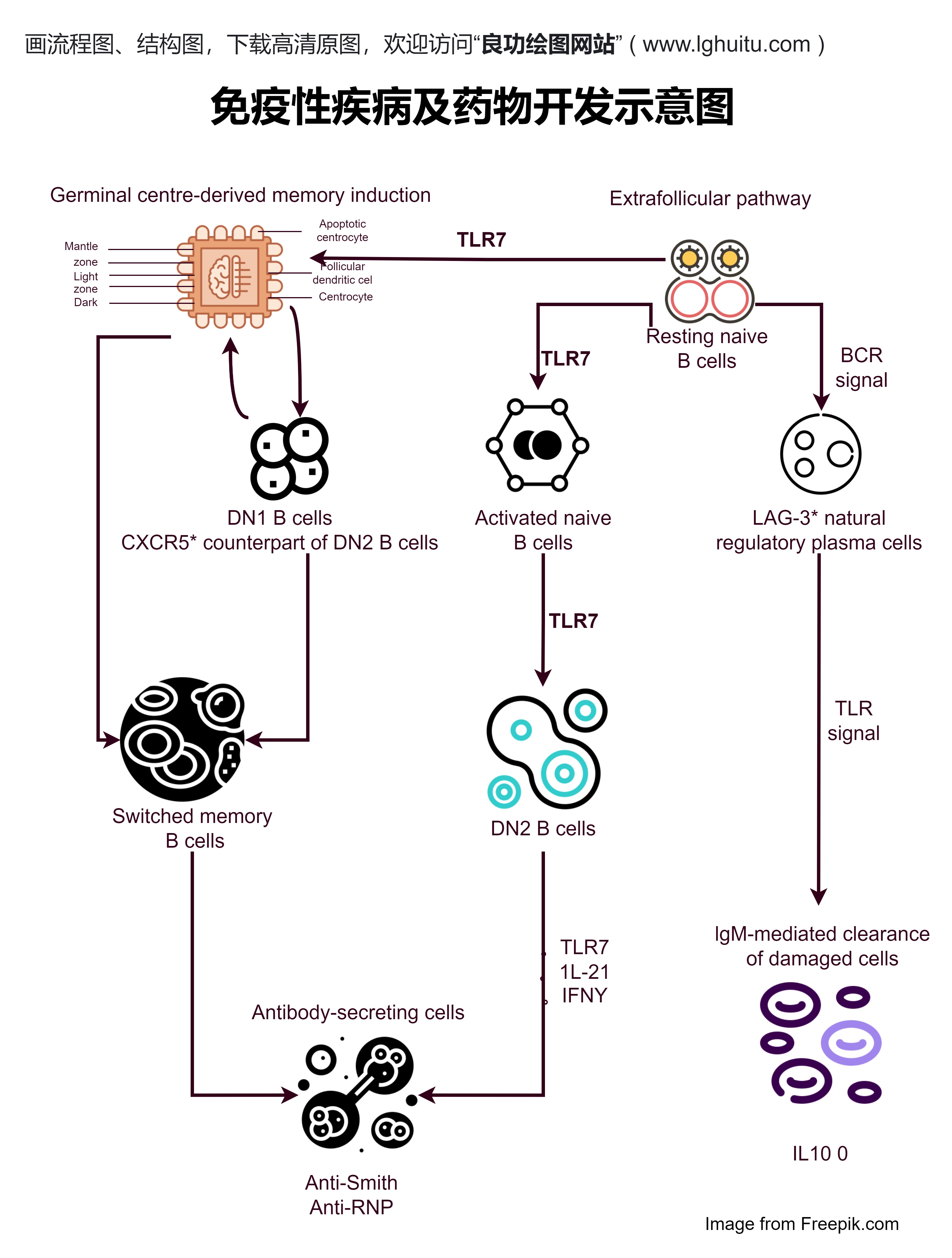
药物研发的第一步是药物发现,也被称为靶点发现阶段。科学家们通过深入分析疾病的分子机制,识别出可能的药物靶点,通常是某种特定的蛋白质或基因,这些靶点在疾病的发生和发展中扮演着重要角色。靶点确定后,科研人员利用化学合成、分子筛选等方法,发现能够与靶点有效结合并调控其功能的化合物。这一阶段的核心是高效的筛选技术和前沿的生物学知识。
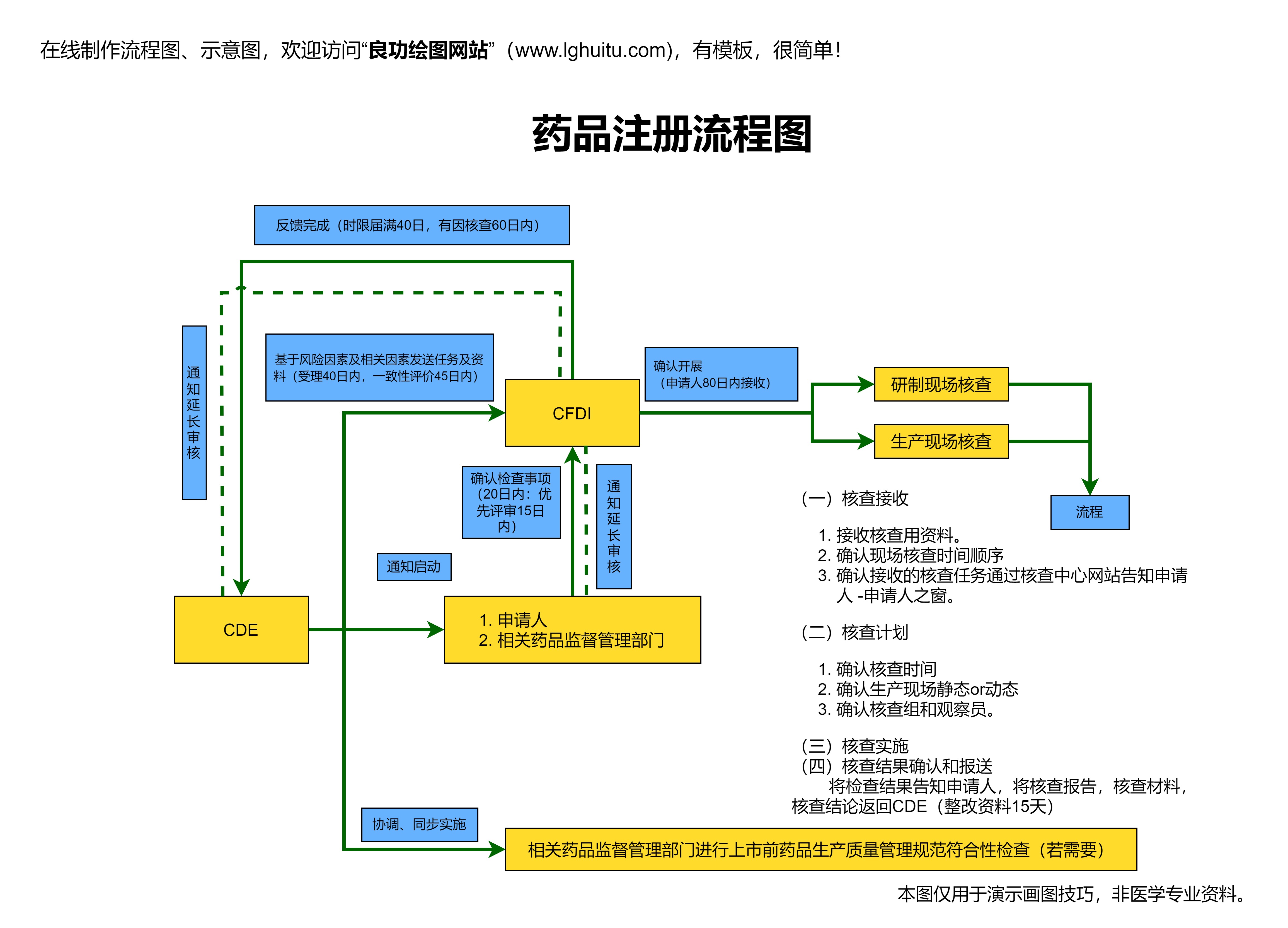
在药物发现阶段成功筛选出候选化合物后,研发团队将进入临床前研究阶段。这一阶段的主要任务是评估药物的安全性和有效性。临床前研究一般包括动物实验、毒理学研究、药代动力学和药效学评估等内容。通过这一系列的实验,研发人员能够初步了解药物的毒性、代谢途径以及是否能够有效对抗目标疾病。只有在通过这些基础性研究后,药物才有可能进入临床试验阶段。
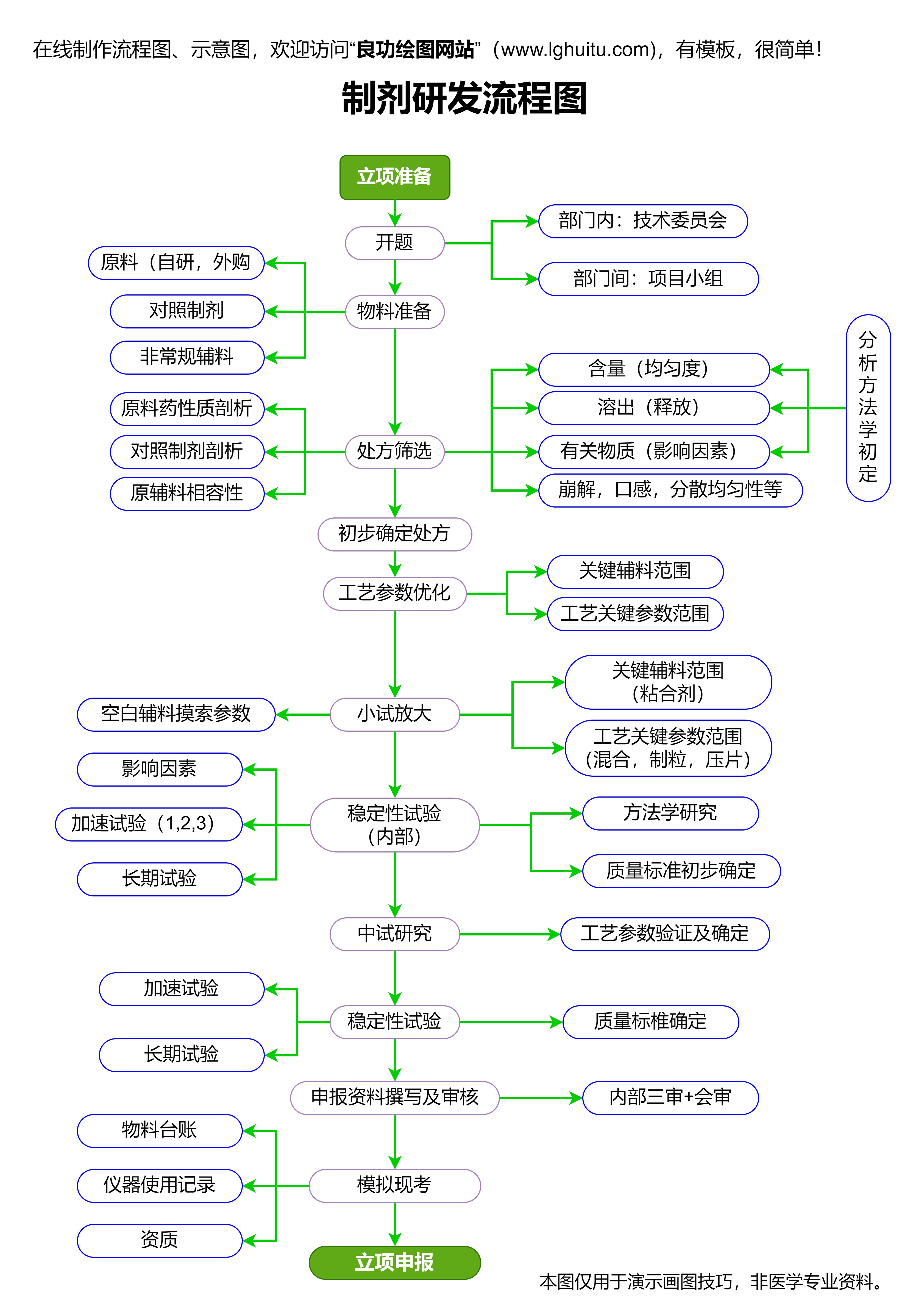
临床试验是药物研发中的重头戏,它是验证药物安全性、有效性和耐受性的关键环节。临床试验分为三个阶段:I期、II期、III期试验,每个阶段都具有不同的目标和实验对象。
I期临床试验主要是在少数健康志愿者中进行,主要目的是评估药物的安全性、剂量范围以及副作用。这一阶段通常为期数个月,确保药物对人体没有明显的毒副作用。
II期临床试验进入患者群体,研究药物的疗效,并进一步优化剂量。此阶段的试验通常为期一年左右,研究药物在特定疾病患者中的有效性。
III期临床试验是药物研发的最后一个阶段,通常在多中心、大规模的患者群体中进行,主要目的是全面评估药物的疗效和安全性,为药物的上市申请提供充分的临床数据。
临床试验阶段结束后,药物将进入药品审批阶段。药品的生产商需要向监管机构(如中国的国家药品监督管理局NMPA或美国的FDA)提交详细的临床试验数据报告和药品注册申请,以获得上市许可。监管机构会严格审查药物的临床试验数据、药品质量以及生产过程等,确保药物符合所有的安全和有效性标准。审批通过后,药物即可进入市场。
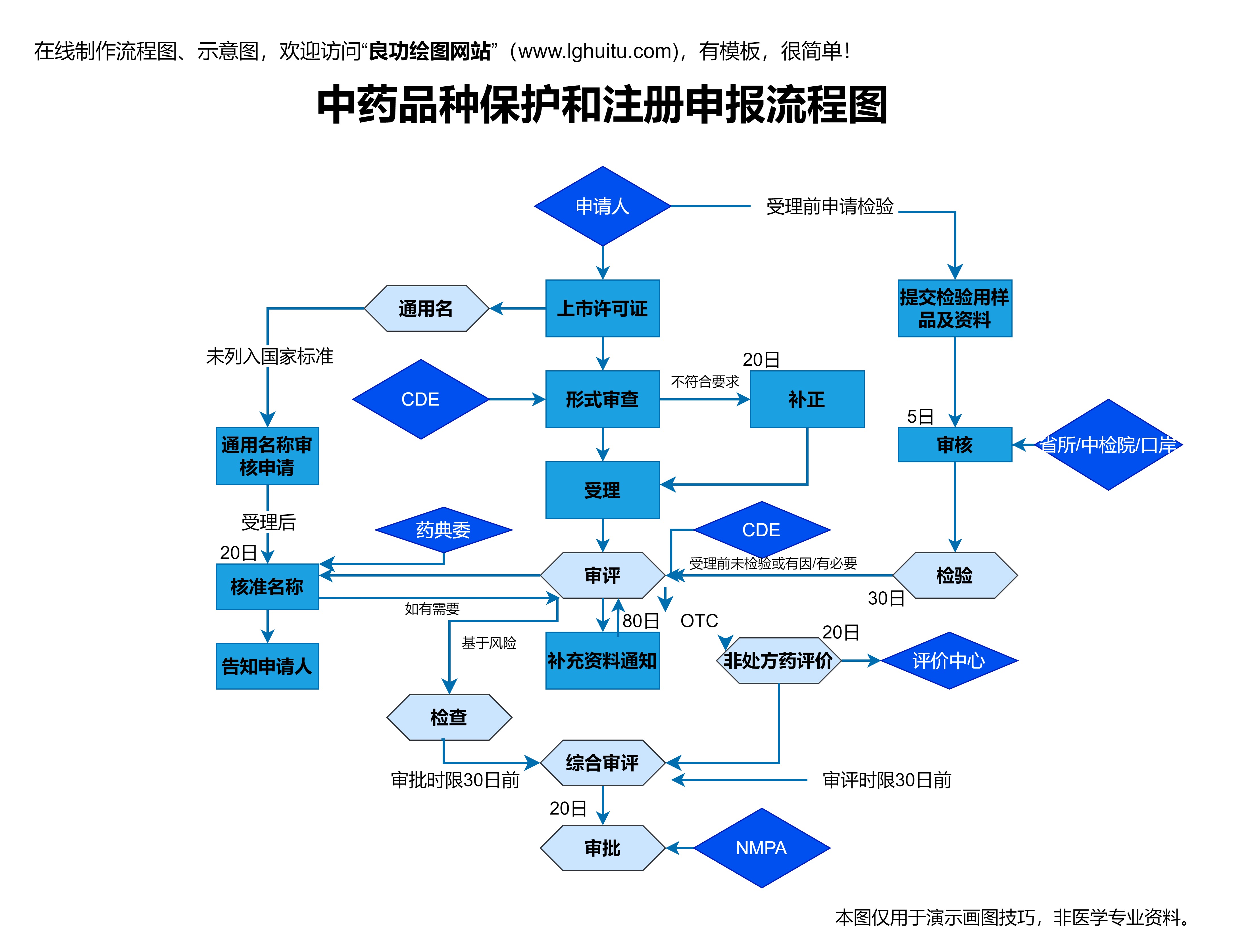
药物一旦上市,它并不意味着研发的终结。药物上市后,仍然需要持续的安全性监控。这一过程被称为四期临床试验或药物上市后的药物监测。虽然临床试验提供了大量的数据支持,但药物在真实世界中的使用环境和特定人群的反应仍可能存在未知的风险。因此,药物上市后,生产商和监管机构会对药物的安全性、疗效及任何可能的副作用进行长期跟踪调查。这一阶段对于患者的健康至关重要,能够及时发现潜在的药物风险,保障公众的用药安全。
药物研发是一项极具挑战性的工作,伴随其中的有高风险、高投入以及长周期等特点。据统计,平均每10000个化合物中,只有1个能够最终上市,这使得药物研发面临着极大的资金压力和市场风险。药物研发的成功不仅需要创新的科学技术,更依赖于跨学科的协作、长期的资金支持以及灵活的研发策略。
随着技术的不断进步,特别是基因组学、人工智能、大数据分析等新技术的不断应用,药物研发的前景依然充满希望。通过精准医学的推动,未来的药物研发将更加个性化和精确。比如,基于基因组学的个体差异,研发人员能够为不同患者量身定制药物,从而提高疗效并降低副作用。

药物研发不仅仅是一个技术层面的挑战,更是对人类智慧和探索精神的考验。无论是在早期的药物发现、临床试验,还是在药物上市后的监管和监测,每一步都充满了未知和不确定性。正是因为有了无数科研人员的辛勤付出,才使得我们能够享受到一个个有效的药物治疗方案,从而延长生命、提高生活质量。药物研发的过程虽然漫长,但每一次突破都在为全球数百万人的健康带来希望。随着科技不断进步,药物研发将更加高效、安全、个性化,未来的药物世界值得我们每个人期待。