作为全球第二大制药市场,中国在药品生产和质量管理方面有着严格的标准和要求。每一部《药典》的更新都标志着制药行业的一次技术革新,而《中国药典2010版二部附录》则是其中的重要组成部分。二部附录内容的发布,给中国制药企业带来了重要的指导意义,尤其在药品的生产、检验、质量控制等方面,提供了更为明确的操作标准和技术要求。
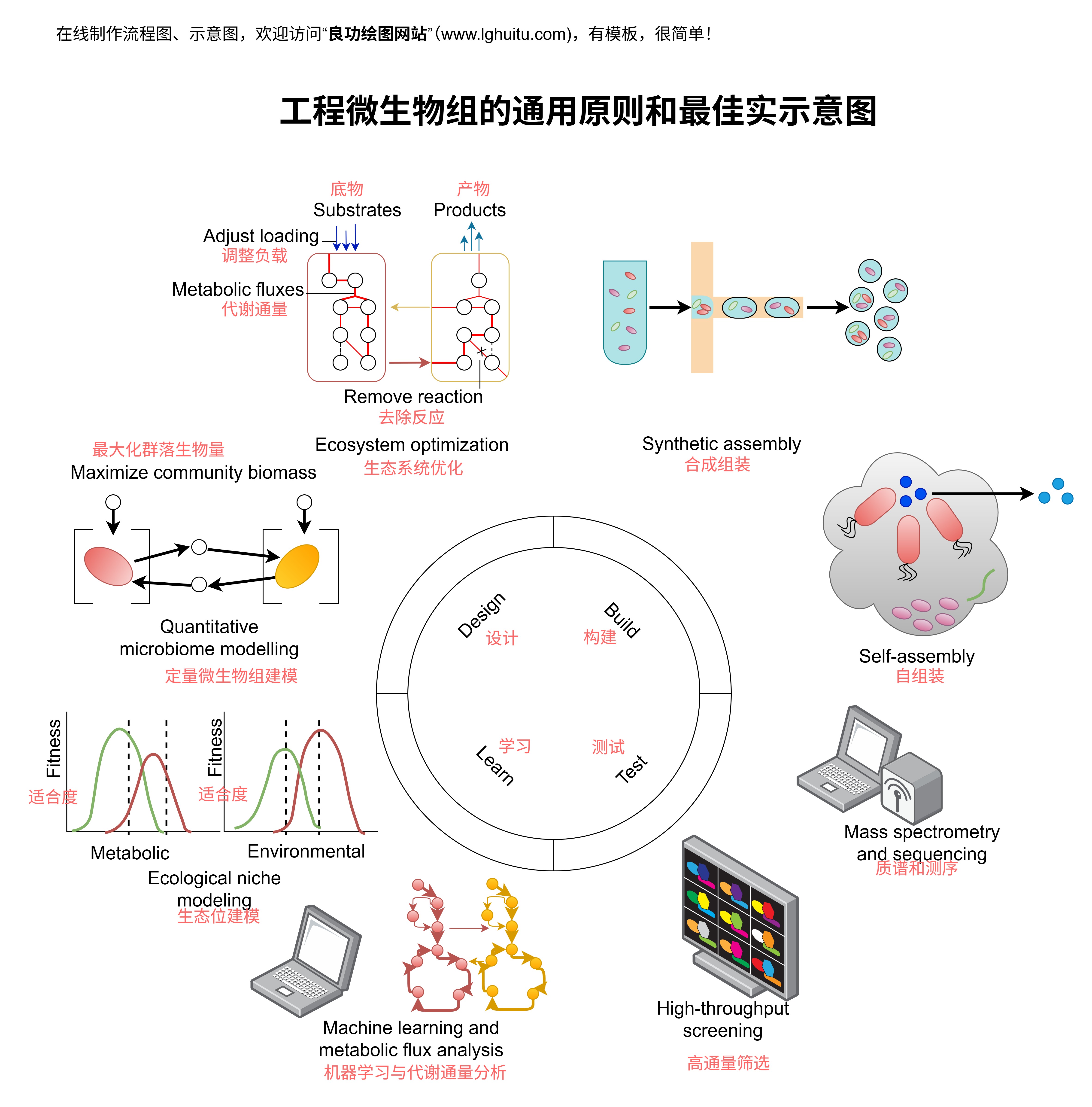
《中国药典2010版二部附录》是《药典》中的一个附加部分,主要针对药品的质量标准、检验方法、生产流程等进行补充和细化。该附录在全书中起到了重要的补充作用,覆盖了多个药品品种以及与药品质量控制相关的各种技术要求。例如,对药品中的有效成分、杂质含量、稳定性等方面提出了更为精细的标准。这些标准不仅对制药企业的生产流程有着重要影响,也对药品的质量监管提供了科学依据。
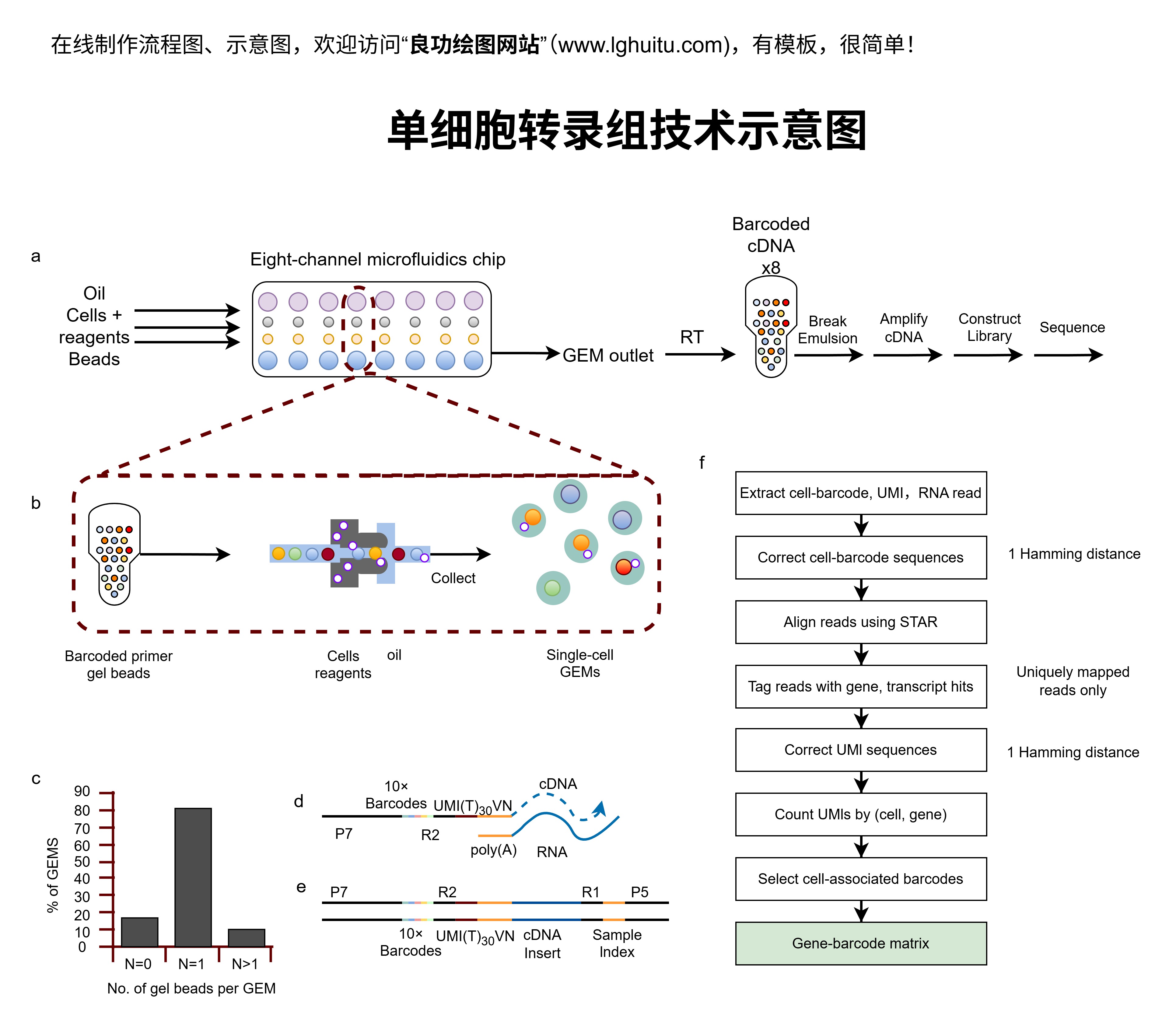
随着中国制药行业的不断发展,尤其是随着中国成为全球第二大药品市场,药品的质量问题日益成为公众和监管机构关注的重点。为了保证药品的安全性、有效性和可控性,中国药监局通过更新《中国药典》来加强对药品生产、流通和使用过程中的质量监管。2010版的更新便是基于行业发展的需求,对原有标准进行的修订和完善。
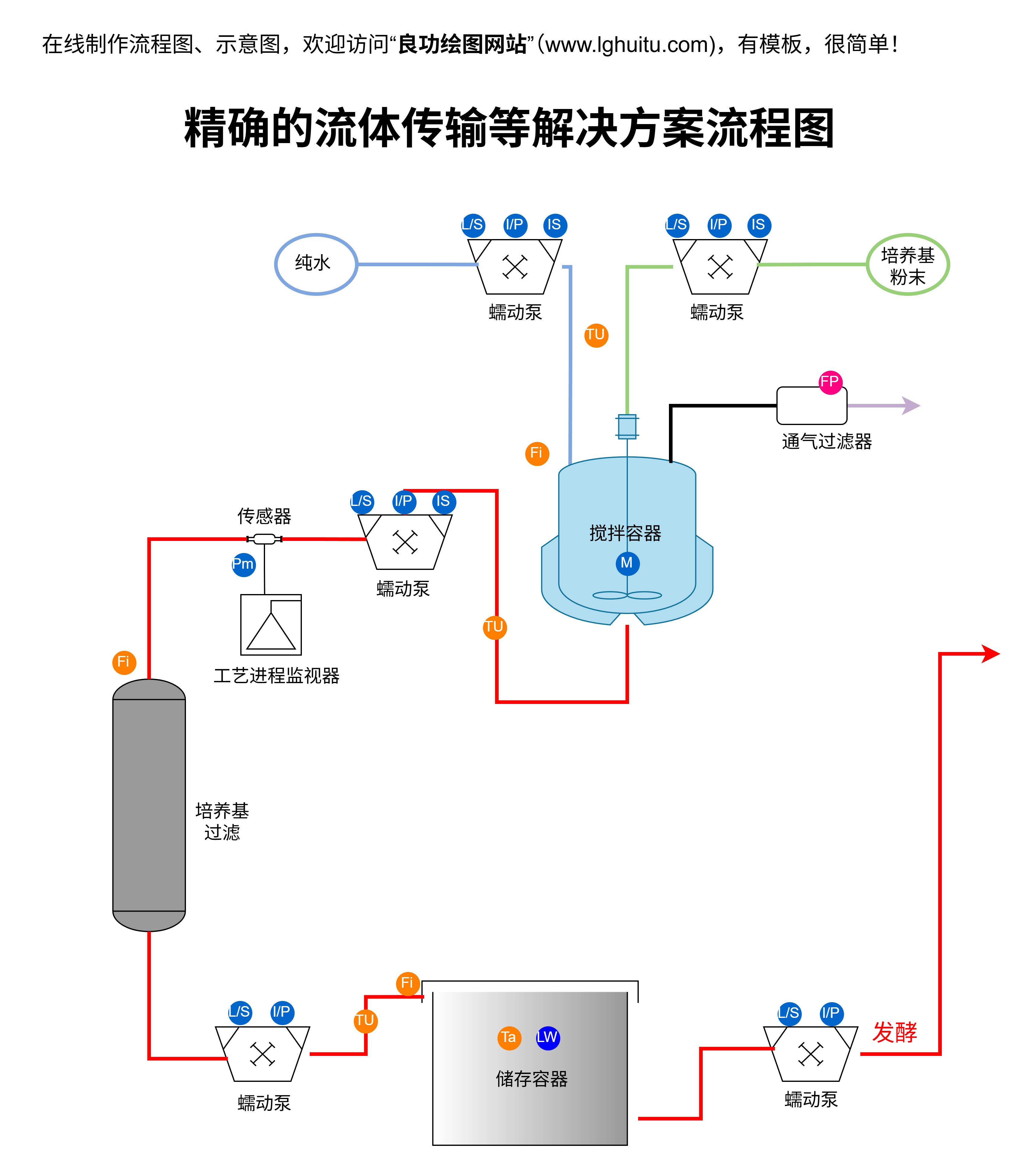
二部附录的实施正是回应了这一需求,它不仅强化了药品质量控制的技术规范,还为企业在实际操作中提供了操作指南。特别是在制药行业中,一些企业可能由于技术设备或人员水平等方面的差异,无法完全做到标准化生产,这时二部附录就为他们提供了一个相对统一且具有可操作性的技术标准。
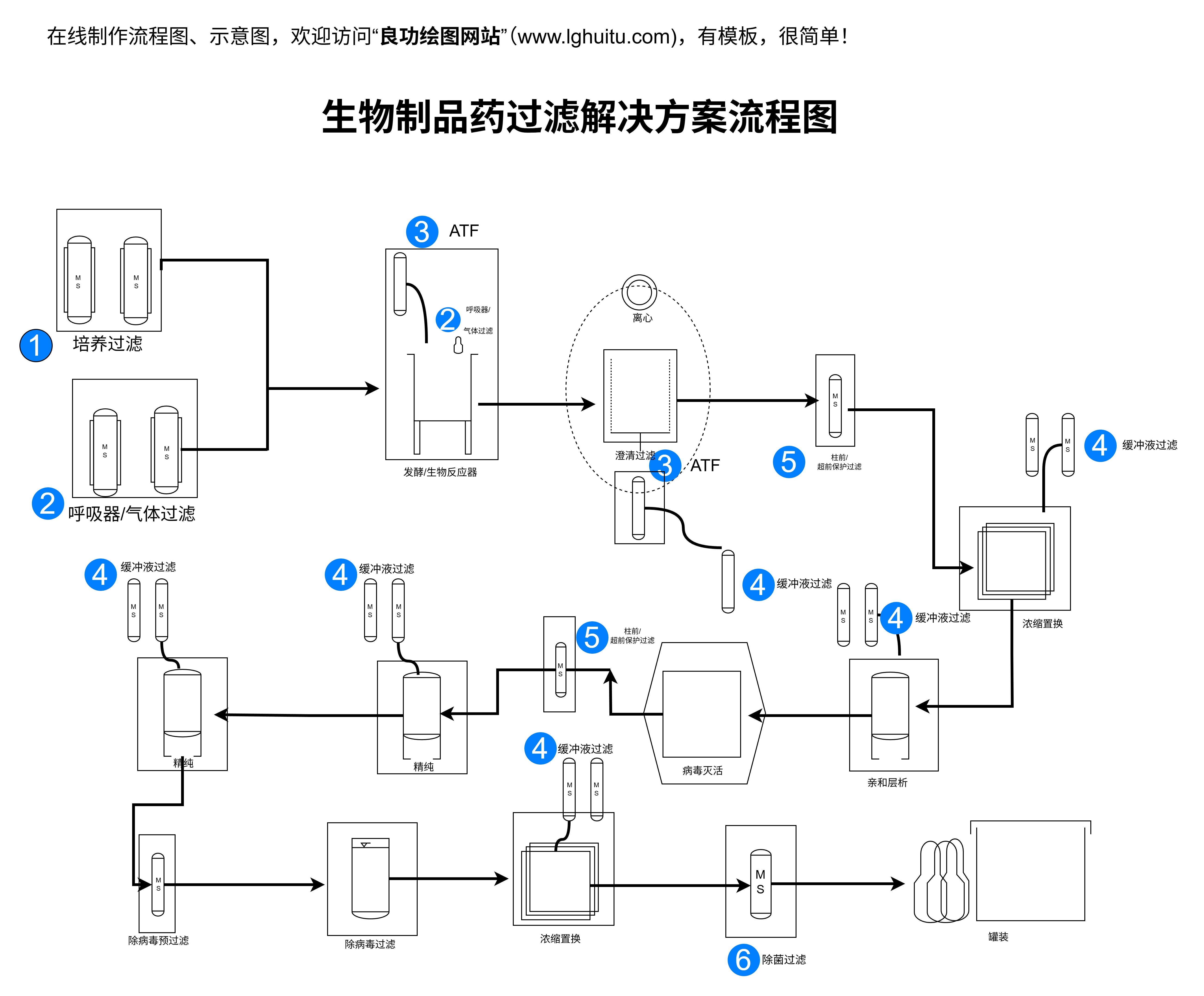
药品质量直接关系到患者的生命健康。随着药品品种的不断增多以及生产工艺的不断进步,药品的质量管理也面临着越来越多的挑战。《中国药典2010版二部附录》明确了药品质量管理的各项标准,旨在规范药品生产企业的操作流程,提高其生产的透明度与可控性,从而有效防范药品质量问题。
通过对药品质量的严格把关,二部附录帮助企业减少因质量问题而带来的市场风险,提升消费者的信任度。更为重要的是,随着附录中的标准化操作流程的推行,药品生产企业能够更加规范地进行质量控制,不仅降低了生产过程中的不良事件,也提升了产品的一致性与稳定性。
《中国药典2010版二部附录》涵盖了多个药品质量管理的核心领域,其中包括对药品生产过程中的关键步骤进行的详细规范。例如,在原料药的检验、包装材料的选择、药品生产设备的验证等方面,附录都给出了相应的标准化要求。这些细化标准的出台,不仅为制药企业的日常运营提供了明确的方向,也帮助监管部门有效加强了对行业的监控与管理。
在药品生产过程中,原料的质量控制是保证成品质量的基础。二部附录详细规定了从原料采购到生产工艺全过程的各项要求,确保了药品的每一环节都能够符合相关标准。对于生产设备的清洁与维护,也提出了严格的规范,以防止药品的交叉污染或设备故障等问题影响产品质量。
对于制药企业来说,二部附录的发布意味着他们需要更严格地遵守新的质量管理标准。这无疑增加了企业的生产成本和技术要求,但从长远来看,严格的标准化操作能够帮助企业提高生产效率,降低不合格产品的产生率。
例如,二部附录中的一项重要内容是对药品生产环境的要求,尤其是洁净室和生产车间的卫生条件。企业必须按照附录的规定,定期对生产设备、车间环境进行清洁、消毒并做好记录。对于药品生产的每一项操作,附录都要求详细记录,确保可追溯性,便于事后调查。
虽然这些措施在短期内可能会增加企业的成本,但它们有助于提高药品的整体质量和市场竞争力。通过严格按照附录要求生产,企业能够减少因产品质量问题而产生的市场投诉和退货,提升消费者对品牌的信任度。
《中国药典2010版二部附录》的发布不仅对制药企业有着深远的影响,更为整个社会的药品安全提供了保障。在全球化日益加深的今天,药品市场的竞争愈发激烈,药品的质量安全问题成为社会关注的焦点。通过推行严格的质量管理标准,不仅可以提升国内药品的国际竞争力,也能够更好地保护消费者的用药安全。
二部附录的发布也促使我国制药行业的管理水平不断提升,从而进一步推动整个行业的创新与进步。通过强化药品的质量监管与标准化管理,我国制药行业逐渐与国际接轨,为全球消费者提供了更为安全、有效的药品。
《中国药典2010版二部附录》不仅是药品质量管理的重要工具,也对整个制药行业的发展具有深远的意义。随着更多企业和机构严格执行附录中的标准,我们有理由相信,未来的中国制药行业将会迈向更加健康、安全的未来。