随着我国医疗器械行业的迅速发展,越来越多的企业希望能顺利进入市场,提供符合要求的医疗产品。在这个过程中,二类医疗器械的备案便成为了企业必须面对的关键环节之一。二类医疗器械备案不仅是产品合法销售的基础,还关系到产品的安全性和有效性。因此,掌握二类医疗器械备案的网上申报流程,对于每一个企业来说都是至关重要的。
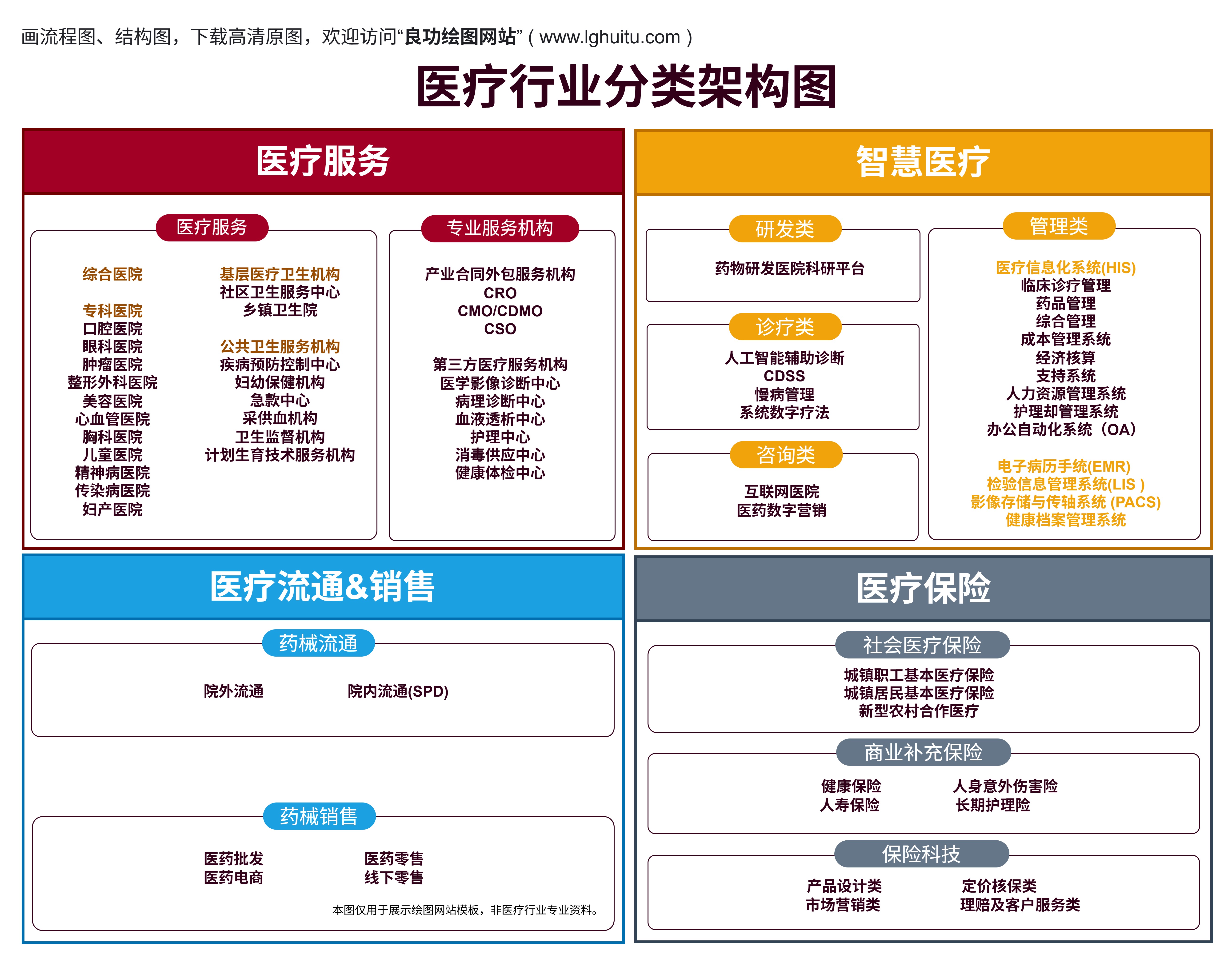
根据我国《医疗器械监督管理条例》规定,医疗器械分为三类,其中二类医疗器械是指对人体有一定风险,但风险较低的器械,通常包括一般诊断设备、治疗设备等。与三类医疗器械相比,二类器械的风险相对较小,但仍然需要通过备案来确保产品的安全性和有效性。
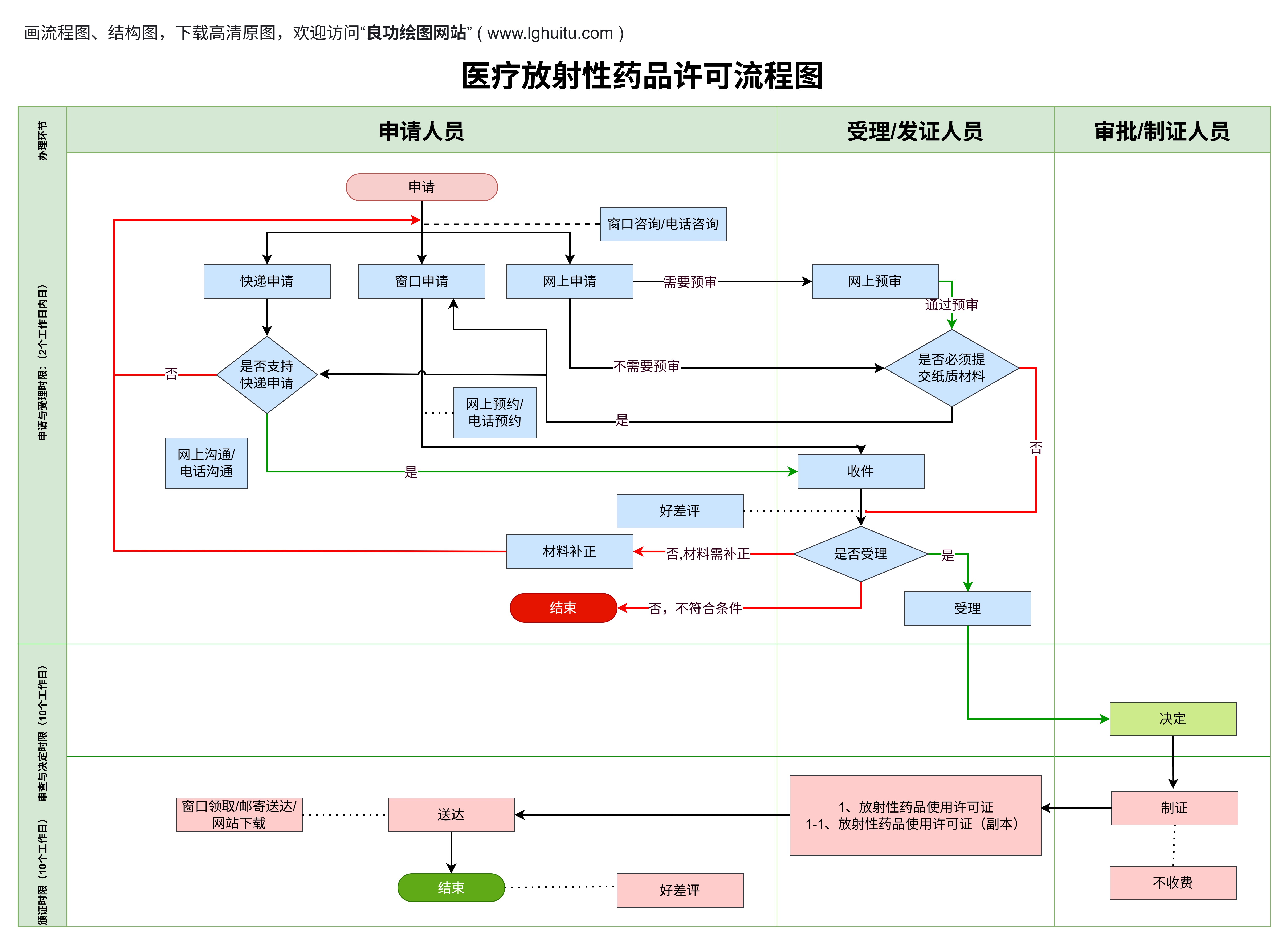
对于二类医疗器械,国家要求企业进行备案管理。备案工作不仅是企业履行法规要求的一部分,也是产品正式上市的前提。通过备案,企业能够获得市场准入的资格,并且让消费者信任该产品符合相应的标准和质量要求。
近年来,随着科技的发展,医疗器械的备案工作逐步走向网络化,企业可以通过“医疗器械注册管理系统”进行网上申报。这个系统的推出,极大地提高了备案工作的效率,减少了传统人工操作中的失误和时间成本。
在开始备案申报之前,企业需要首先在“医疗器械注册管理系统”上注册一个账号。通过注册,企业可以获取到专属的账号权限,进入申报系统。这一步骤需要提供企业的基本信息,包括公司名称、统一社会信用代码、联系人信息等。
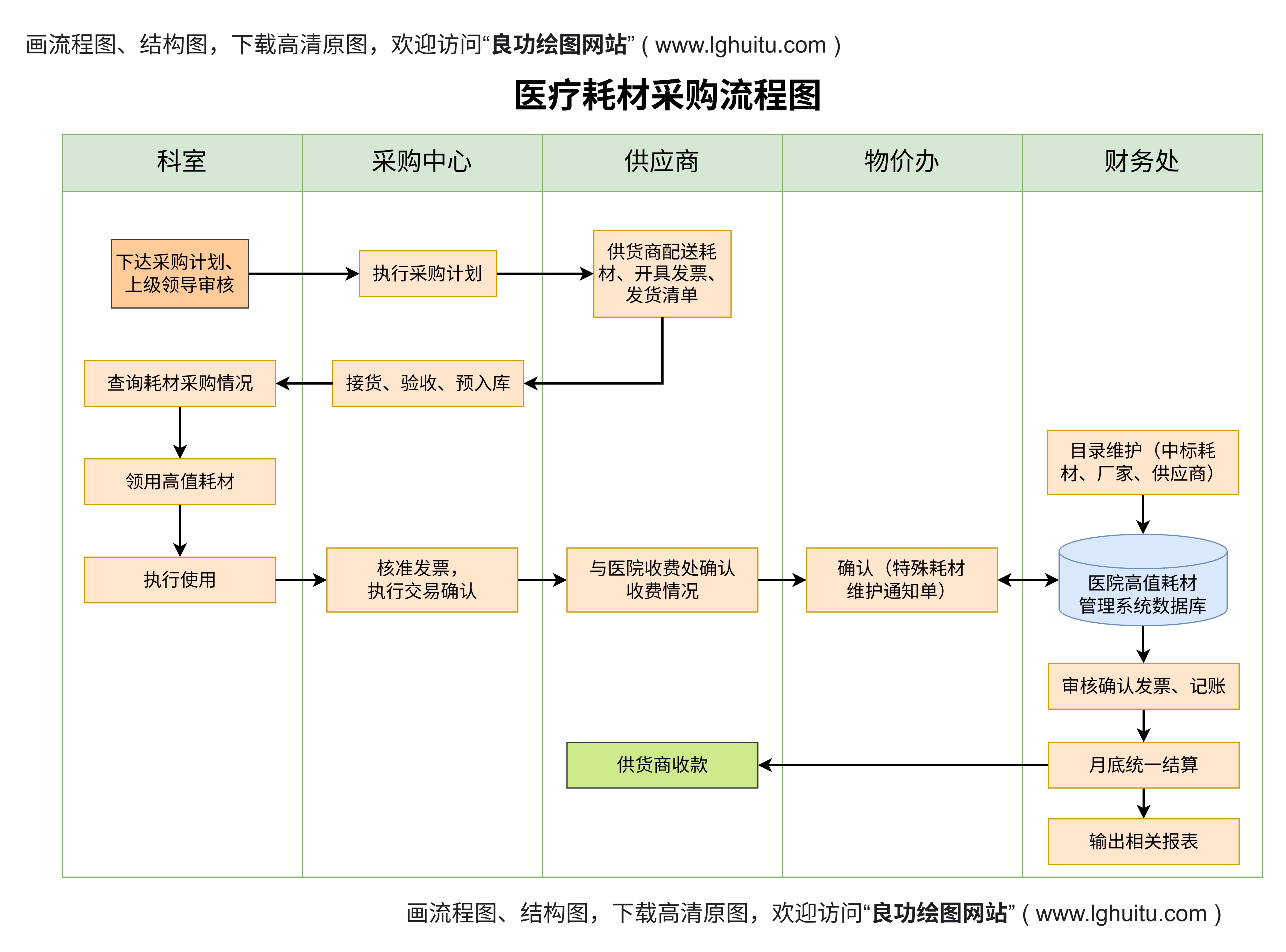
注册完成后,企业可以登录系统,进入“二类医疗器械备案”界面,填写相关产品信息。包括产品名称、型号、规格、技术参数、使用说明书等。企业还需要上传相关的产品资料,如质量管理体系文件、产品检测报告等。确保所提交的信息真实、准确且完整。

系统提交的资料会被相关监管部门进行审核。审核人员会根据法规要求,审查企业提交的所有资料是否符合备案标准。企业需要耐心等待审核结果,通常情况下,审核过程会有一定的时效性。如果资料不全或者不合规,审核人员可能会要求企业补充或修改。

审核通过后,企业将会收到来自监管部门的备案通知书,并获得备案号。备案号是医疗器械合法销售和流通的依据,因此企业要妥善保管。此时,企业可以开始正式销售该产品,并向市场推广。
尽管二类医疗器械备案的流程相对简便,但在实际操作中,企业仍然可能会遇到一些常见问题。比如资料提交不全、系统操作不当、审核结果不合格等。遇到这些问题时,企业应及时查阅相关资料,修正错误并重新提交。
通过以上步骤,企业便能够顺利完成二类医疗器械的备案申报,进入市场销售自己的产品。接下来我们将深入探讨更多备案过程中的注意事项以及如何提高申报成功率,确保企业顺利合规。
在实际操作中,许多企业往往会因为不熟悉流程或是资料准备不充分而导致备案申请失败。因此,在备案过程中,如何提高申报的成功率,确保顺利通过审核,是每个企业都应关注的重点。以下是一些实用的技巧和注意事项:
企业在进行备案申报之前,必须仔细阅读并理解国家相关法律法规,了解备案的具体要求。可以通过查询《医疗器械监督管理条例》及相关政策文件,确保自己的产品符合备案的标准。这样可以避免因对要求理解不透彻而提交不合格资料。
在网上提交备案申请时,企业需要准备齐全且符合规范的资料。这些资料包括产品技术文档、质量管理体系文件、生产许可证等。资料的准确性和完整性直接关系到备案是否能够顺利通过。因此,企业应认真检查提交的每一份文件,确保没有遗漏和错误。
如果企业在备案过程中遇到困难,选择一个专业的医疗器械服务机构或咨询公司也是一个不错的选择。这些机构通常会提供从产品设计、测试到备案申报的全套服务,可以大大提高备案通过的几率。他们也可以帮助企业完善资料、处理申报过程中的各类问题。
如果备案审核过程中,相关部门要求补充材料或修改资料,企业需要尽快响应并提供所需材料。迟迟不做回应可能会导致备案延期甚至无法通过。因此,保持与监管部门的良好沟通,并及时提交所需材料,是确保备案顺利完成的重要一环。
二类医疗器械备案的过程中,企业需要提供质量管理体系相关文件,证明其生产过程符合国家的质量要求。因此,企业应建立并维护完善的质量管理体系,并确保其符合《医疗器械生产质量管理规范》的要求。通过这种方式,企业可以提高备案的成功率,并为后续的产品生产和市场推广打下坚实的基础。
备案通过后,企业也不能掉以轻心。需要定期检查产品的质量和安全性,确保其始终符合相关标准。在市场推广过程中,企业还需密切关注产品的反馈,及时处理可能出现的问题。如果产品出现质量问题,企业应及时向监管部门报告,并采取必要的补救措施,以保障消费者的安全。
企业还需要定期进行备案更新。一些法规和技术标准可能会发生变化,企业需要及时根据新的法规要求进行备案信息的更新,确保产品始终符合最新的监管要求。
通过本文的详细介绍,相信您已经对二类医疗器械备案的网上申报流程有了充分的了解。从注册账户到最终获得备案号,每个环节都需要企业的高度关注和精准操作。只有掌握了流程的每一个细节,确保资料的准确性和合规性,企业才能顺利通过备案,进入市场,提供合格的医疗产品。
希望企业在备案过程中能够顺利顺利,抓住机遇,顺利打开市场的大门,成为行业中的佼佼者。