在中国,医疗器械市场的发展日新月异,而二类医疗器械凭借其广泛的应用和较高的市场需求,成为许多企业关注的重点。二类医疗器械想要进入市场并合法销售,必须取得相应的注册证。二类医疗器械的注册过程相对较为复杂,需要企业准备大量材料并经过多重审批。本文将为您详细解析二类医疗器械注册证申请流程,帮助您的产品顺利通过认证,赢得市场竞争优势。
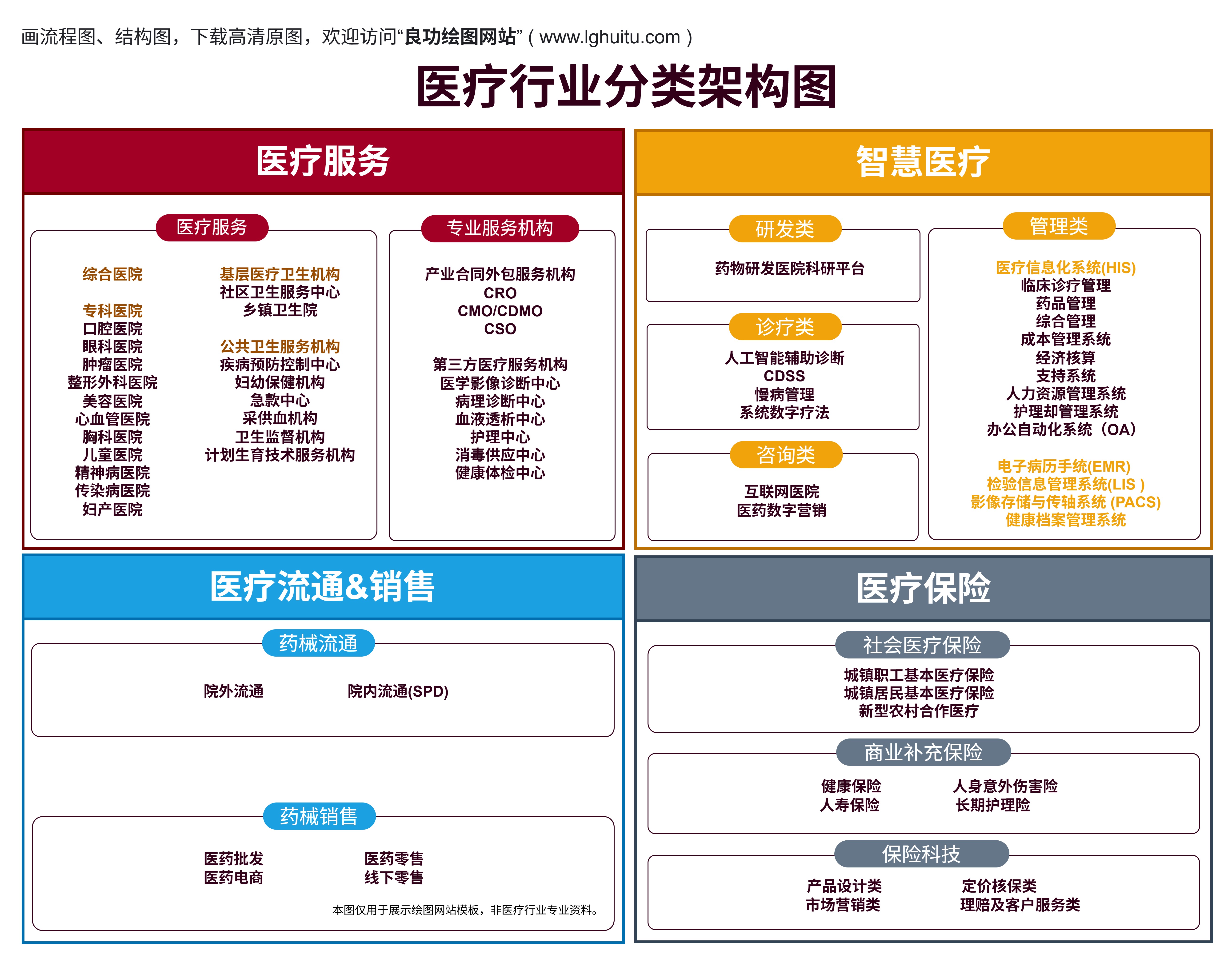
二类医疗器械是指那些对人体有一定风险,必须经过严格管理的医疗器械。与一类医疗器械相比,二类医疗器械的风险性相对较高,涉及的技术、性能要求也更为严格。常见的二类医疗器械包括监护仪、超声设备、医用影像设备、体外诊断试剂等。这些产品需要通过医疗器械注册获得合法市场准入。
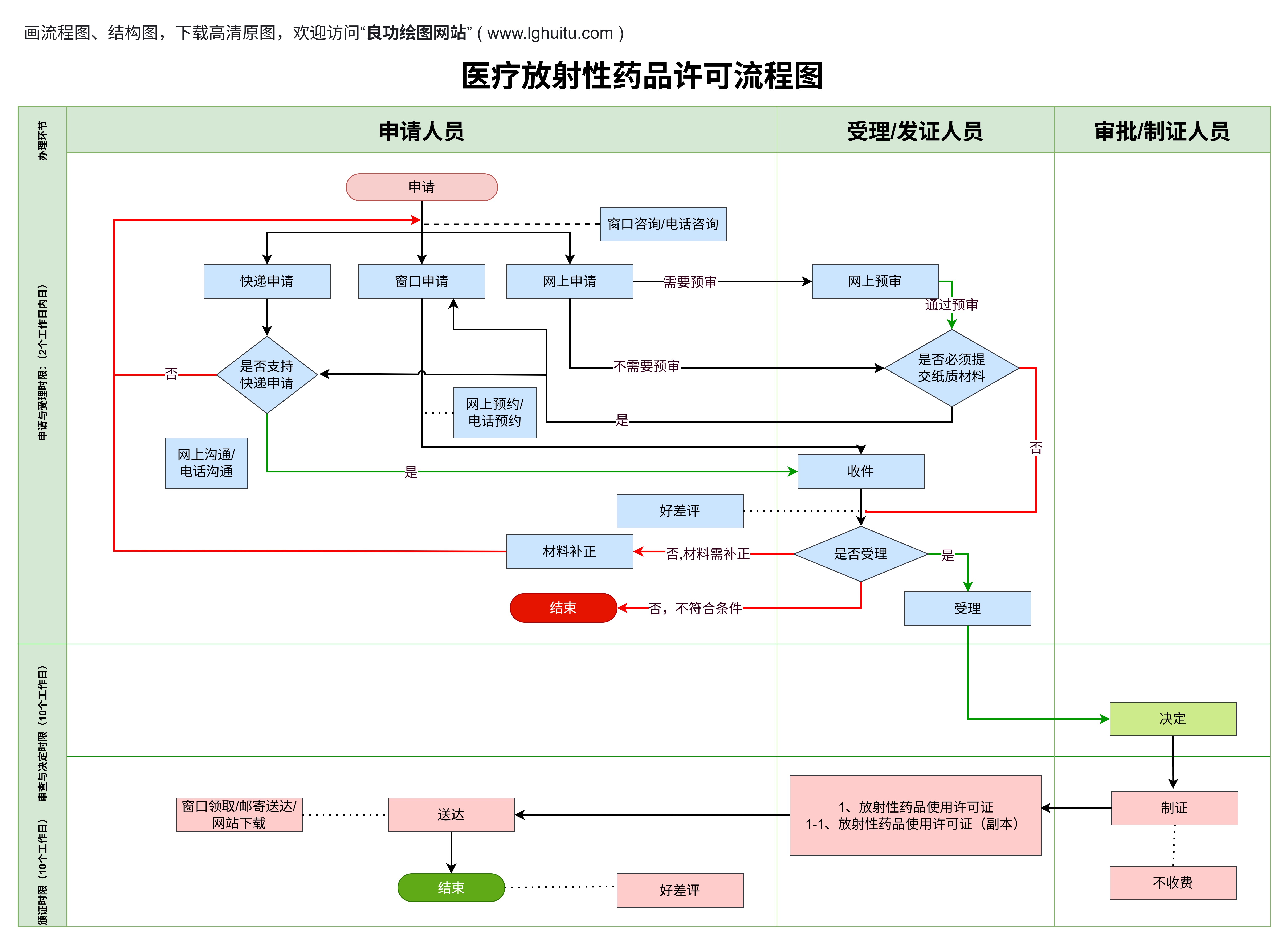
二类医疗器械的注册证申请分为多个步骤,每一步都需要严格按照规定操作,以确保产品能够顺利通过审批。以下是二类医疗器械注册证的主要申请流程:
在申请注册证之前,企业需要准备一系列的材料,包括但不限于:
产品技术文件:包括产品说明书、技术参数、产品设计图纸、生产工艺流程等。
质量管理体系文件:二类医疗器械需要符合GMP(良好生产规范)或ISO13485等质量管理体系的要求,因此企业需要提供相关的认证和审核文件。
临床试验数据:部分二类医疗器械需要进行临床试验,申请者需要提供相应的临床试验报告。
生产企业资质:企业需要提供相关的生产许可证、营业执照、税务登记证等材料。
材料准备完毕后,企业需要将所有申请材料提交至国家药品监督管理局(NMPA)或地方药监局进行审查。提交方式通常为电子申报和纸质申报相结合。企业在提交申请时需要确保所有文件齐全,避免因缺失材料而导致的审查延误。
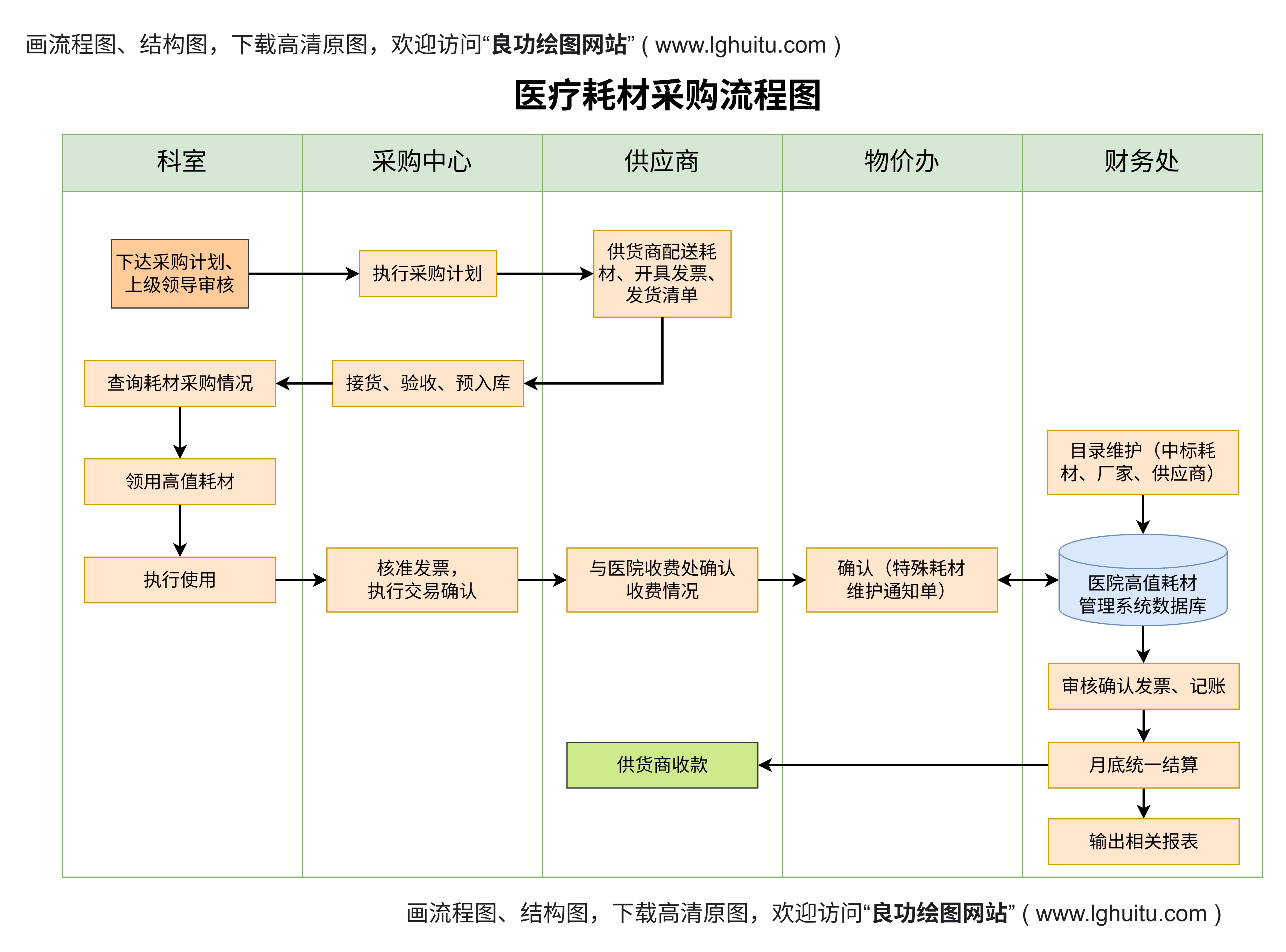
在提交申请后,药监局将对注册材料进行技术审查,审查的重点包括产品的安全性、有效性、质量管理体系等。对于部分复杂的二类医疗器械,药监局可能还会进行现场核查,核查内容包括生产设施、生产环境、人员资质等。
对于部分二类医疗器械,药监局会要求提供临床试验数据。这些数据将作为产品安全性和有效性的依据,药监局会对临床试验的设计、执行过程以及数据的真实性进行严格审查。企业需要确保临床试验符合相关规范,并及时提供所有必要的试验报告。

一旦通过技术审查和现场核查,药监局将根据审查结果做出决定,颁发二类医疗器械注册证。注册证是产品进入市场的重要凭证,获得注册证后,企业可以合法地销售该产品。
在申请二类医疗器械注册证的过程中,企业需要特别注意以下几个方面:
产品符合性:确保产品设计、生产符合相关标准和规定,避免因产品不符合要求而无法通过审核。
文件准备充分:申请材料必须完整且符合要求,否则可能会被退回或要求补充材料。
质量管理体系:完善的质量管理体系是二类医疗器械注册证申请的重要基础,企业应确保其质量管理体系符合国际和国内相关标准。
审查周期:二类医疗器械的注册审查周期较长,企业应提前做好时间安排,避免因注册证未能按时获得而影响产品上市。
通过这些步骤的精心准备,企业可以大大提高二类医疗器械注册证申请的成功率。
在前面的部分,我们已经详细了解了二类医疗器械注册证申请的基础流程和关键步骤。我们将进一步探讨如何优化申请过程,提升申请效率,并确保顺利获得注册证。
在开始申请之前,企业应当对二类医疗器械注册证的相关法规和政策进行充分了解,尤其是药监局最新的规定和要求。通过参加培训、咨询专家等方式,企业可以确保自身产品设计和申请材料符合最新的规定要求,从而避免因法规变化而导致的申请延误。

在申请过程中,企业与药监局保持良好的沟通至关重要。通过主动咨询、及时反馈,可以确保申请材料不会出现偏差,减少因为信息不对称而造成的错误。如果出现问题,药监局的反馈和指导也能帮助企业迅速纠正并继续推进注册过程。
对于需要进行临床试验的二类医疗器械,企业应尽早安排好临床试验的进程,确保临床数据的完整性和可靠性。试验过程中,企业需要密切关注临床试验的各项指标,确保数据真实、有效。技术审查过程中的反馈也需要企业及时响应,保证注册过程不受延误。
由于二类医疗器械注册证申请涉及的法规复杂且繁琐,企业可以考虑聘请专业的医疗器械注册代理机构。这些机构通常具有丰富的经验,能够帮助企业高效地准备申请材料,协助与药监局沟通,并确保申请过程顺利进行。选择合适的代理机构,可以大大缩短申请周期,并减少潜在的申请风险。
对于企业而言,二类医疗器械注册证不仅仅是一个法律合规的证明,它还具有重要的市场价值。获得注册证后,产品将获得更高的市场认可度,进入市场的渠道将更加畅通。注册证也为企业拓展国际市场提供了更多的机会。国际市场对于医疗器械的监管也非常严格,具有二类医疗器械注册证的企业在全球市场中更具竞争力。
二类医疗器械的注册证申请流程看似复杂,但只要企业在过程中认真准备,确保各环节符合规定,便能够顺利获得注册证并成功进入市场。通过了解申请流程的每个细节,合理优化申请策略,您将能够在激烈的市场竞争中脱颖而出,抓住更多的发展机遇。希望本文能够为您的二类医疗器械注册之路提供有力的支持,助力您的企业在医疗器械行业中迈向新的高峰。