在现代医学的快速发展中,药物的研发和创新已成为各国科技竞争的重要领域。随着科技的进步和人类对健康需求的增加,药物研发的过程越来越受到公众的关注。而在这一过程中,临床试验无疑是一个至关重要的环节。特别是二期和三期临床试验,它们是药物研发的核心阶段,每一阶段的成果都直接影响着药物的最终上市和应用。
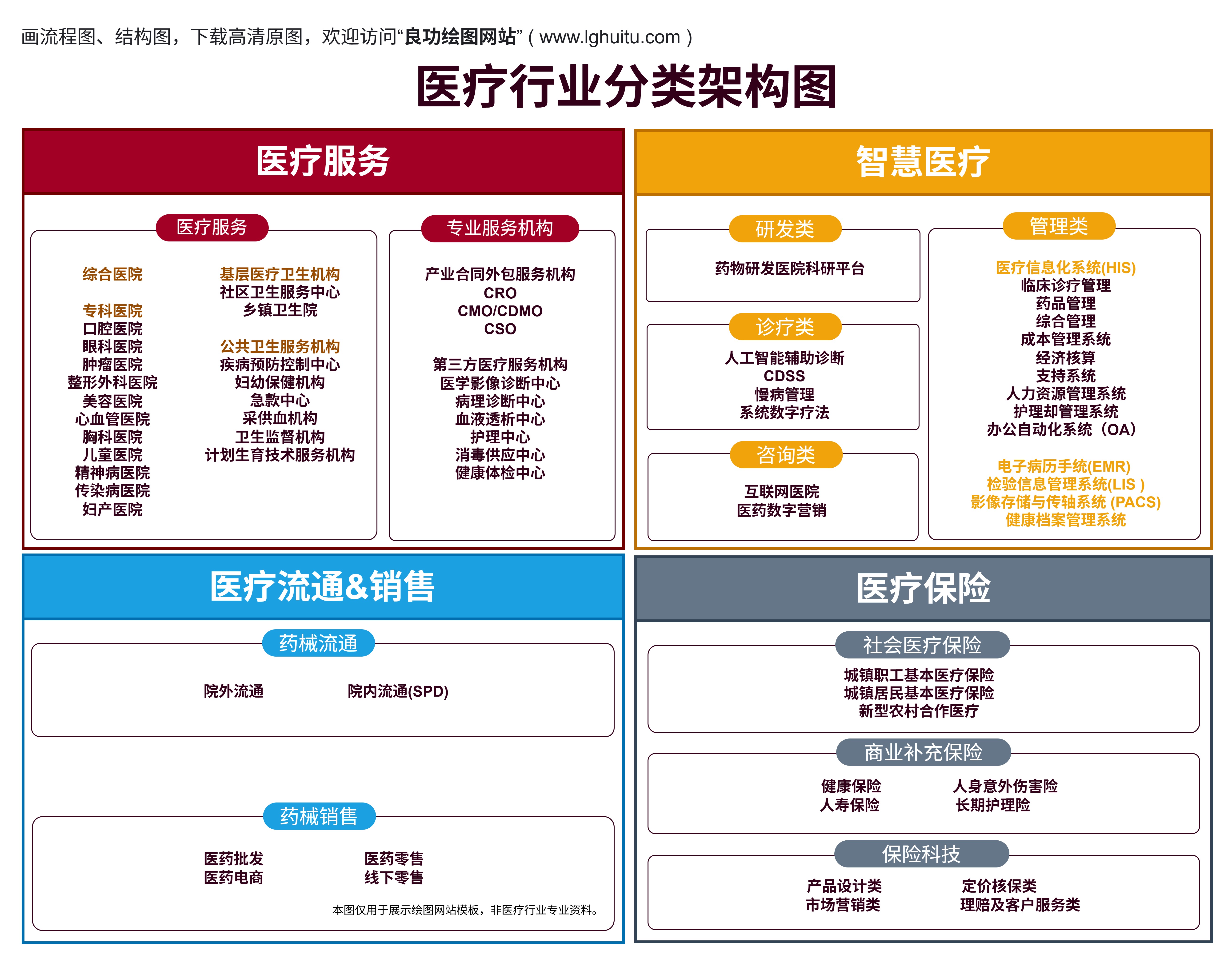
临床试验是指通过在人体身上进行的科学实验来验证药物的安全性、有效性以及适应症等。它通常分为几个阶段,包括临床前试验、一期试验、二期试验、三期试验和四期试验。每一个阶段都承载着不同的目标,而二期和三期试验作为关键的临床试验阶段,承担着将药物从实验室到临床应用的桥梁作用。
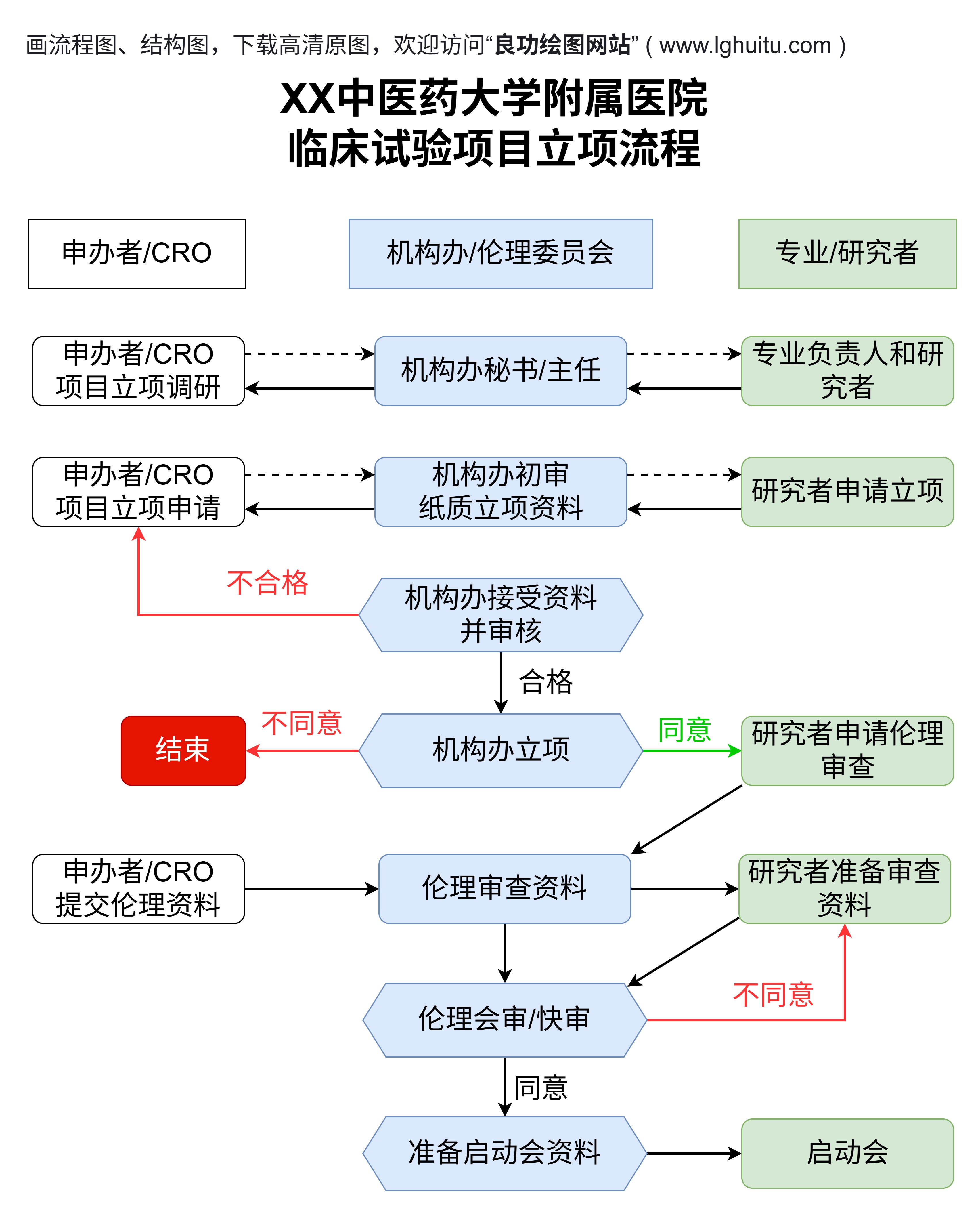
二期临床试验通常是在一期临床试验之后进行,它的主要目的是进一步评估药物的疗效,并继续观察药物的安全性。在这一阶段,药物已通过初步的安全性评估,能够被用于较大范围的患者群体中进行试验。
药物疗效的初步评估:二期试验的核心目标之一是确定药物是否能够在临床上发挥预期的效果。这一阶段的研究会选择特定的患者群体,通常是该药物预计治疗的疾病患者,通过随机对照试验的方式,测试药物的有效性。
副作用的监测:虽然二期试验的重点是药物的疗效,但它也会进一步收集关于药物副作用的数据。通过这种方式,研究人员可以确保药物的风险与收益之间处于合理的平衡。
需要注意的是,二期临床试验通常只有数百名患者参与,数据收集相对有限。因此,这一阶段的结果并不能完全证明药物在更大范围内的有效性和安全性。
三期临床试验是药物研发过程中的关键环节,也是药物最终能否获得批准上市的决定性阶段。在这一阶段,药物将进入更加广泛的临床验证,目的是确认药物在多种不同人群中的疗效与安全性,确保药物在实际应用中的可靠性。
三期试验通常涉及几千到几万名患者,涵盖了更广泛的疾病种类和人群背景。与二期试验相比,三期试验的规模和复杂性都要大得多,其研究目标包括:
药物疗效的确认:三期试验的目标之一是验证药物在多种不同患者群体中的疗效。研究人员会进一步确定药物在不同年龄、性别以及不同病理条件下的表现,确保其效果具有普适性。
药物副作用的全面评估:由于三期试验的规模较大,研究人员能够收集到更多的副作用数据。通过这些数据,药物在大规模人群中的风险评估会更加精准,研究人员可以判断药物在更广泛应用中的安全性。
药物与现有治疗方案的比较:在三期试验中,药物往往会与现有的标准治疗方案进行比较,以证明其相对优势。这一对比可以帮助医生在临床实践中决定是否采用该药物,特别是在某些疾病中,可能已经有了有效的治疗方法。
从以上的介绍中,我们可以看出,二期与三期临床试验的核心区别主要体现在试验的规模、研究目标以及数据收集的深度上。具体而言,二期试验更加注重药物的初步疗效和副作用的监测,而三期试验则着重于药物的广泛验证,包括更大范围的安全性评估和疗效确认。三期试验的参与者数量远大于二期试验,因此其结论也更加具有代表性和普适性。
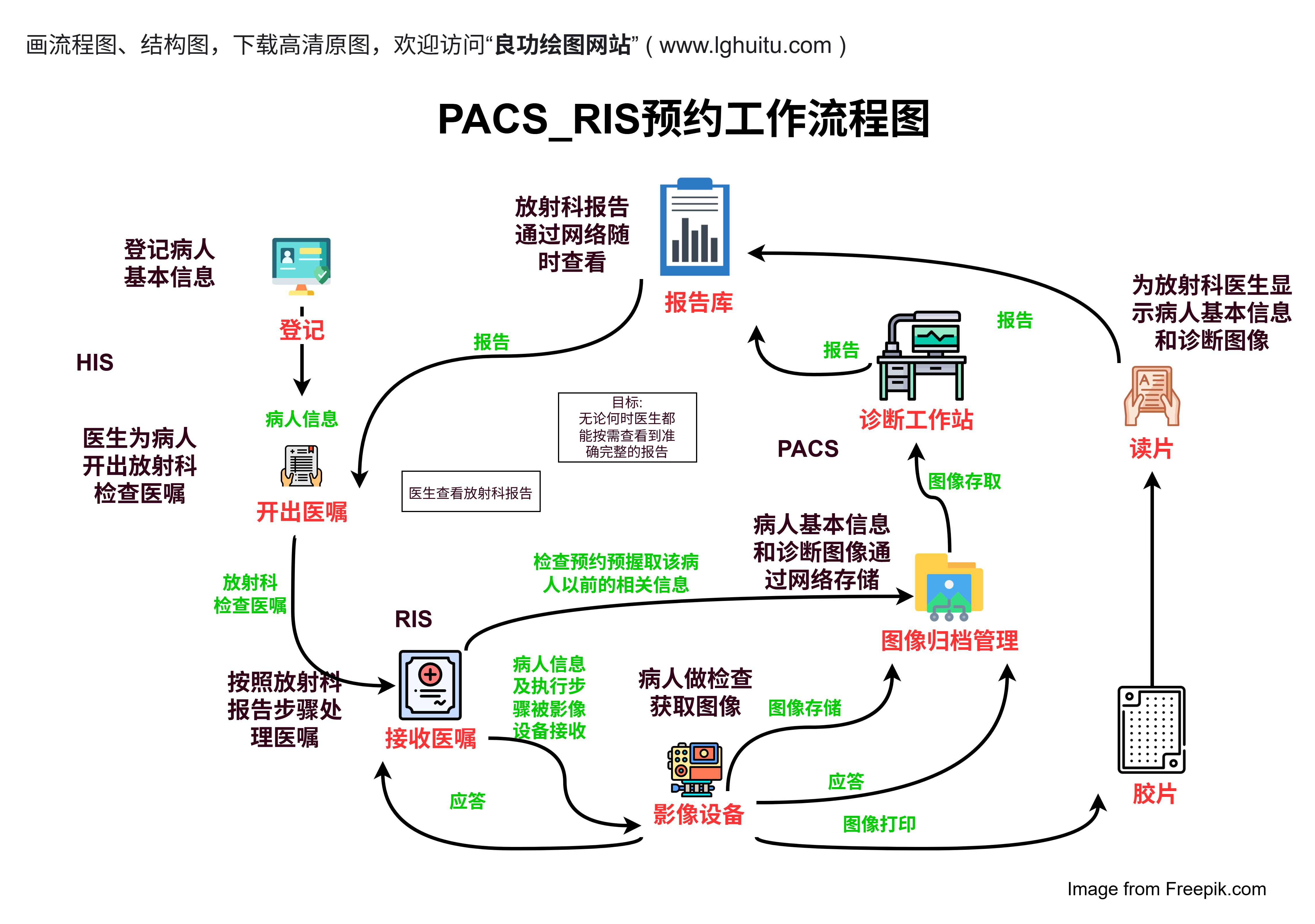
临床试验不仅是药物研发的必要步骤,更是确保公众健康安全的重要保障。在二期和三期试验阶段,研究人员会通过严格的科学方法和大量的数据分析,来评估药物的效果及其可能带来的风险。通过这些试验,药物在上市之前能够得到充分的验证,确保它在真实世界中的安全性和有效性。

对于药物研发公司来说,二期和三期临床试验是药物走向市场的关键一步。药物在这两个阶段的成功通过,意味着它有可能最终获得药品监管部门的批准,进入市场进行广泛应用。这一过程无疑是漫长且充满挑战的,但也是每一款成功药物背后的科学探索与努力。

随着临床试验的规模和复杂性不断扩大,相关的伦理问题和监管要求也变得越来越严格。在二期和三期试验中,研究人员必须确保所有参与者都在自愿的基础上参与试验,并且他们的隐私和数据得到充分保护。
药品监管部门,如中国的国家药品监督管理局(NMPA)和美国的食品药品监督管理局(FDA),对临床试验有着严格的监管要求。在试验过程中,任何不符合伦理或安全规定的行为都可能导致试验被暂停或中止。因此,二期和三期临床试验不仅需要科学的设计,还需要遵循严格的道德规范。
随着生物医学技术的进步,临床试验的模式和方法也在不断创新。个体化医疗、精准医学等新兴领域为药物研发带来了新的挑战和机遇。未来,二期和三期临床试验可能会更加注重患者的个体差异,利用大数据和人工智能技术进行更加精确的分析和预测。
二期与三期临床试验是药物研发中不可或缺的阶段,它们不仅关系到药物的安全与效果,还直接影响到公众的健康。因此,了解二期和三期临床试验的区别,不仅能够让我们更好地理解药物研发的过程,也能帮助我们认识到医学研究中每一个细节的重要性。