在全球制药行业中,医学临床试验是新药研发过程中至关重要的一环。如何管理和实施一项临床试验,不仅关系到药物的研发进程,更关乎患者的生命安全和药物上市后的效果。为了规范临床试验管理,提高临床研究的质量与效率,国家出台了《医学临床试验项目管理办法》,为临床试验项目的顺利进行提供了规范化的指导。作为制药企业、科研机构以及临床研究人员了解和遵守的基本法规,该办法具有重要的实践意义。
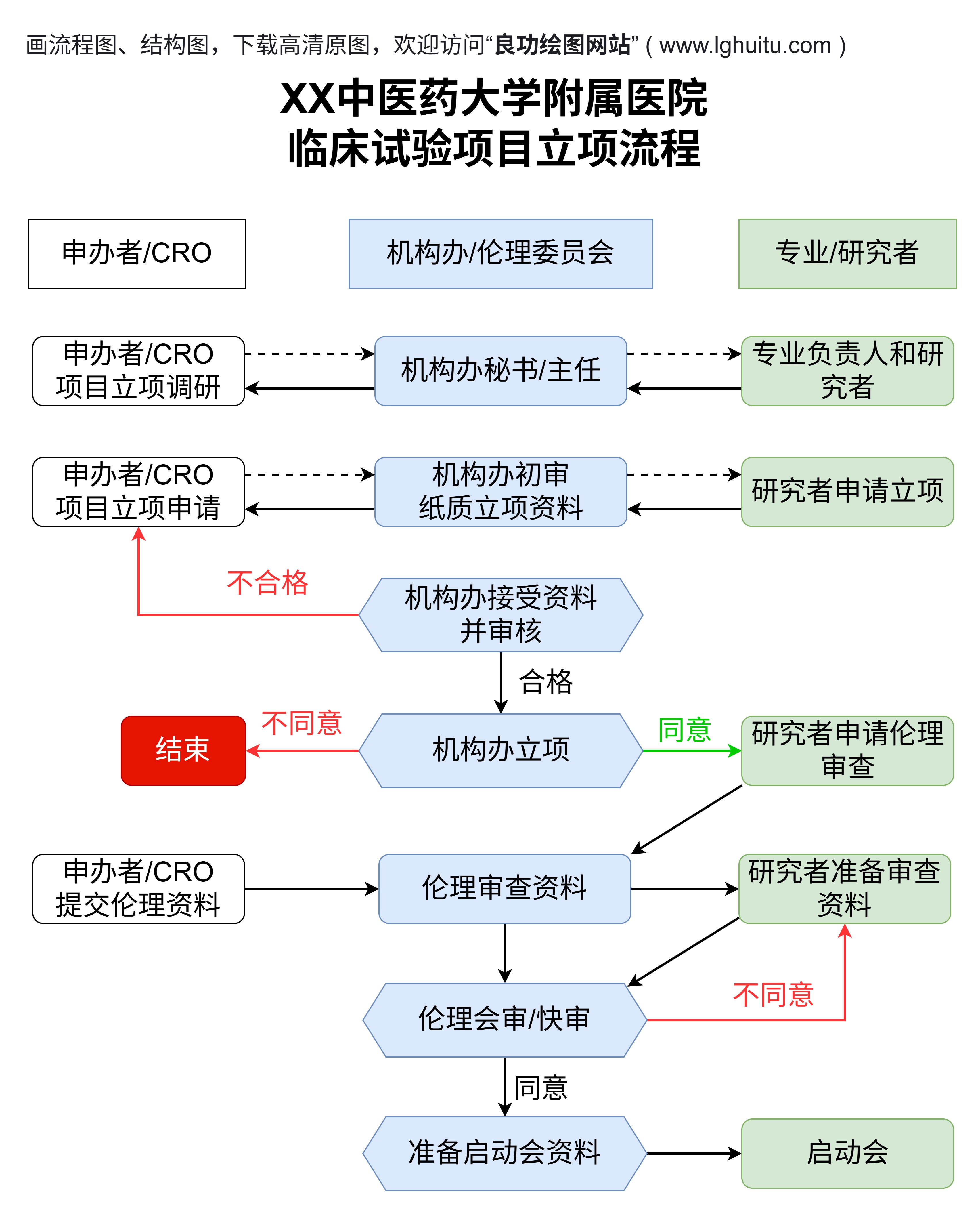
《医学临床试验项目管理办法》明确了临床试验项目的管理框架与责任分工,强调了各参与方的职责,并规定了临床试验全过程中的具体要求。这些内容为临床试验的实施、监督和评估提供了坚实的法律依据和规范支持。通过这一管理办法的实施,可以确保试验设计合理、数据采集科学、试验操作合规,从而有效提升药物研发效率和试验的成功率。
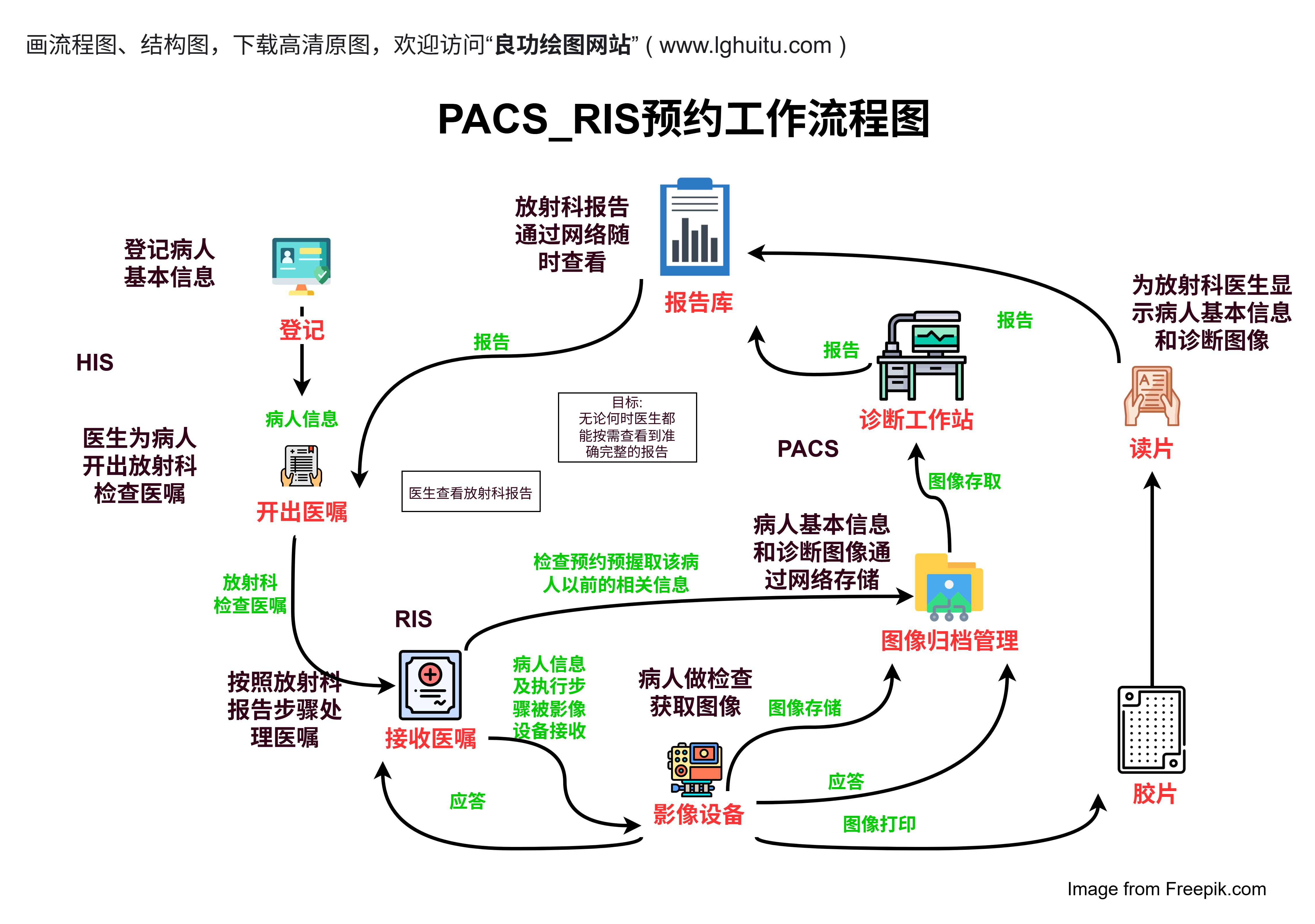
办法中明确了临床试验的基本流程和规范要求。包括试验前期的伦理审查、研究计划的制定、患者招募与知情同意的获得等。对试验设计、药物管理、数据收集、实验室检查等环节的管理作出了详细规定。这些细致的要求有助于减少临床试验中可能出现的误差,保证数据的准确性和可信度。

管理办法还强调了临床试验各环节的透明度和责任追溯。临床试验的各方责任方,包括药物研发公司、临床研究机构、临床医生、实验室等,都需要按照法规的要求进行各自的操作,确保每一环节都经过严格审核和监督。这不仅能避免试验过程中因不规范操作导致的失误,也能够确保患者在试验过程中的安全性,保障试验结果的科学性。

更重要的是,该管理办法还对临床试验的全过程管理进行了系统性规定,强调了试验数据的真实性、完整性和可追溯性。这一规定确保了试验过程中的每一个数据都可以被追溯和验证,为药物上市后的市场监督和药品安全性评估提供了保障。它为药物的临床试验合规性评审提供了重要依据,帮助监管部门对试验过程进行监督检查。
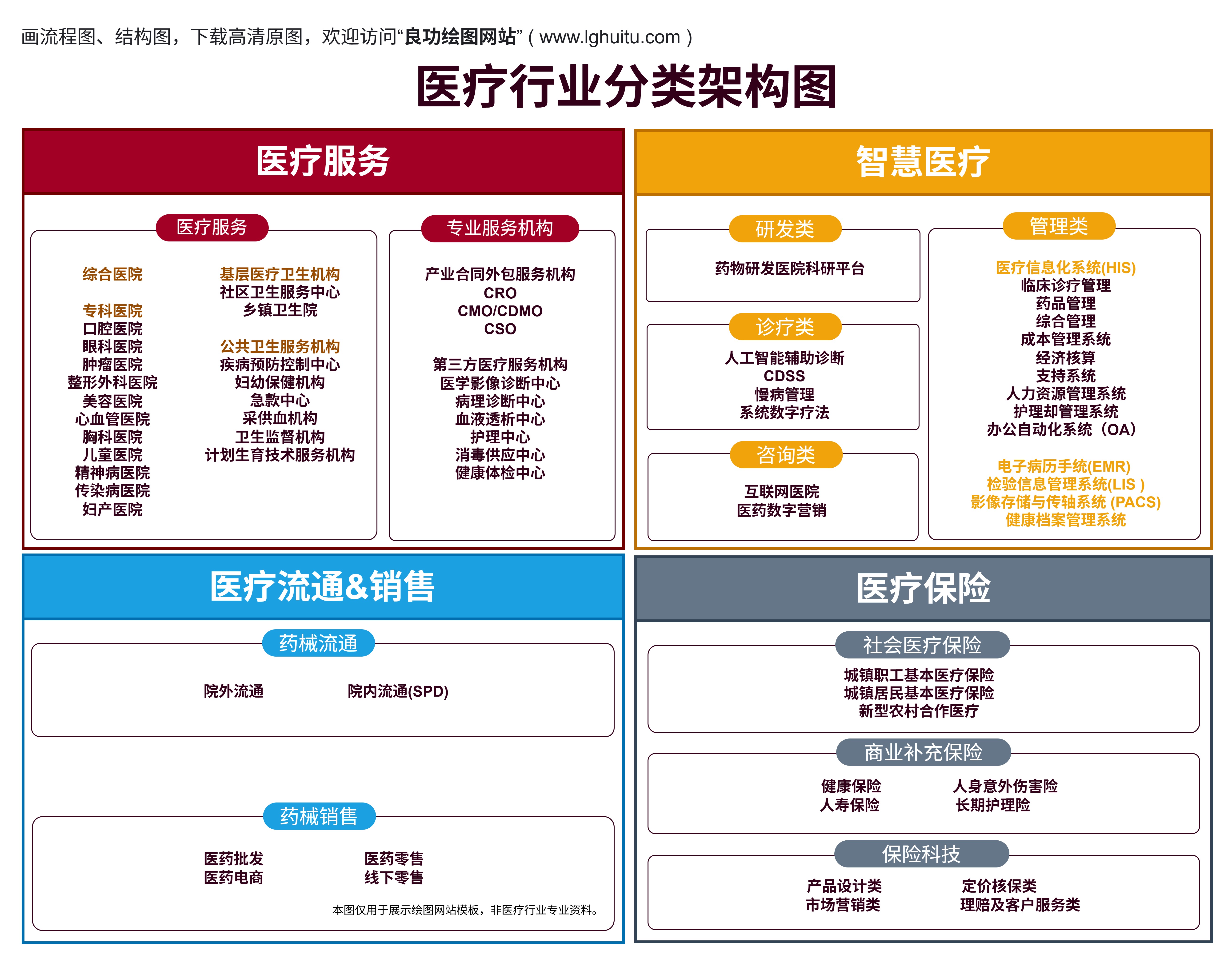
《医学临床试验项目管理办法》的出台,为医学临床试验的顺利进行奠定了坚实的基础,它不仅提升了药物研发的整体效率,也进一步保障了患者的健康与生命安全。作为医药行业的重要规范性文件,办法的实施将推动临床试验管理水平的不断提高,促进新药研发的健康发展。
随着《医学临床试验项目管理办法》的实施,药品研发领域的临床试验管理进入了一个新的阶段。这一管理办法不仅仅是对法规的补充,它更是对整个医学临床试验行业的一次深刻变革,为提升临床试验的质量、效率和透明度提供了全面的指导。
为了确保《医学临床试验项目管理办法》的顺利实施,相关部门需要加强对试验过程中的监督与检查。监管部门的作用不仅仅是对试验中的规范操作进行审查,还要对研究团队的专业水平进行评估,确保试验者具备足够的临床经验与科研能力。办法明确规定了临床试验的合规性要求,任何不符合规定的行为都将受到相应的处罚,这为整个行业设立了明确的规范,避免了法律漏洞的存在。
在实际应用中,《医学临床试验项目管理办法》进一步促进了跨学科、跨机构的合作。药物研发不仅仅是单一学科或单一机构的工作,而是一个涉及医学、药学、伦理学、数据科学等多个领域的复杂系统。办法要求各方在试验过程中保持良好的沟通与协作,通过数据共享、信息交流等方式,确保各方能够高效、精准地完成自己的任务。这种协作精神为临床试验的成功实施奠定了更加坚实的基础。
值得一提的是,随着科技的发展,临床试验中涉及的技术工具和数据处理手段也在不断更新换代。从电子数据采集到人工智能的辅助决策,越来越多的新技术开始应用于临床试验中。《医学临床试验项目管理办法》对这些技术的应用进行了适当的规范,确保这些技术能够在保障试验质量和数据安全的前提下,为药物研发提供有效的支持。比如,数据管理平台的引入,让各方能够实时监控试验进展,及时发现潜在问题并加以调整,极大提高了临床试验的效率和准确性。
办法还明确提出了对临床试验中患者权益的保护措施。在临床试验过程中,患者的知情同意是至关重要的一环。管理办法规定,临床试验必须得到伦理委员会的审查批准,试验前需要详细告知患者试验的目的、可能的风险与获益,确保患者能够在充分知情的情况下参与试验。这不仅是对患者权益的保护,也是对医学伦理的尊重。
随着国家对临床试验管理的不断加强和法规的逐步完善,制药行业的发展迎来了更加规范化的时代。通过《医学临床试验项目管理办法》的实施,整个行业的透明度、合规性和科学性都得到了显著提升。未来,随着各类药物研发的不断推进和临床试验管理办法的持续优化,医学临床试验将更加高效、安全,推动全球健康事业的进一步发展。